Amoxicilline - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Amoxicilline | ||
|---|---|---|
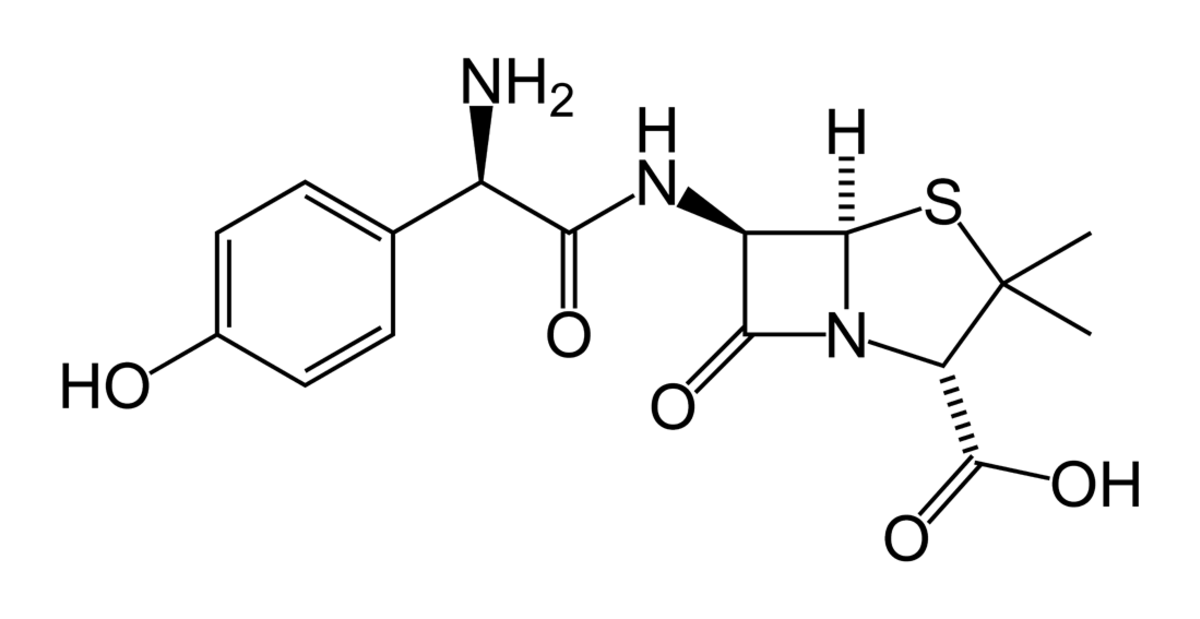
| ||
| Général | ||
| Nom IUPAC | ||
| No CAS | ||
| No EINECS | ||
| Code ATC | J01 | |
| DrugBank | ||
| PubChem | ||
| SMILES | ||
| InChI | ||
| Apparence | Poudre blanche | |
| Propriétés chimiques | ||
| Formule brute | C16H19N3O5S | |
| Masse molaire | 365,404 ± 0,021 g·mol-1 | |
| pKa | 2,8 | |
| Propriétés physiques | ||
| T° fusion | 194 °C | |
| Solubilité | 3 430 mg·l-1 eau à 25 °C | |
| Pression de vapeur saturante | 4,69.10-17 mmHg à 25 °C | |
| Précautions | ||
| | ||
| ||
| Phrases R : 42/43, | ||
| Phrases S : 22, 36/37, | ||
| Écotoxicologie | ||
| DL | 3 590 mg·kg-1 souris i.p. | |
| Classe thérapeutique | ||
| Antibiotique bêta-lactamine Aminopénicilline | ||
| Données pharmacocinétiques | ||
| Biodisponibilité | 95 % (orale) | |
| Métabolisme | Hépatique (< 30 %) | |
| Demi-vie d’élim. | 61,3 minutes | |
| Excrétion | Urinaire | |
| Considérations thérapeutiques | ||
| Voie d’administration | Orale Intraveineuse Intramusculaire | |
| Grossesse | Autorisée | |
| | ||
L'amoxicilline est un antibiotique bêta-lactamine bactéricide de la famille des aminopénicillines indiqué dans le traitement des infections bactériennes à germes sensibles.
Elle est également indiquée chez l'adulte dans le traitement de certains ulcères de l'estomac ou du duodénum causés par une bactérie (helicobacter pylori) en combinaison avec le metronidazole ou la clarithromycine et un inhibiteur de la pompe à protons.
Mode d'action
Principale : Interruption du processus de transpeptidation qui lie les peptidoglycanes de la paroi bactérienne. Les bêta-lactamines se lient et inactivent des cibles enzymatiques situées sur la paroi interne de la membrane bactérienne : les protéines de liaison des pénicillines, transpeptidases, carboxypeptidases, endopeptidases. L'inactivation des protéines PBP, A, 1BS, 2 et 3 provoque la mort cellulaire. Les bêta-lactamines inactivent également des inhibiteurs endogènes des autolysines bactériennes. (- Pharmacol and Therapeutics 1985;27:1-35.)
Sensible à la bêta-lactamase des staphylocoques et de certaines bactéries à Gram négatif. Résistance extra-chromosomique par plasmide R chez les entérobactéries, les bacilles Gram- et les staphylocoques.
Posologie
La dose d'amoxicilline utilisée en thérapeutique humaine s'échelonne de 50 à 200 mg·kg-1·j-1 en deux à quatre prises. Variant en fonction du mode d'administration, de l'infection à traiter.
Voie d'administration
L'amoxicilline simple, ou combinée à l'acide clavulanique, l'administration se fait par voie orale ou intraveineuse (injection ou perfusion)
Germes habituellement sensibles
- Les streptocoques β-hémolytiques.
- Les Streptococcus pneumoniae (pneumocoque) : l'amoxicilline est utilisée dans le traitement de la pneumonie typique et de la méningite à pneumocoque (par voie parentérale dans ces cas-ci).
- D'une manière générale, les espèces à Gram positif (streptocoques, Listeria, Clostridium perfringens). Pour ces bactéries, l'amoxicilline constitue le traitement de première ligne tant la sensibilité des germes est grande. Son action contre le staphylocoque doré est bonne également à condition que la souche ne produise pas de β-lactamase, ce qui est de plus en plus fréquent.
- Certaines espèces à Gram négatif fragiles, aérobies et anaérobies (gonocoque, méningocoque, Helicobacter pylori, Campylobacter, Leptospira, Borrelia, Treponema, Fusobacterium...)
Ce spectre peut être amélioré en combinant l'amoxicilline avec un inhibiteur de β-lactamase, c'est-à-dire une substance qui protège l'amoxicilline contre les enzymes défensives anti-β-lactamines produites par certaines bactéries. Par exemple, une combinaison d'amoxicilline et d'acide clavulanique (association dont le nom commercial est Augmentin) inclut dans son spectre toutes les souches dHaemophilus influenzae, toutes les Moraxella, encore plus dEscherichia coli, et de nombreuses souches de Proteus.