Clarithromycine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Clarithromycine | ||
|---|---|---|
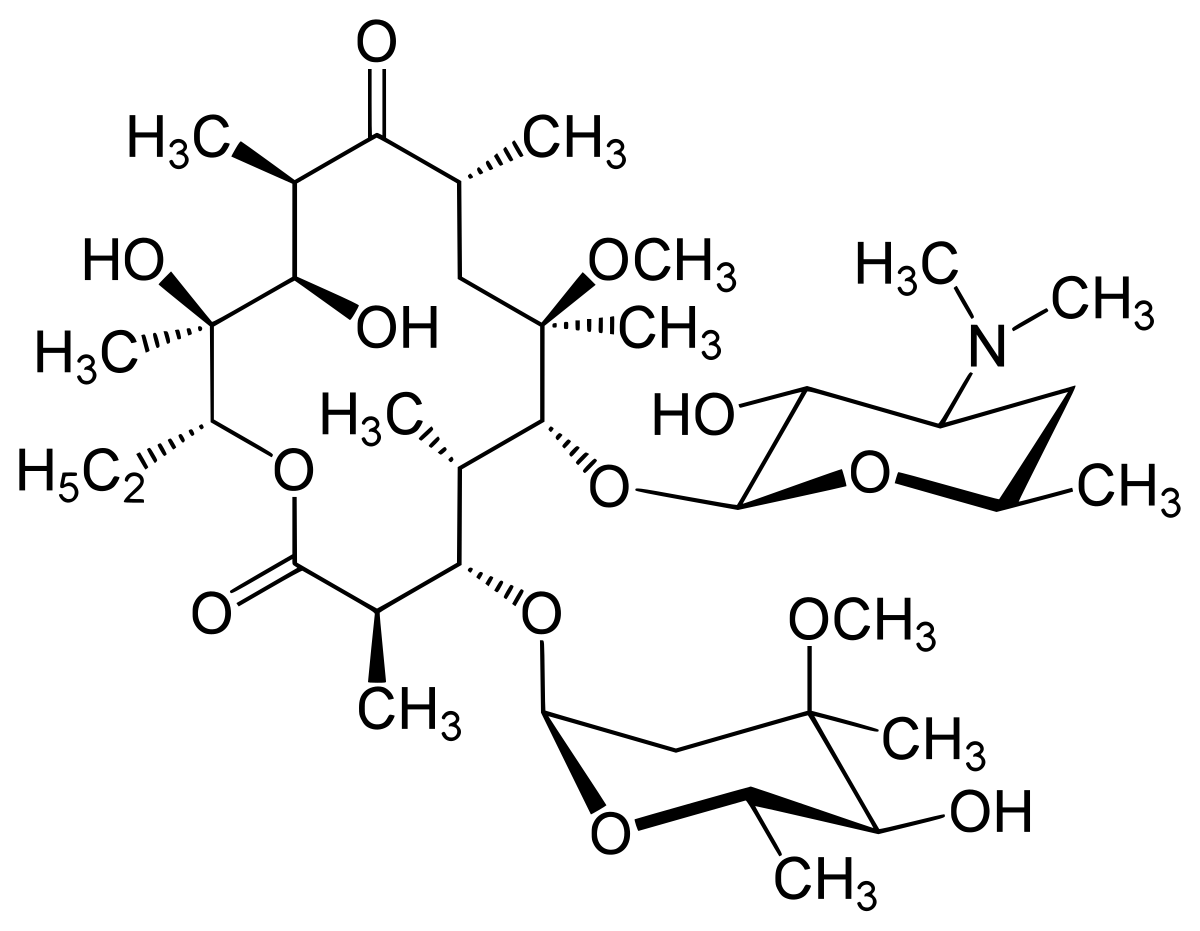
| ||
| Général | ||
| Nom IUPAC | ||
| No CAS | ||
| Code ATC | J01 | |
| DrugBank | ||
| PubChem | ||
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule brute | C38H69NO13 | |
| Masse molaire | 747,9534 ± 0,0393 g·mol-1 | |
| pKa | 8.99 à 25 °C | |
| Propriétés physiques | ||
| T° fusion | 217 à 220 °C | |
| Solubilité | 0,342 mg·l-1 eau à 25 °C (estimation) | |
| Précautions | ||
| | ||
| ||
| Phrases R : 22, | ||
| Écotoxicologie | ||
| DL | 1 230 mg·kg-1 souris oral 173 mg·kg-1 souris i.v. >5 000 mg·kg-1 souris s.c. 850 mg·kg-1 souris i.p. | |
| Données pharmacocinétiques | ||
| Métabolisme | Foie | |
| Considérations thérapeutiques | ||
| Grossesse | C (États-Unis) ou B3 (Australie) | |
| | ||
La clarithromycine est un antibiotique macrolide utilisé pour traiter les pharyngites, les angines, les sinusites aiguës maxillaires, les complications bactériennes aiguës de la bronchite chronique, les pneumonies (en particulier les pneumonies atypiques associées à Chlamydia pneumoniae), les infections cutanées, et, chez les patients porteurs de VIH, pour prévenir et traiter le Mycobacterium avium complex disséminé ou MAC.
De plus, on l'utilise parfois pour traiter les légionelloses et l'éradication d'helicobacter pylori responsable de maladies ulcéreuses de l'estomac.
Historique
La molécule, d'invention japonaise, a été commercialisée en 1991 dans ce pays et en occident par le laboratoire Abbott.
Mécanisme d'action
La clarithromycine empêche la croissance bactérienne en interférant avec la synthèse des protéines bactériennes.
Formes disponibles
Granules flottantes pour enfants, ou comprimés enrobés
Effets secondaires
Nausées, vomissements, douleurs d'estomac, diarrhée, candidose, manifestations cutanées allergiques, acouphène.
Métabolisme
La molécule de clarithromycine est partiellement métabolisée au niveau du foie par le cytochrome P 450 3A4. La molécule de clarithromycine inactif lors de l’absorption est ensuite transformée par une réaction de phase 1 en 14-OH-clarithromycine, qui est le métabolite actif, donc celui qui a un effet pharmacologique au niveau tissulaire sur les ribosomes. Elle est aussi métabolisée par le foie dans une moindre mesure en descladinosyl-clarithromycine et N-déméthyl-clarithromycine. La biodisponibilité de la clarithromycine qui est d’environ de 50 % nous renseigne sur le fait que l’effet de premier passage hépatique sur cette molécule est généralement de façon modérée. Par contre, il a été établi que la clarithromycine inhibait l’isoenzyme 3A4 du cytochrome P450 du foie et de l’intestin, et donc les concentrations des médicaments qu’une personne prend et qui sont métabolisées par ce type d’enzyme s’en trouvent augmentées et prolongées lorsqu’on les administre avec de la clarithromycine. Il faut donc être vigilant et surveiller attentivement les concentrations sériques de ces médicaments.
La clarithromycine est aussi excrétée par les reins, la 14-OH-clarithromycine est le principal métabolite que l'on retrouve dans l'urine.