Carbonate de magnésium - Définition
Source: Wikipédia sous licence CC-BY-SA 3.0.
La liste des auteurs de cet article est disponible ici.
La liste des auteurs de cet article est disponible ici.
Introduction
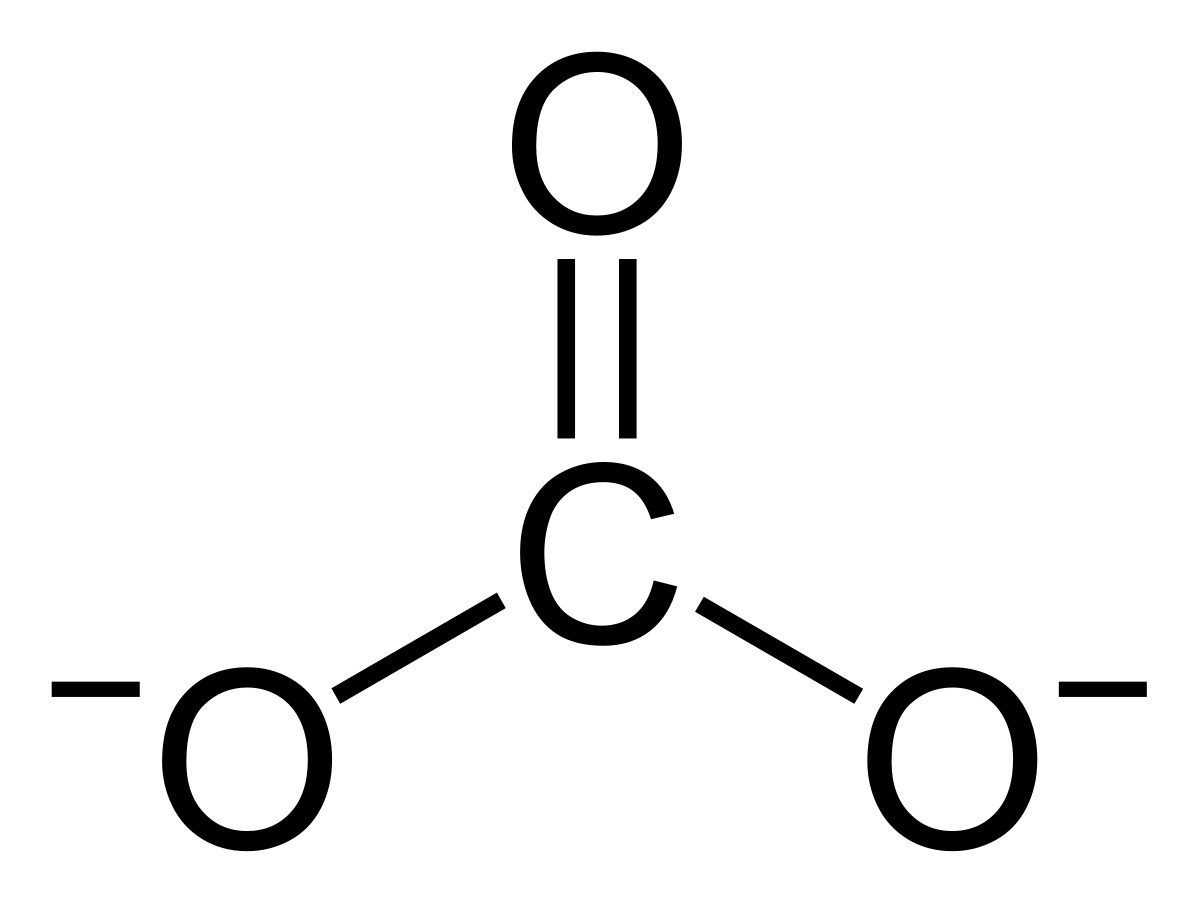
| Carbonate de magnésium | |
|---|---|
| |
| Général | |
| Nom IUPAC | |
| Synonymes | magnésite magnésie blanche |
| No CAS | |
| No EINECS | |
| Code ATC | A02 A06 |
| PubChem | |
| ChEBI | |
| SMILES | |
| InChI | |
| Apparence | poudre blanche |
| Propriétés chimiques | |
| Formule brute | MgCO3 |
| Masse molaire | 84,3139 ± 0,0023 g·mol-1 |
| Propriétés physiques | |
| T° fusion | 350 °C (décomposition) |
| Solubilité | 0,106 g·l-1 (eau,20 °C) |
| Masse volumique | 2,96 g·cm-3 à 20 °C |
| Thermochimie | |
| S0 | 65,84 J·K-1·mol-1 |
| ΔH0 | -1 111,69 kJ·mol-1 |
| Précautions | |
| | |
|
0 1 0 | |
| | |
Le carbonate de magnésium (MgCO3) est un solide de couleur blanche, qui se trouve à l'état minéral dans la nature. C'est un composant de la magnésite. Sous forme de poudre, le carbonate de magnésium est utilisé comme anti-transpirant dans de nombreux sports, connu sous le nom de magnésie.
Propriétés physico-chimiques
A des températures supérieures à 400 °C, une décarboxylation a lieu et forme l'oxyde de magnésium
Utilisation
Sous forme de poudre appelée couramment « magnésie », le carbonate de magnésium est utilisée dans certains sports comme la gymnastique artistique, l'escalade ou l'haltérophilie pour assécher la paume des mains.
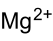

![MgCO_3 \ \xrightarrow[]{\Delta} \ MgO \ + \ CO_2](https://static.techno-science.net/illustration/Definitions/autres/1/1431b259c8270478a991061e0b4f7549_38a56088edd0ece7f9d08bc7b12eab5f.png)


















































