Formule de Lewis - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
En chimie, une formule de Lewis est une représentation en 2 dimensions permettant de représenter la structure électronique externe des atomes composant une molécule. Inventée par Gilbert Lewis, elle se base sur la topologie de la molécule (connexion entre les atomes par des liaisons covalentes).
Définition
La représentation de Lewis consiste à définir l'allocation des électrons sur ou entre les atomes de la molécule. Seuls les électrons de valence sont considérés. On obtient ainsi une certaine vision de la structure électronique de la molécule par ses doublets libres, ses doublets liants (liaisons σ et π), ses lacunes et ses éventuels électrons célibataires (dans le cas des radicaux).
Un code de représentation
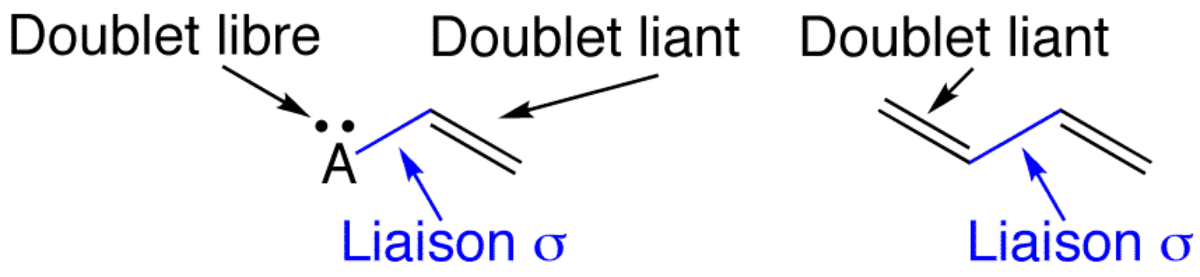
Dans cette représentation, les électrons célibataires sont notés par des points et les paires d'électrons par des traits (plus rarement par deux points). Les traits peuvent être localisés sur un atome (doublet libre ou non liant) ou entre les atomes (doublet liant, liaison covalente).
Construction
La construction du modèle de Lewis d'une molécule se base sur la détermination de la valence des atomes la constituant, ce qui définit le nombre total d'électrons externes de la molécule. L'établissement de la structure de Lewis, consiste à répartir ces électrons sur le squelette moléculaire tout en respectant la règle de l'octet. Le squelette moléculaire est fait de liaisons σ qui mobilisent chacune 2 électrons sur le total des électrons de valence de la molécule. Une structure de Lewis est d'autant plus probable qu'elle respecte l'octet et ne présente pas de séparation de charge.
Exceptions
Quelques atomes sont connus pour violer la règle de l'octet. On parle d'hypervalence (soufre, phosphore, xénon) lorsqu'il y a plus de 8 électrons autour de l'atome, et de d'hypovalence lorsqu'il y a moins de 8 électrons (cas du bore notamment). Les atomes d'hydrogène ont 2 électrons autour d'eux dans la molécule. On parle pour eux de règle du duet.
Lorsqu'un atome a exactement 6 électrons autour de lui, on parle d'une lacune (représentée par un petit rectangle vide). Le bore et les carbocations ont une lacune. La lacune confère à l'atome une acidité particulière pour les électrons voisins (acidité de Lewis).
Validité
Une structure de Lewis est une représentation simplifiée de la structure électronique. Les notions d'hypervalence ou d'hypovalence par exemple sont des caricatures de la densité électronique autour d'un atome. Au XXIe siècle, ils font encore l'objet de recherche.
La représentation de Lewis présente des cas problématiques :
- Dans le cas du dioxygène, la représentation de Lewis donne : . Dans cette représentation, chaque électron se trouve en apparié (sous forme de doublet), ce qui donnerait à la molécule de dioxygène des propriétés diamagnétiques. Or celle-ci est paramégnétique, c'est-à-dire qu'elle présente des électrons non-appariés.
- Dans le cas du borane (BH3), le bore partage ses trois électrons avec les trois atomes d'hydrogène qui l'entourent, en formant trois liaisons simples. Il est alors entouré uniquement de six électrons, ce qui contredit la règle de l'octet. C'est aussi le cas de tous les composés trivalents du bore
Malgré ses limites, le modèle de Lewis est un outil indispensable pour les chimistes et permet d'expliquer la composition et la réactivité de nombreux composés, surtout en chimie organique. Par contre, il ne peut pas expliquer la réactivité des éléments de transition.