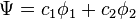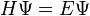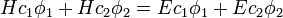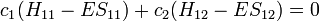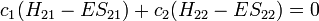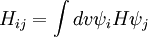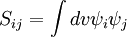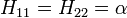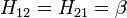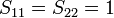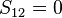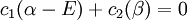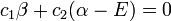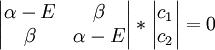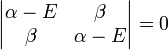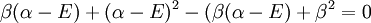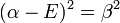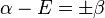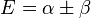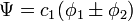Méthode de Hückel - Définition
La liste des auteurs de cet article est disponible ici.
Exemple de l'éthène
Dans le traitement selon Hückel de l'éthylène, l'orbitale moléculaire
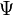
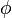

Cette équation est alors introduite dans l'équation de Schrödinger :
où
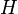
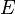
L'équation est alors multipliée par


où :
Les hamiltoniens entièrement diagonaux
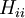
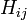
Un autre des postulats sont que l'intégrale de recouvrement entre deux orbitales atomiques est nulle :
Ceci conduit à deux équations homogènes :
avec un total de cinq variables. Après avoir converti cet ensemble en notation matricielle:
La solution triviale fournit les deux coefficients des fonctions d'ondes c égaux à zéro, ce qui n'est pas extrêmement utile pour la résolution. L'autre solution non triviale est :
qui peut être résolue en développant son déterminant:
ou
et
Après normalisation, les coefficients sont obtenus :
La constante β dans le terme d'énergie est négatif et ainsi α + β est l'énergie la plus basse, correspondant à l'orbitale la plus haute occupée (HO) et α - β à la plus basse vacante (BV).