Structure des protéines - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
La structure des protéines est la composition en acides aminés et la conformation en trois dimensions des protéines. Elle décrit la position relative des différents atomes qui composent une protéine donnée.
Les protéines sont des macromolécules de la cellule, dont elles constituent la « boîte à outils », lui permettant de digérer sa nourriture, produire son énergie, de fabriquer ses constituants, de se déplacer, etc. Elles se composent d'un enchaînement linéaire d'acides aminés liés par des liaisons peptidiques. Cet enchaînement possède une organisation tridimensionnelle (ou repliement) qui lui est propre. De la séquence au repliement, il existe 4 niveaux de structuration de la protéine.
Structure primaire
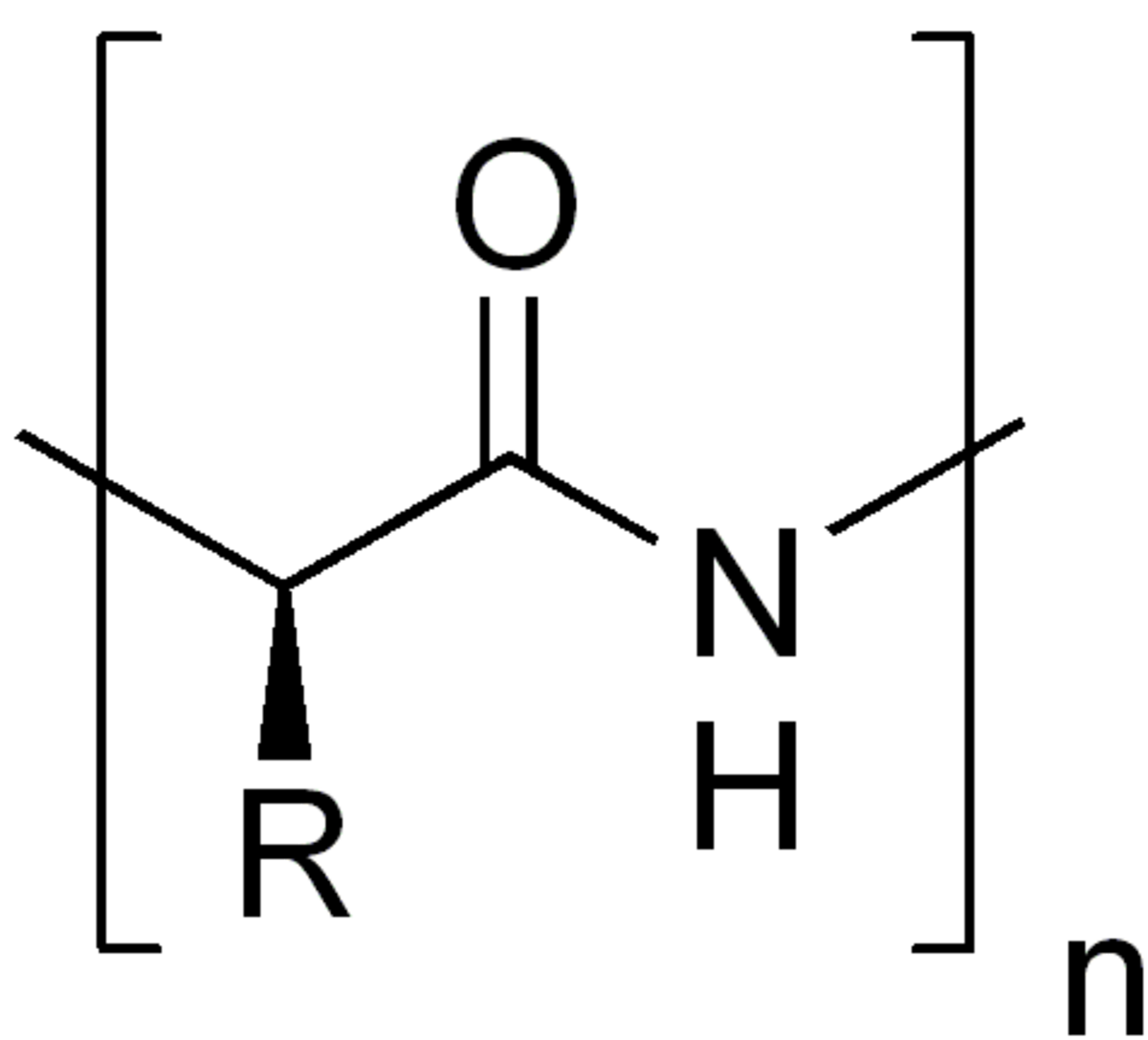
La structure primaire, ou séquence, d'une protéine correspond à la succession linéaire des acides aminés (ou résidus) la constituant. Les protéines sont donc des polymères d'acides aminés, reliés entre eux par des liaisons peptidiques.La structure primaire d'une protéine est le fruit de la traduction de l'ARNm en séquence protéique par le ribosome. C'est grâce au code génétique que l'information génétique (sous forme d'ARN) est traduite en acides aminés. Concrètement, la structure primaire est représentée par une succession de 20 lettres (code 1 lettre) différentes correspondant aux 20 acides aminés.
| Nom | code 3 lettres | code 1 lettre | Abondance relative (%) E.C. | M | Chargé, Polaire, Hydrophobe |
|---|---|---|---|---|---|
| Alanine | ALA | A | 13.0 | 71 | H |
| Arginine | ARG | R | 5.3 | 157 | C+ |
| Asparagine | ASN | N | 9.9 | 114 | P |
| Aspartate | ASP | D | 9.9 | 114 | C- |
| Cystéine | CYS | C | 1.8 | 103 | P |
| Glutamate | GLU | E | 10.8 | 128 | C- |
| Glutamine | GLN | Q | 10.8 | 128 | P |
| Glycine | GLY | G | 7.8 | 57 | - |
| Histidine | HIS | H | 0.7 | 137 | P,C+ |
| Isoleucine | ILE | I | 4.4 | 113 | H |
| Leucine | LEU | L | 7.8 | 113 | H |
| Lysine | LYS | K | 7.0 | 129 | C+ |
| Méthionine | MET | M | 3.8 | 131 | H |
| Phénylalanine | PHE | F | 3.3 | 147 | H |
| Proline | PRO | P | 4.6 | 97 | H |
| Sérine | SER | S | 6.0 | 87 | P |
| Thréonine | THR | T | 4.6 | 101 | P |
| Tryptophane | TRP | W | 1.0 | 186 | P |
| Tyrosine | TYR | Y | 2.2 | 163 | P |
| Valine | VAL | V | 6.0 | 99 | H |
| Sélénocystéine | SEC | U | rare | - | |
| Pyrrolysine | PYL | J | rare | - |
Polarité, extrémités N- et C-terminales
La séquence primaire d'une protéine a un sens bien défini ou polarité. Le premier acide aminé de la séquence de la protéine est par convention celui qui possède une extrémité amine libre, on parle d'extrémité N-terminale ou de N-terminal. De manière symétrique le dernier acide aminé est celui qui possède une extrémité carboxylate libre, on parle de C-terminal.
Exemple d'une séquence d'acide aminé, l'α-lactalbumine humaine :
MRFFVPLFLVGILFPAILAKQFTKCELSQLLKDIDGYGGIALPELICTMFHTSGYDTQAI VENNESTEYGLFQISNKLWCKSSQVPQSRNICDISCDKFLDDDITDDIMCAKKILDIKGI DYWLAHKALCTEKLEQWLCEKL
Il existe des méthodes expérimentales de détermination de la structure primaire.

















































