Phénylalanine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Phénylalanine | |
|---|---|
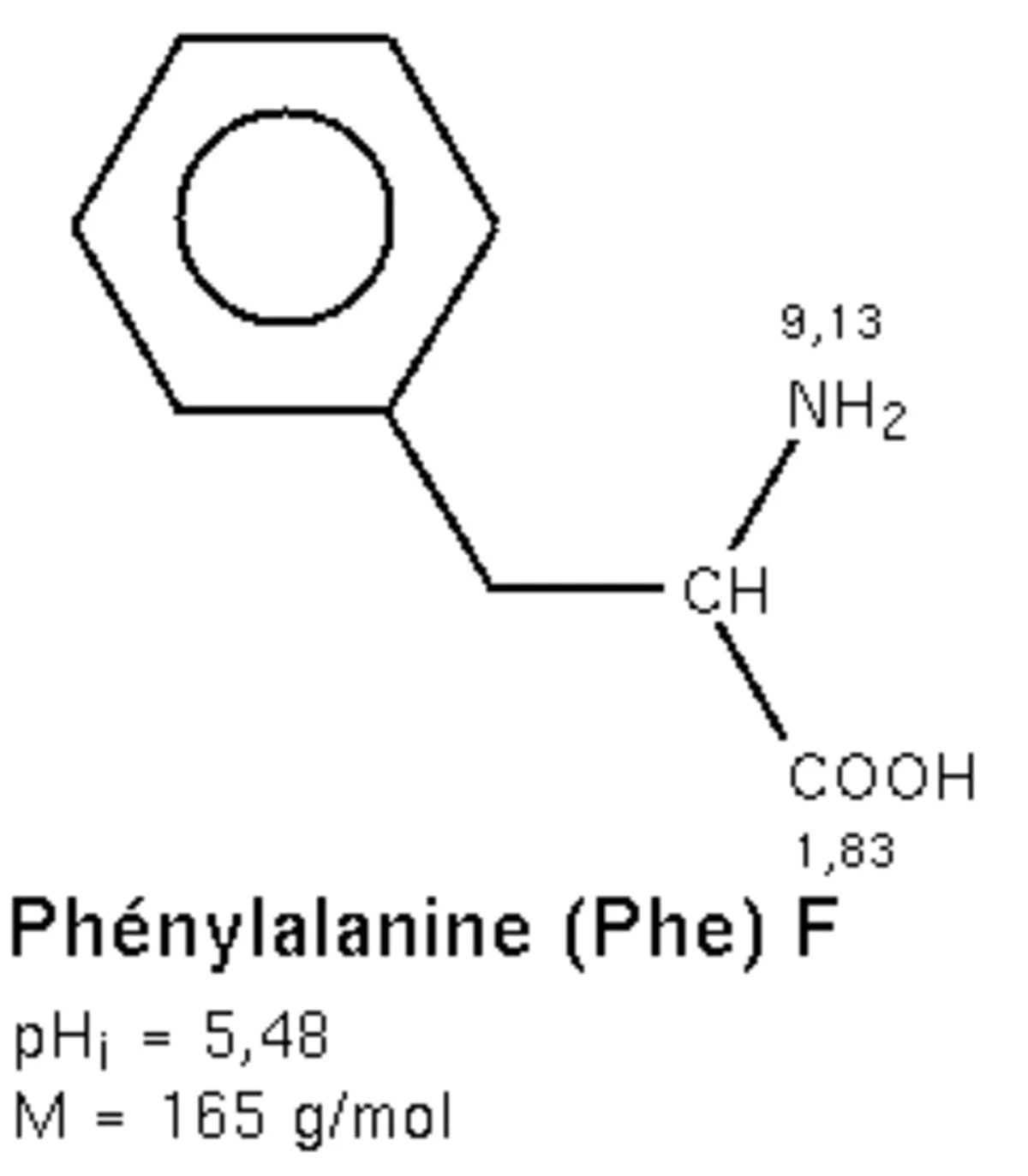
| |
| Général | |
| Nom IUPAC | |
| Synonymes | F, Phe |
| No CAS | (racémique) (L) ou S(–) (D) ou R(+) |
| No EINECS | (L) (D) |
| DrugBank | |
| PubChem | |
| FEMA | |
| SMILES | |
| InChI | |
| Apparence | poudre blanche |
| Propriétés chimiques | |
| Formule brute | C9H11NO2 |
| Masse molaire | 165,1891 ± 0,0088 g·mol-1 |
| pKa | 1,83 (fonction acide) 9,13 (fonction amine) |
| Propriétés physiques | |
| T° fusion | 275 à 283 °C |
| Propriétés biochimiques | |
| Codons | UUC, UUU |
| pH isoélectrique | 5,48 |
| Acide aminé essentiel | oui |
| Précautions | |
| | |
| Produit non contrôlé | |
| | |
La phénylalanine est un acide aminé aromatique non polaire dont sont issus, notamment, la tyrosine et l'aspartame. Son noyau benzénique lui confère un spectre d'absorption particulier dans l'U.V, autour de 260 nm de longueur d'onde. Elle se présente sous la forme de deux énantiomères du fait de la chiralité de l'atome de carbone portant les fonctions amine et acide. Elle est un acide aminé essentiel, c'est-à-dire qu'elle doit être apportée par l'alimentation, car l'organisme est incapable de la synthétiser.
L'action de la phénylalanine hydroxylase la transforme en un autre acide aminé : la tyrosine, qui n'est de ce fait pas un acide aminé essentiel.
Chimie industrielle
La phénylalanine est, avec l'aspartate, l'un des deux constituants de l'aspartame, un dipeptide utilisé comme édulcorant dans les boissons et les aliments dits « légers » (notamment les sodas light) pour son pouvoir sucrant 200 fois supérieur à celui du saccharose et sa faible valeur énergétique.
Phénylpropanoïdes
La phénylalanine joue un rôle majeur dans le monde végétal : il s'agit de la molécule dont dérivent tous les phénylpropanoïdes, qui comprennent entre autres les coumarines, les flavonoïdes, les stilbénoïdes, ainsi que les monolignols, les monomères de la lignine et de la lignane qui constituent les parois des cellules végétales.
La phénylalanine est d'abord transformée en acide cinnamique par l'action de l'enzyme phénylalanine ammonia-lyase (PAL). Ce dernier est ensuite converti par des séries d'hydroxylation, méthylation et réductions enzymatiques en différents précurseurs de chacune des classes de phénylpropanoïdes.
Biochimie
La phénylcétonurie est une maladie génétique caractérisée par des troubles comportementaux. Elle est due à la progression d'une version non efficiente de l'enzyme dégradant la phénylalanine, la phénylalanine hydroxylase, entraînant une concentration sanguine trop élevée chez l'individu malade.
Médicale
La phénylalanine est présente notamment dans les gommes à mâcher, si cette molécule n'a pas d'effets dans les proportions d'une gomme voir deux ou plus par jour, elle aura par contre un effet laxatif à plus forte quantité (soit 2 voire 3 paquets de gommes à mâcher par jours), en effet l'action de la phénylalanine sur le corps à forte dose devient un accélérant du transit intestinal.