Vancomycine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Vancomycine | |
|---|---|
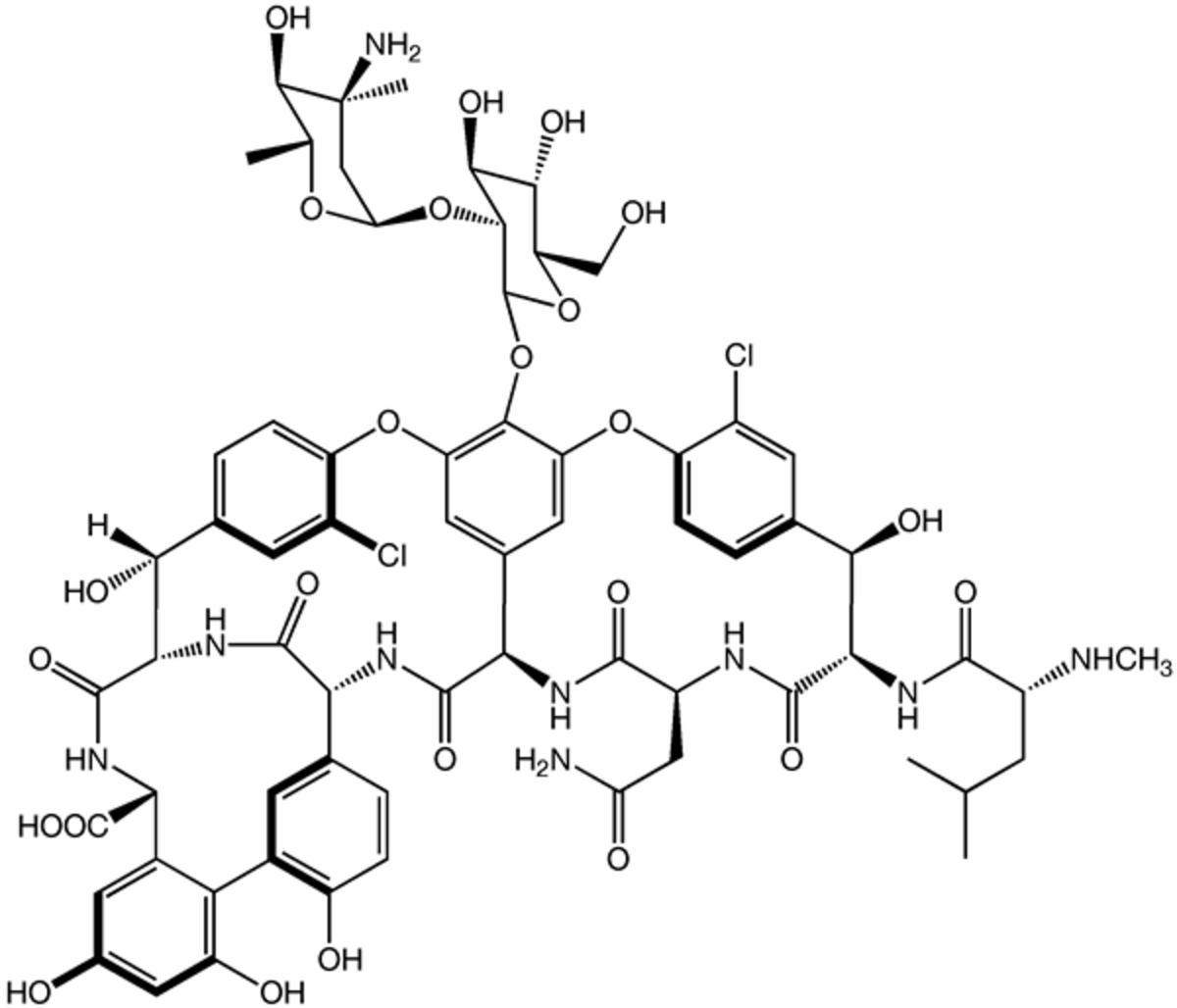
| |
| Général | |
| No CAS | |
| No EINECS | |
| Code ATC | A07, J01 |
| DrugBank | |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | Solide |
| Propriétés chimiques | |
| Formule brute | C66H75Cl2N9O24 |
| Masse molaire | 1 449,254 ± 0,071 g·mol-1 |
| Écotoxicologie | |
| DL | 430 mg·kg-1 souris i.v. 5 000 mg·kg-1 souris s.c. 1 734 mg·kg-1 souris i.p. |
| Classe thérapeutique | |
| Antibiotique glycopeptide | |
| Données pharmacocinétiques | |
| Biodisponibilité | ~0 % per os |
| Métabolisme | Non métabolisée |
| Demi-vie d’élim. | 4 à 11 h (adultes) 6 à 10 h (insuff. rénaux) |
| Excrétion | Rénale |
| Considérations thérapeutiques | |
| Voie d’administration | Intraveineuse |
| Grossesse | Utilisable en cas de nécessité |
| | |
La vancomycine est un antibiotique de la famille des glycopeptides. Volumineuse (1 500 à 2 000 daltons) et complexe, elle est, au même titre que les β-lactamines, une inhibitrice de la synthèse du peptidoglycane de la paroi bactérienne. Mais, du fait de son poids élevé, elle ne peut emprunter les porines de la membrane externe des Gram négatifs. Son spectre d’action touche donc uniquement les Gram positifs.
La Vancomycine est bactéricide, mais cette bactéricidie est lente à apparaître ; sa biodisponibilité par voie orale est négligeable, la voie intraveineuse s’impose donc le plus souvent.
Les principaux effets secondaires sont une atteinte rénale et auditive, il est donc justifié d’entreprendre une surveillance régulière des taux plasmatiques de vancomycine.
Enfin, son coût n’est pas négligeable et elle est souvent un traitement de dernier recours.
Indications des glycopeptides
En curatif, elles se limitent aux situations suivantes:
- infections sévères aux germes résistants aux β-lactamines, ou lorsque le patient est allergique à ces dernières,
- colite pseudo-membraneuse à Clostridium difficile.
Deux situations prophylactiques sont éventuellement possible:
- Antibioprophylaxie de l’endocardite bactérienne chez des patients porteurs d’une cardiopathie à risque, allergiques aux β-lactamines et devant subir un geste à risque.
- Antibioprophylaxie des infections du site opératoire dans des chirurgies à risque staphylococcique (chirurgie cardiaque, vasculaire, orthopédique, neurochirurgie), dans des circonstances où le risque d’infection à staphylocoque résistant à la Méticilline est accru (reprise chirurgicale précoce surtout) ou chez des patients allergiques aux β-lactamines.
Pharmacodynamie
Comme pour les β-lactamines, la vancomycine est inhibitrice de la synthèse du peptidoglycane de la paroi bactérienne. Son mécanisme d’action est toutefois différent : elle se fixe au niveau des extrémités peptidyl-D-Ala-D-Ala des précurseurs lipopeptidiques lorsqu'ils émergent de la membrane cytoplasmique, durant leur transport à travers celle-ci, et inhibe ainsi les étapes de transglycosylation et de transpeptidation, nécessaire à la bonne synthèse du peptidoglycane, action subséquente de la transpeptidase (qui catalyse l'enlèvement du D-Ala terminal et la réticulation du peptidoglycane).
Plus prosaïquement, elle agit en se liant aux composants de la paroi des bactéries à Gram positifs et en provoquant la dégradation de celle-ci.