Éthinylestradiol - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Éthinylestradiol | |
|---|---|
| |
| Général | |
| Nom IUPAC | |
| No CAS | |
| No EINECS | |
| Code ATC | L02 |
| DrugBank | |
| PubChem | |
| ChEBI | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C20H24O2 |
| Masse molaire | 296,4034 ± 0,0183 g·mol-1 |
| Classe thérapeutique | |
| estrogène | |
| Données pharmacocinétiques | |
| Biodisponibilité | ~100 % |
| Liaison protéique | 97 % |
| Métabolisme | hépatique |
| Demi-vie d’élim. | 36 ± 13 heures |
| Excrétion | rénale |
| Considérations thérapeutiques | |
| Voie d’administration | orale, percutanée |
| | |
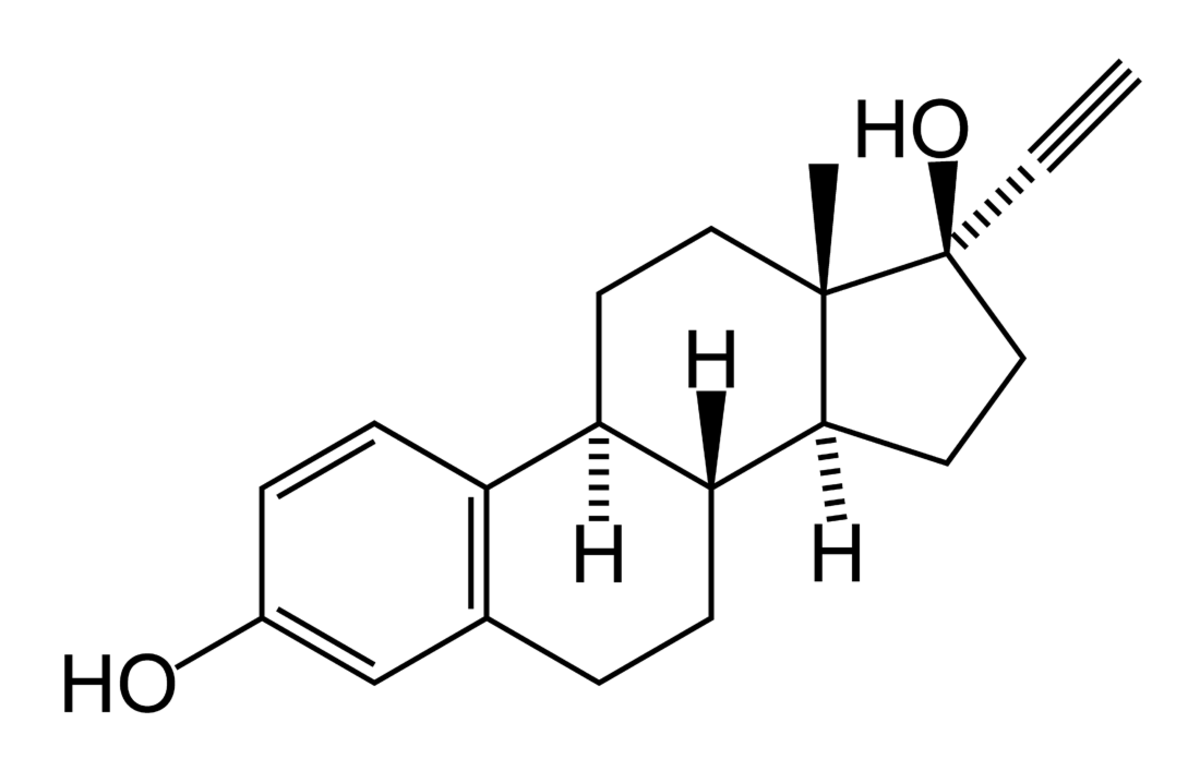
L'Éthinylestradiol, ou éthinyl estradiol (EE), est un dérivé de synthèse de l'estradiol. C'est l'œstrogène actif par voie orale le plus utilisé au monde. On le trouve dans presque toutes les formulations modernes des pilules contraceptives combinées.
Le premier stéroïde œstrogénique de synthèse actif par voie orale, l'éthinylestradiol, l'analogue 17α-éthynyl de l'estradiol, a été synthétisé chimiquement en 1938 par Hans Herloff Inhoffen et Walter Hohlweg dans les laboratoires Schering à Berlin.
L'éthinylestradiol fut autorisé par la FDA aux États-Unis le 25 juin 1943 et commercialisé par Schering-Plough sous le nom de Estinyl. La FDA a retiré son autorisation à l’Estinyl le 4 juin 2004 à la demande du laboratoire Schering qui avait arrêté de le commercialiser.
Bien que l'estradiol soit facilement absorbé quand il est pris par voie orale, il est également rapidement dégradé par le foie. La substitution de l'hydrogène sur le carbone 17 de la molécule d'estrane par un groupe éthinyl a montré que l'on obtenait ainsi un œstrogène bien plus résistant à la dégradation hépatique et a ouvert la voie au développement de contraceptifs oraux.
L'éthinylestradiol est absorbé dans l'intestin grêle et atteint un pic sérique environ 2h plus tard. Il subit une forte métabolisation dans le foie qui implique l'isoenzyme cytochrome P450.
L'éthinylestradiol et ses métabolites sont excrétés dans la bile. À cause de la circulation entérohépatique, un second pic est observé plusieurs heures après.
Il existe de grandes variations entre les individus dans le processus global d'absorption qui peut de plus être modifié par les drogues (par exemple, les antibiotiques qui affectent la circulation entérohépatique ou bien les enzymes du foie.).
Dans la circulation sanguine, EE est quasiment intégralement fixé à l'albumine du plasma sanguin.
Sa métabolisation se fait par hydroxylation du noyau aromatique et est excrété à la fois dans les fèces et dans les urines sous forme de glucuronide et de sulfate conjugués.
L'EE est actif au plan hormonal en activant les récepteurs des œstrogènes et, par là même, est donc un œstrogène. Il trouve son emploi le plus commun dans les associations estrogène-progestérone utilisées dans les préparations contraceptives. Au cours du temps, les quantités d'éthinylestradiol utilisées de façon quotidienne ont diminué de 100 μg à 20 μg.
Les mêmes contre-indications et précautions que pour les autres médicaments à base d'œstrogène s'appliquent à l'EE.
L’Estinyl était un médicament ayant comme seul principe actif l'EE utilisé pour calmer les symptômes de la ménopause et l'hypogonadisme féminin.
L'EE est excrété dans les urines et les fèces. C'est un estrogène de synthèse qui est donc relargué dans la nature sans que l'on en connaisse les conséquences.