Éfavirenz - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
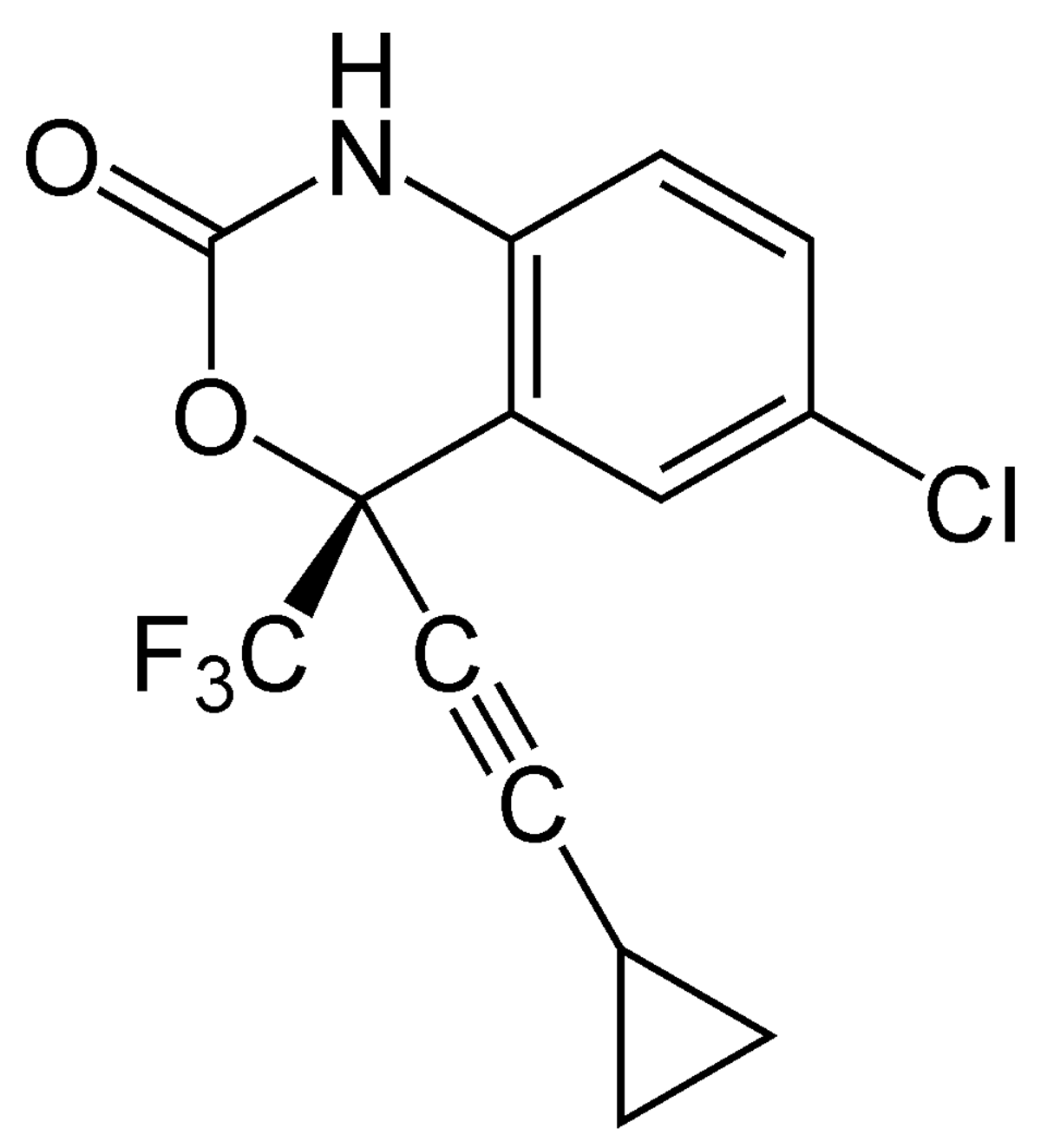
| Éfavirenz | |
|---|---|
| |
| Général | |
| Nom IUPAC | |
| Synonymes | EFV |
| No CAS | |
| Code ATC | J05 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C14H9ClF3NO2 |
| Masse molaire | 315,675 ± 0,015 g·mol-1 |
| pKa | 10,2 |
| Propriétés physiques | |
| T° fusion | 137,2 ± 1,4 °C. |
| Considérations thérapeutiques | |
| Voie d’administration | Orale, IV |
| Grossesse | classe D |
| Antidote | aucun |
| | |
L'éfavirenz (EFV) est un médicament antirétroviral, c'est un analogue non nucléosidique, inhibiteur de la transcriptase inverse (nNRTI) utilisé pour le traitement de l'infection par le VIH. Cette molécule est commercialisée sous le nom de Sustiva® ou Stocrin® et est disponible sous forme de comprimé ou de capsule.
Mécanisme d’action
L’éfavirenz agit comme un inhibiteur sélectif non nucléosidique de la transcriptase inverse du virus de l’immunodéficience humaine de type-1 (VIH-1). Il agit de façon non compétitive contre la transcriptase inverse du VIH-1. Ni la transcriptase inverse du VIH de type 2, ni les polymérases cellulaires alpha (α), bêta (β), gamma (γ) et delta (δ) ne sont affectées par les concentrations utilisées en clinique.
Symptômes
Voici un résumé non exhaustif des principaux problèmes liés à l’utilisation chez l’humain d’éfavirenz. L’éfavirenz a fait l’objet d’études chez 9 200 patients et en association avec 1 ou 2 autres médicaments (indivanir, zidovudine et lamivudine).
Système nerveux
53 % des patients qui ont utilisés, lors de l’étude, éfavirenz on déclaré avoir des symptômes. Les plus communs sont des céphalées, des étourdissements et de l’insomnie. Des symptômes plus graves, tels que l’amnésie et la dépersonnalisation ont apparu chez 2 % des patients.
Effet psychiatrique
Les symptômes les plus courants sont la dépression, l’anxiété et la nervosité à 19%, 16% et 7% respectivement. Des cas de dépression grave, d’idée suicidaire et de tentative de suicide étaient plus fréquents dans les groupes traités avec de l’éfavirenz.
L’éruption cutanée
Il s’agit d’une éruption maculopapuleuse légère à modérée. Habituellement l’éruption cutanée apparait après 1 à 2 semaines et disparait en moins d’un mois même si on continue le traitement. Il est conseillé d’arrêter le traitement à l’éfavirenz si l’éruption cutanée est importante, s’il y a formation de phlyctène, si des muqueuses sont touchées ou s’il y a de la fièvre. Les éruptions cutanées de grade 2 sont les plus communes lors de la prise d’éfavirenz.
Pharmacocinétique
Absorption
Lors de tests sur des patients séronégatifs, la concentration plasmatique maximale est atteinte dans les 5 heures suivant l’administration d’une dose unique par voie orale. Les tests ont été effectués avec des doses variant de 100 mg à 1 600 mg.
Effet des aliments sur l’absorption
La prise d’une capsule de 600 mg d’éfavirenz avec un repas riche en matières grasses et en calories et un repas pauvre en matières grasses et équilibré en calories, provoque une augmentation de 39 % et de 51 %, respectivement, de la concentration maximale d’éfavirenz dans le sang par rapport à un état à jeun et la prise d’une capsule de 600 mg d’éfavirenz.
La prise d’un comprimé de 600 mg d’éfavirenz avec un repas riche en matières grasses et en calories provoque une augmentation de 79 % de la concentration maximale d’éfavirenz dans le sang par rapport à un état à jeun et la prise d’un comprimé de 600 mg d’éfavirenz.
Métabolisme
L’éfavirenz est principalement métabolisé par le cytochrome P450 dans le foie. Il est métabolisé en métabolites hydroxylés, qui sont de nouveau métabolisés en glucuronides. Ces métabolites ne présentent aucune action contre le VIH-1. Selon des études in vitro, les isoenzymes CYP3A4 et CYP2B6 sont, en premier lieu, responsables de la métabolisation de l’éfavirenz. Si la concentration d’éfavirenz est de 82 à 160µM, il se peut qu’il inhibe les isoenzymes CYP2D6 et CYP1A2.
Un des avantages de l’éfavirenz est qu’il induit les enzymes du cytochrome P450 et donc son propre cycle de métabolisation. L’utilisation répétée de l’éfavirenz réduit son temps de demi-vie terminale d’environ 10 à 20 heures de moins comparer à une seule dose.
Élimination
L’éfavirenz possède une longue demi-vie terminale de 52 à 76 heures après l’administration d’une seule dose, mais de 40 à 55 heures après l’administration de doses multiples. Une étude d’une durée d’un mois pour vérifier la quantité résiduelle et la quantité éliminée (excrétée). Des sujets ont des doses de 400 mg d’éfavirenz par jour, la 8e dose a été marqué au 14C. une proportion d’éfavirenz radiomarqués a été trouvée dans l’urine et dans les fèces entre 14 à 34 % et 16 à 61 %, respectivement. Dans l’urine, il s’agit entièrement de métabolite et dans les fèces la majorité est de l’éfavirenz.
Données démographiques
La pharmacocinétique de l’éfavirenz ne semble être affectée ni par le sexe ni par l’origine de la personne.