Trifluorure de bore - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Trifluorure de bore | |||
|---|---|---|---|
| |||
| Général | |||
| Synonymes | Trifluoroborane | ||
| No CAS | |||
| No EINECS | |||
| Apparence | gaz comprime, incolore, d'odeur acre. Forme des fumées blanches en atmosphère humide. | ||
| Propriétés chimiques | |||
| Formule brute | BF3 | ||
| Masse molaire | 67,806 ± 0,007 g·mol-1 | ||
| Propriétés physiques | |||
| T° fusion | -127 °C | ||
| T° ébullition | -100 °C | ||
| Solubilité | 3 320 g·l-1 dans l'eau à 0 °C | ||
| Masse volumique | 2,4 (air=1) | ||
| T° d’auto-inflammation | ininflammable | ||
| Point critique | 49,9 bar, -12,35 °C | ||
| Thermochimie | |||
| ΔH° | 19,33 kJ·mol-1 (1 atm, -99,9 °C) | ||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 15,7 ± 0,3 eV (gaz) | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 14, 26, 35, | |||
| Phrases S : (1/2), 9, 26, 28, 36/37/39, 45, | |||
| | |||
|
0 4 1 | |||
| | |||


| |||
| | |||



Danger | |||
| Inhalation | Toux | ||
| Peau | Rougeur, douleur | ||
| Yeux | Rougeur, douleur | ||
| Écotoxicologie | |||
| Seuil de l’odorat | bas : 1,5 ppm | ||
| | |||
Le trifluorure de bore est un gaz toxique et incolore de formule chimique BF3. Il réagit avec l'air humide en formant des fumées blanches composés de fluorure d'hydrogène, d'acide borique et d'acide fluoroborique.
Dans ce composé, le bore est déficitaire en électrons. Au cours des réactions chimiques, BF3 se comporte donc comme un acide de Lewis. Il réagit par exemple avec les fluorures en formant des sels de tétrafluorure :
CsF + BF3 → CsBF4
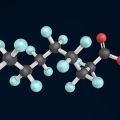
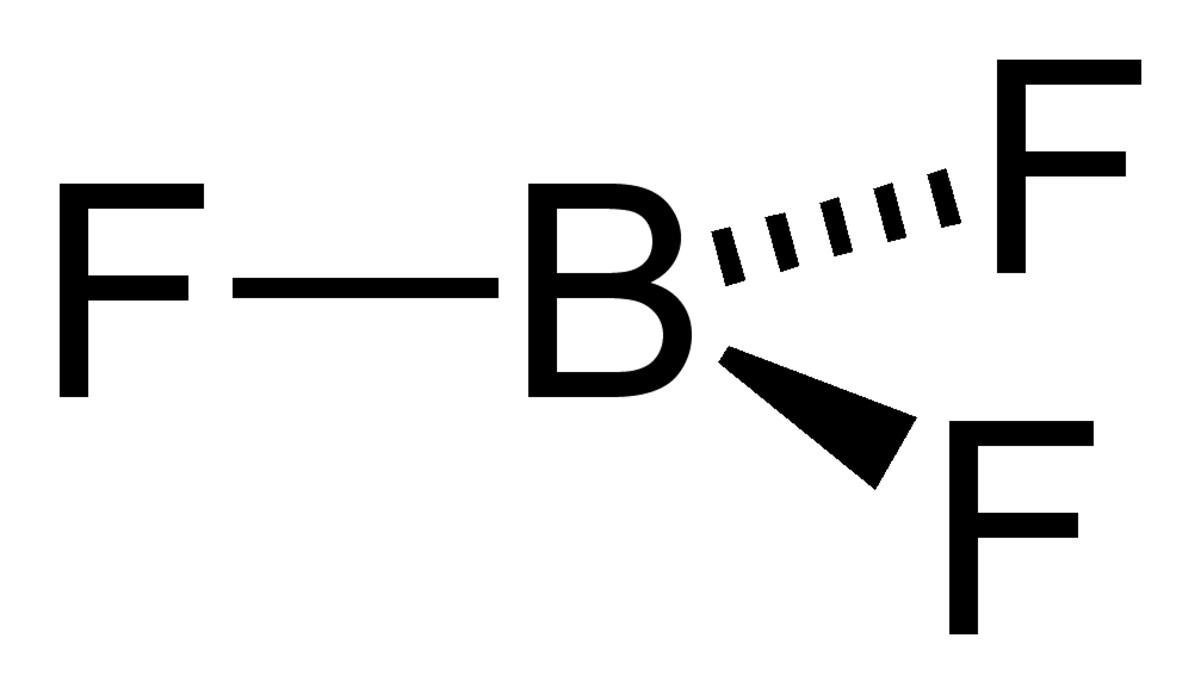
Structure
La configuration spatiale adoptée par cette molécule est celle qui minimise au maximum les paires de liaison électronique. Elle correspond à une structure dans laquelle les 4 atomes sont coplanaires avec des angles de valence égaux à 120 °. La molécule est plane, trigonale et forme un triangle équilatéral.
Sécurité
Le trifluorore de bore est un composé corrosif. Une inhalation prolongée peut occasionner un œdème pulmonaire. Il réagit violemment avec l'eau. Il doit être manipulé avec précautions.
La valeur limite d'exposition est fixée en France à 1 ppm (2,77 mg·m-3).
Utilisation
- Il est principalement utilisé comme dopant pour l'implantation d'ions dans les semi-conducteurs
- Il permet aussi d'initier des réactions de polymérisation de composés insaturés.
- Le 10BF3 est utilisé dans les détecteurs de neutrons lents (par exemple dans les sondes à neutrons).