Benzène - Définition
La liste des auteurs de cet article est disponible ici.
Délocalisation-mésomérie
On explique la planéité du benzène par le fait que dans cette conformation, les orbitales 2p (x ou y) pures (c’est-à-dire non hybridées) des atomes de carbone optimisent leur recouvrement latéral. Il n'y a donc pas réellement de double liaison entre deux carbones donnés, mais ce qui est appelé un système pi résonnant (ou délocalisé) que l'on peut décrire comme un vaste nuage électronique réparti équitablement entre tous les atomes de carbone.
Les électrons pi sont donc répartis sur tous les atomes de carbone, et la molécule peut être représentée comme la superposition des deux formes suivantes, appelées formes mésomères :
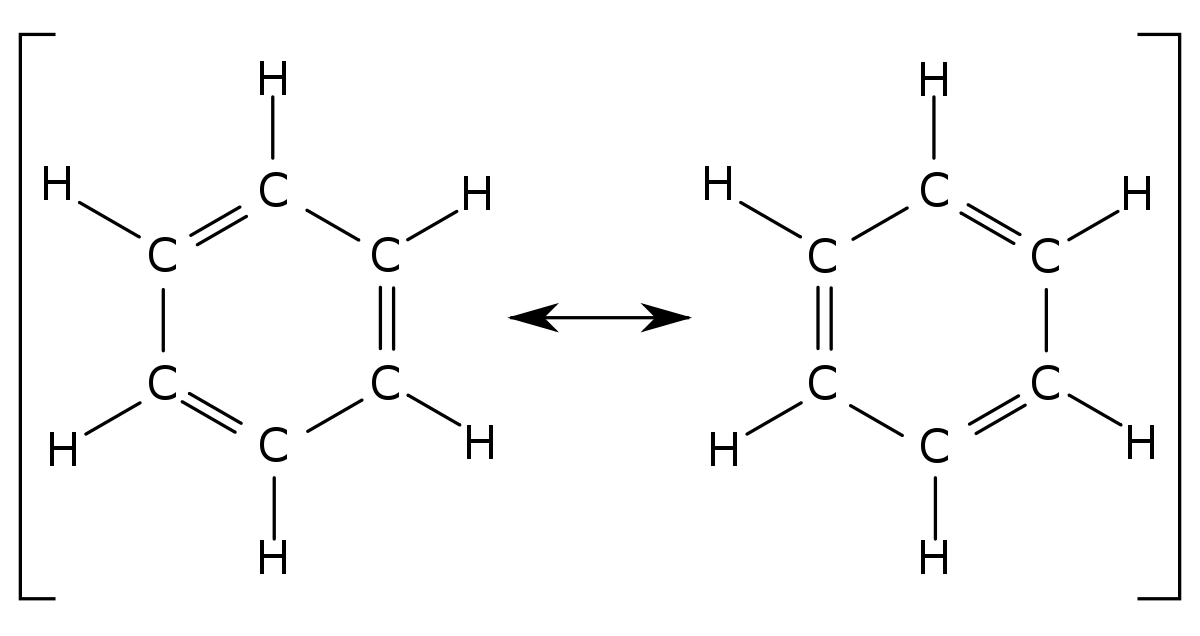
En réalité, aucune des deux formes représentées ci-dessus n'existe. La délocalisation doit être représentée d'une manière différente que par la simple utilisation de liaisons simples et de liaisons doubles. Dans une molécule organique, les liaisons simples sont des liaisons σ, formées d'électrons dont la probabilité de présence est très importante entre les atomes (recouvrement axial). Les liaisons doubles sont formées à la fois d'une liaison σ et d'une liaison π, celles-ci étant construites à partir des électrons 2p (x ou y) du carbone, comme illustré sur le schéma suivant (dans la partie de gauche, les liaisons σ sont représentées en rouge, les orbitales 2p en blanc et gris) :
Les orbitales 2p (x ou y) étant en dehors du plan constitué par les atomes, elles peuvent interagir librement, ce qui conduit à la délocalisation des électrons : chaque électron n'est pas rattaché spécifiquement à un atome ou une liaison, mais est délocalisé sur tout l'anneau, renforçant chacune des liaisons de manière équivalente :
Pour représenter ce caractère délocalisé des liaisons, le benzène est généralement représenté par un cercle contenu dans un hexagone :
Une méthode plus puissante permet de mieux décrire la structure électronique du benzène : la méthode des orbitales moléculaires. Cette méthode a été mise en œuvre par Erich Hückel en 1931 et nécessite le calcul d’un déterminant à six lignes et six colonnes et permet d'obtenir le diagramme énergétique du benzène.
Production
Le benzène est produit lorsque des composés riches en carbone subissent une combustion incomplète. Par exemple, il est produit naturellement dans les volcans ou les incendies de forêts. Il est également présent dans la fumée de cigarette.
Jusqu'à la Seconde Guerre mondiale, le benzène était en majeure partie un produit secondaire de la production de coke dans l'industrie de l'acier. Cependant au cours des années 1950, la demande croissante de benzène, notamment dans l'industrie du plastique, a entraîné la nécessité de produire du benzène à partir de pétrole. À l'heure actuelle, la majeure partie du benzène est produite par l'industrie pétrochimique, avec une part mineure issue du charbon.
La production industrielle de benzène est issue de manière à peu près égale de trois procédés chimiques : le reformage catalytique, l'hydrodésalkylation du toluène et le vapocraquage. En 1996, la production mondiale de benzène était de 33 millions de tonnes dont 7 millions aux États-Unis, 6,5 millions dans l'Union européenne, 4,2 millions au Japon, 1,4 million en Corée du Sud et 1 million en Chine.
Reformage catalytique
Au cours du reformage catalytique, un mélange d'hydrocarbures de températures d'ébullition comprises entre 60 °C et 200 °C est mélangé à du dihydrogène, puis passé sur des catalyseurs (chlorure de platine ou chlorure de rhénium) à une température comprise entre 500 °C et 525 °C et une pression comprise entre 8 et 50 atm. Dans ces conditions, les hydrocarbures aliphatiques forment des cycles et perdent des atomes d'hydrogène pour devenir aromatiques. Les composés aromatiques produits au cours de la réaction sont alors séparés du mélange réactionnel par extraction en utilisant des solvants comme le sulfolane ou le diéthylène glycol. Le benzène est ensuite séparé des autres composés aromatiques par distillation.
Hydrodésalkylation du toluène
L'hydrodésalkylation du toluène permet de convertir le toluène en benzène. Dans ce procédé chimique, le toluène est mélangé à du dihydrogène, puis passé sur un catalyseur (oxyde de chrome, de molybdène ou de platine) à une température comprise entre 500 °C et 600 °C et une pression comprise entre 40 et 60 atm. Il est également possible de se passer de catalyseur en utilisant des températures plus élevées. Dans ces conditions, le toluène subit une désalkylation (perte du groupement alkyle, ici un groupement méthyle) :
- C6H5CH3 + H2 → C6H6 + CH4
Le rendement de cette réaction est supérieur à 95 %. Parfois, des composés aromatiques plus lourds comme le xylène sont utilisés à la place du toluène avec des rendements similaires.
Vapocraquage
Le vapocraquage est un procédé utilisé pour produire de l'éthylène et d'autres alcènes à partir d'hydrocarbures aliphatiques. Suivant le composé de départ utilisé dans le procédé, le vapocraquage peut également produire un produit secondaire liquide riche en benzène. Ce liquide peut être mélangé à d'autres hydrocarbures en tant qu'additif pour l'essence, ou distillé pour le séparer en différents composés dont le benzène.