Cyanoacrylate - Définition
La liste des auteurs de cet article est disponible ici.
Propriétés
Dans sa forme liquide, le cyanoacrylate consiste en des monomères de molécules de cyanoacrylates, CH2=C(CN)COOCH3 (Formule brute : C5H5NO2), et a une masse moléculaire de 111,1 g/mol. Son point d'éclair se situe à 79°C et sa densité est 1,1 par rapport à l'eau (H2O).
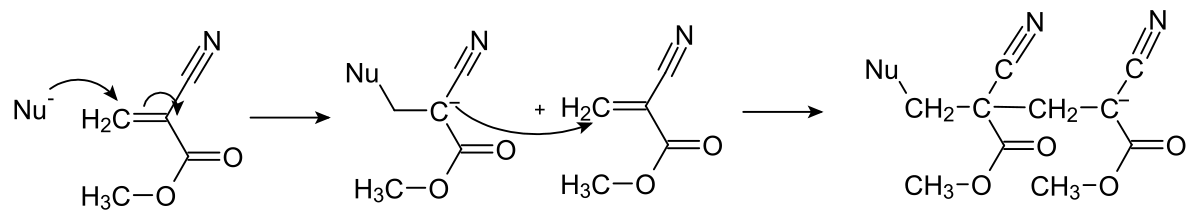
C'est une résine acrylique qui polymérise rapidement en présence d'anions (la polymérisation démarre avec un amorceur anionique, tel que l'hydroxyde, les amines, les alcools, ...). Dans ce cas précis de polymérisation anionique, l'eau suffit à amorcer la polymérisation, l'intermédiaire réactionnel étant stabilisé par la présence du groupement carbonyle et du groupement cyano en alpha du carbanion. Lors de la polymérisation, il y a formation de longues et solides chaînes, joignant les surfaces à coller.
Un autre trait important est que le cyanoacrylate colle rapidement, souvent en moins d'une minute, face à un collage normal qui obtient sa solidité maximale en deux heures ; et est résistant à l'eau. Des accélérants permettent d'obtenir le collage en 2 ou 3 secondes, au prix d'une perte de solidité. Deux centimètres carrés de surface de collage supportent aisément le poids d'une masse supérieure à une tonne.
L'acétone (que l'on retrouve dans le dissolvant pour vernis à ongles), est un solvant facilement disponible, capable de ramollir le cyanoacrylate polymérisé.
Sécurité
Attention à la manipulation de ce produit: une goutte serrée entre ses doigts les collerait l'un sur l'autre et une intervention chirurgicale risquerait d'être nécessaire.
Il est possible de les décoller sous eau du robinet, à la chaleur maximale.(attention aux brûlures) On peut aussi utiliser du dissolvant à ongles pour séparer les parties collées. Ne pas utiliser sur les muqueuses.
Application pour le bricolage
- Appliquer une couche d'activateur sur une face de la cassure
- Laisser sécher environ une minute
- Appliquer ensuite une couche de résine sur l'autre face
- Mettre en contact les deux parties, attention la prise de colle est immédiate
- Presser fortement pendant une minute
- Enlever les bavures immédiatement avec un chiffon imbibé d'alcool à 90°
- Laisser sécher une demi-heure sans y toucher
Synonyme
- alpha-cyanoacrylate de méthyle
- MCA
- Mécrylate
- Mécrilate
- Ergo Kisling
Voir aussi
Conservation
Après usage, conserver le produit dans un endroit frais et sec et à l'abri de la lumière (raison pour laquelle, ils sont déconseillés pour recoller le verre).

















































