Oxysulfure de carbone - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Oxysulfure de carbone | |||
|---|---|---|---|
| |||
| Général | |||
| Nom IUPAC | |||
| Synonymes | carbone oxysulfure sulfure de carbonyle | ||
| No CAS | |||
| No EINECS | |||
| PubChem | |||
| ChEBI | |||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule brute | COS | ||
| Masse molaire | 60,075 ± 0,006 g·mol-1 | ||
| Moment dipolaire | 0,715189 D | ||
| Propriétés physiques | |||
| T° fusion | -138,81 °C | ||
| T° ébullition | -50,2 °C | ||
| Solubilité | 1,49 g·l-1 (eau,20 °C)) | ||
| Masse volumique | 1,178 g·cm-3 à -50,2 °C | ||
| T° d’auto-inflammation | 250 °C | ||
| Limites d’explosivité dans l’air | 6,5–29 %vol | ||
| Pression de vapeur saturante | 11,28 bar à 20 °C | ||
| Point critique | 63,5 bar, 105,65 °C | ||
| Thermochimie | |||
| S0 | 231,57 J·K-1·mol-1 | ||
| S0 | 136,31 J·K-1·mol-1 | ||
| ΔH0 | -138,41 kJ·mol-1 | ||
| ΔH° | 4,728 kJ·mol-1 à -138,82 °C | ||
| ΔH° | 18,506 kJ·mol-1 { -50,24 °C | ||
| Cp | 41,48 J·K-1·mol-1 (gaz,24,85 °C) 71,25 J·K-1·mol-1 (liquide,-53,15 °C) | ||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 11,18 ± 0,01 eV (gaz) | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 12, 23, | |||
| Phrases S : 9, 16, 33, 36, 45, | |||
| | |||
| |||
| Écotoxicologie | |||
| DL | 23 mg·kg-1 (rat, i.p.) | ||
| | |||
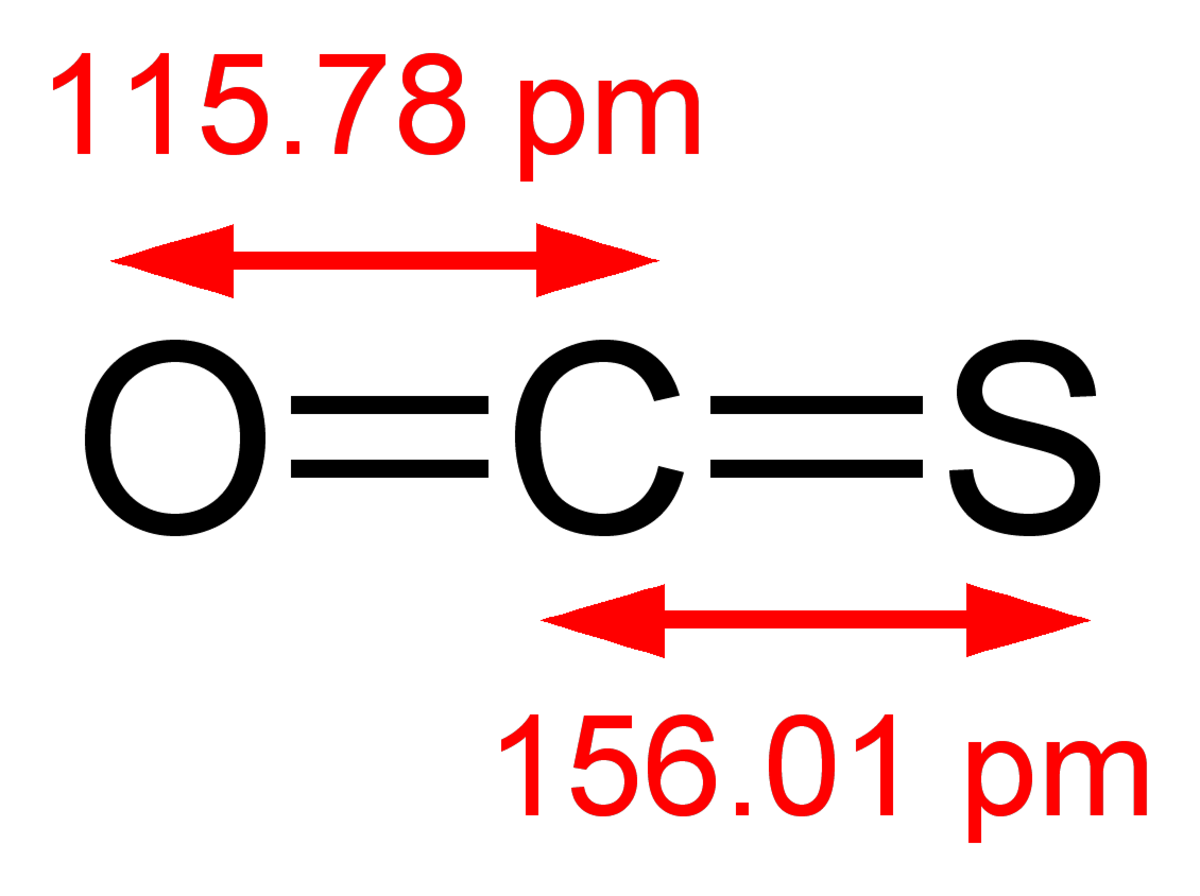
L'oxysulfure de carbone (ou sulfure de carbonyle), de formule chimique COS, est un gaz incolore, toxique et inflammable, principalement émis dans l'environnement par l'activité volcanique.
Il fait partie des ligands soufrés volatils (composés chimiques appartenant au cycle du soufre et interagissant chimiquement avec certains métaux).
C'est un puissant gaz à effet de serre dont le rôle présent et passé dans les cycles biogéochimiques est encore mal compris.
Dans notre atmosphère riche en dioxygène ce gaz est rapidement dégradé (photolyse + probables phénomènes catalytiques). Il perd alors ses capacités de gaz réchauffant puisqu'au contraire, les composés issus de cette dégradation forment des aérosols soufrés qui renvoient vers l'espace une partie du rayonnement infrarouge solaire (mais en contribuant secondairement à l'acidification des mers... laquelle, au delà d'un certain seuil pourrait rétroactivement diminuer la capacité des océans à stocker le CO2 sous forme de CaCO3, c'est-à-dire faire de l'océan une source de dioxyde de carbone, voire de méthane qui accélèrerait le réchauffement).



















































