Réaction organique - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
Les réactions organiques sont des réactions chimiques impliquant des composés organiques. Les principaux types de réactions organiques sont l'élimination, l'addition, la substitution, le réarrangement et les réactions d'oxydoréduction impliquant des composés organiques. Ces réactions sont utilisées en synthèse organique pour construire de nouvelles molécules organiques. La production de nombreuses substances chimiques, comme les médicaments, les plastiques, les additifs alimentaires, etc., met en jeu des réactions organiques.
Les plus anciennes réactions organiques réalisées par l'homme seraient la combustion de combustible et la saponification de corps gras pour obtenir du savon. La chimie organique moderne commence avec la synthèse de Wöhler en 1828. L'histoire des remises de prix Nobel en chimie est jalonnée de découvertes de réactions organiques particulières, comme la réaction de Grignard en 1912, celle de Diels-Alder en 1950, celle de Wittig en 1979 ou la métathèse des alcènes en 2005.
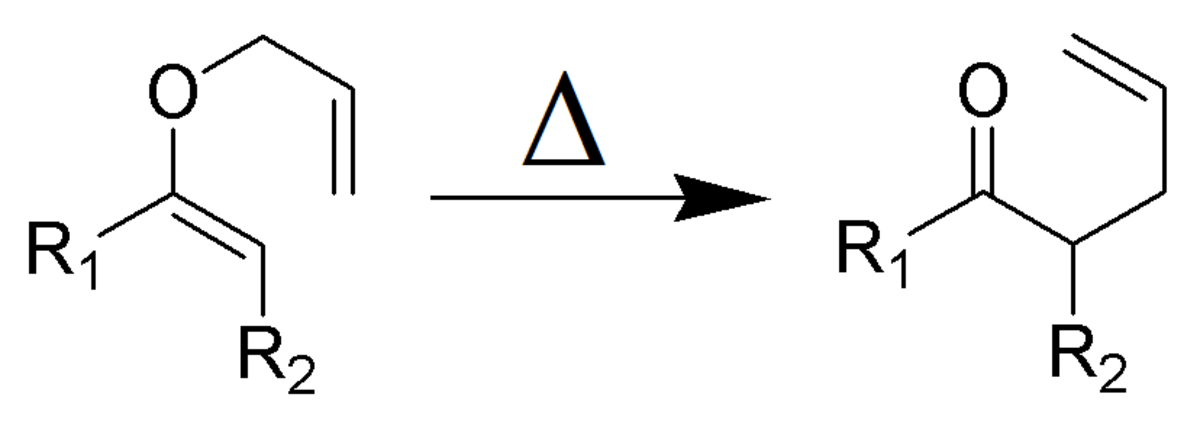
le réarrangement de Claisen
Appellation et classification
Les réactions organiques portent souvent le nom de leur inventeur. Ainsi, parmi tant d'autres, du réarrangement de Claisen (1912), ou de la réaction de Bingel (1993). Lorsque le nom est difficile à prononcer ou trop long, il est parfois abrégé : la réaction de Corey-House-Posner-Whitesides est plus connue sous le nom de réduction CBS. Actuellement la manière de nommer change. C'est le cas, par exemple, de l'aldolisation.
On peut classer ces réactions par mécanisme, par groupe fonctionnel (voir ci dessous) ou bien encore selon le type de réactif (souvent inorganique) nécessaire pour attaquer une substance organique : un oxydant comme le tétroxyde d'osmium, un réducteur comme le tétrahydruroaluminate de lithium, une base comme le diisopropylamidure de lithium, ou bien encore un acide comme l'acide sulfurique.
Réactions organiques par mécanisme
Le nombre de réactions organiques et de mécanismes est illimité. Cependant l'observation permet de classer la plupart des réactions courantes et utiles selon certains modèles généraux, et bien que les étapes de la transformation ne soient pas toujours connues avec précision, chaque réaction peut être décrite selon un mécanisme réactionnel qui explique comment elle se déroule. Parmi les réactions organiques, qui peuvent donc être classées dans différents types de base, certaines doivent entrer dans plus d'une catégorie. Des substitutions, par exemple, sont constituées d'une addition suivie d'une élimination. Le tableau suivant permet cependant de classer les réactions basiques :
| type de réaction | sous type | Commentaire |
|---|---|---|
| Réactions d'addition | addition électrophile | inclut des réactions comme l'halogénation, l'hydrohalogénation et l'hydratation. |
| addition nucléophile | ||
| addition radicalaire | ||
| réactions d'élimination | inclut la déshydratation, suivent un mécanisme E1, E2 ou E1cB | |
| Réactions de substitution | substitution nucléophile aliphatique | mécanismes SN1, SN2 et SNi |
| substitution nucléophile aromatique | ||
| substitution nucléophile acylique | ||
| substitution électrophile | ||
| substitution électrophile aromatique | ||
| substitution radicalaire | ||
| réactions organiques rédox | réactions rédox spécifiques aux composés organiques et très courantes | |
| Réactions de réarrangement | réarrangements 1,2 | |
| réactions péricycliques | ||
| métathèse |
Dans les réactions de condensation, une petite molécule, celle de l'eau par exemple, se forme quand deux réactifs se combinent par réaction chimique. La réaction opposée, où l'eau est consommée, est appelée hydrolyse.
De nombreuses réactions de polymérisation dérivent de réactions organiques, des polyadditions ou des polycondensations.
Le mécanisme d'une réaction peut souvent être figuré à l'aide de flèches qui représentent les mouvements d'électrons (célibataires, d'une liaison, d'un doublet non liant, etc.) pendant le passage des réactifs aux produits.

















































