Chaleur sensible - Définition
On appelle chaleur sensible la quantité de chaleur qui est échangée, sans transition de phase physique, entre deux corps formant un système isolé.
Le qualificatif sensible se justifie par le fait que l'échange de chaleur, sans changement de phase physique, correspond à une variation de la température du corps, laquelle peut être ressentie ou mesurée pour un observateur. En cela, la chaleur sensible s'oppose à la chaleur latente, qui, elle, ne se traduit pas par un changement de température, mais par un changement de phase (par exemple, dans des conditions normales, la température de fusion de la glace (eau pure)est 0°C).
Relation calorimétrique
Mathématiquement, la quantité de chaleur sensible Q échangée par un corps qui passe d'une température T1 à une température T2 est donnée par la relation :
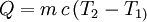
où m est la masse du corps (en kg) et c est la chaleur massique de ce corps (en J.kg–1.K–1).
c est aussi appelée capacité thermique massique ou encore chaleur spécifique qui correspond à l'apport de chaleur nécessaire pour élever la température de l'unité de masse de la substance de 1 Kelvin (1 K) lors de la transformation considérée. Cette grandeur c est caractéristique d'une substance donnée.
Pour les échanges de chaleur en continu, le système fonctionne en régime stationnaire par rapport au temps, mais en régime transitoire par rapport à l'espace. Donc, pour le dimensionnement des échangeurs de chaleur, on utilise habituellement la moyenne logarithmique des différences de températures (LMTD) telle que:
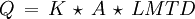
ou K est le coefficient global d'échange de chaleur (en W m–2K–1), A l'aire (en m2) et LMTD est la moyenne logarithmique des différences de température soit
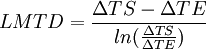
avec: ?TE: la différence de température d'entrée des fluides et ?TS: la différence de température de sortie des fluides
Capacité thermique des solides
En première approximation, la capacité thermique des solides est décrite par la loi de Dulong et Petit
Capacité thermique des liquides
En première approximation, la capacité thermique des liquides est constante. Pour l'eau : c = 1 cal g–1 K–1 (= 4,18 J kg–1 K–1). de façon générale : 0,5 cal g–1 K–1 < c < 1,0 cal g–1 K–1
Notions liées
- Calorie

















































