Cétone - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
Une cétone est un composé organique, faisant partie de la famille des composés carbonylés, dont l'un des carbones porte un groupement carbonyle. Les aldéhydes ont un carbone primaire et les cétones un carbone secondaire (lié à exactement 2 atomes de carbones voisins) qui porte le groupement carbonyle. Une cétone contient donc la séquence :
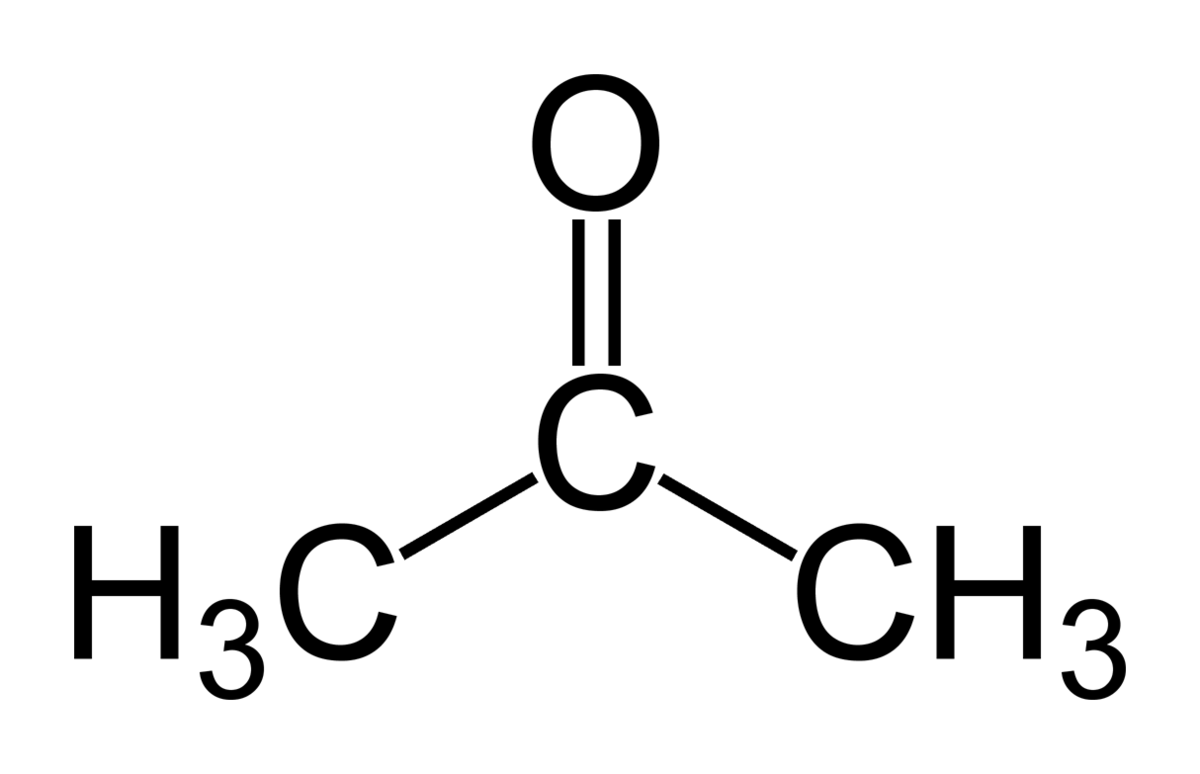
On peut par exemple citer l'acétone (propan-2-one) CH3-CO-CH3.
Nomenclature
- Groupe principal :
Le nom de la cétone s'obtient en ajoutant le suffixe -one au nom de l'hydrocarbure correspondante, en précisant la place de la liaison carbonyle dans la chaîne carbonée
- Groupe secondaire :
On rajoute le préfixe oxo-, en précisant sa place dans la chaîne carbonée
Propriétés, réactivité
Elles sont générales aux aldéhydes et aux cétones, en particulier concernant leur équilibre céto/énol. Voir l'article général composé carbonylé.
Principales cétones
- Propanone (acétone)
- Butanone
Utilisation des cétones
Les cétones sont utilisés dans la fabrication de matières plastiques, comme solvants, mais aussi comme colorants en parfumerie et pour les médicaments comme les aldéhydes.
Acétalisation
L'acétalisation est une réaction réversible permettant de transformer un composé carbonylé et deux alcools (ou un diol) en acétal. Cette réaction permet en fait de protéger le groupe carbonyle, ou l'alcool.
Réaction
Conditions
Caractéristiques et remarques
- Quand on utilise un aldéhyde, on nomme le produit obtenu « acétal ». Quand on utilise une cétone, on nomme le produit obtenu « cétal ». Cependant, de plus en plus on utilise le terme acétal comme terme générique pour désigner les 2 produits. On appelle par contre toujours la réaction (aussi bien pour les aldéhydes et pour les cétones) « acétalisation ».
- Cette réaction est en général en défaveur du cétal (contrairement aux acétals). Si on veut la favoriser dans le sens de la formation de celui-ci, on utilise un excès d'alcool (qui sert par la même occasion de solvant). Il faut aussi distiller l'eau (distillation hétéroazéotropique) à l'aide de l'appareil de Dean et Stark. Pour favoriser la réaction inverse, c'est le contraire : on met un excès d'eau pour hydrolyser le cétal.
- Quand on veut protéger la fonction carbonyle, on utilise le plus souvent un diol, comme l'éthane-1,2-diol:
- Cette réaction peut aussi très bien servir à protéger une fonction alcool, en particulier les diols vicinaux.
- Dans certains cas, la réaction peut s'arrêter à l'hémiacétal (cas des hémiacétals cycliques).
Action d'un organomagnésien
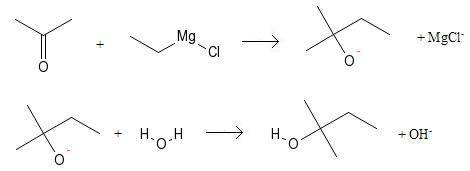
Un organomagnésien mixte réagit sur une cétone pour former un alcoolate tertiaire. Le carbone porteur de l'organomagnésien est ajouté sur le carbone porteur du groupement carbonyle. En milieu aqueux, l'alcoolate, base forte, gagne un proton pour former un alcool.
Réaction de Wittig
La réaction de Wittig transforme une cétone en dérivé éthylènique. Il transforme en fait la liaison C=O en liaison C=C.
Réaction de Shapiro
Réduction des cétones
En alcools
Industriellement
On utilise le dihydrogène H2 dans un solvant inerte, en présence d'un catalyseur (catalyse hétérogène). Il s'agit bien souvent de métaux, comme le platine (Pt), le palladium (Pd), le nickel (Ni) ou le rhodium (Rh). Si jamais la cétone possède aussi une liaison C=C, celle-ci aussi est hydrogénée (la réaction est plus facile sur C=C que sur C=O). Pour éviter cela, il faut effectuer une addition nucléophile d'hydrures. La réaction est exothermique.

Par les hydrures
Voir addition nucléophiles d'hydrures (plus bas).
En alcane
- Réduction de Clemmensen
- Réduction de Wolff-Kishner
Additions nucléophiles
d'hydrures (LiAlH4, NaBH4)
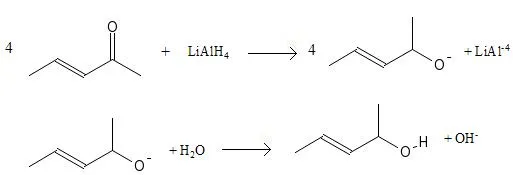
L'addition d'hydrures permet la réduction de l'oxygène du groupement carbonyle sans toutefois altérer une double liaison (la partie alcène) d'une molécule, comparativement à la simple addition d'hydrogène.
Une cétone portant également un alcène, lorsque traitée à un hydrure, produit un alcoolate qui porte un alcène. Cet alcoolate, traité avec un acide faible (comme l'eau) est alors transformé en alcool qui porte un alcène.
d'organométalliques
organomagnésiens mixtes, ou organolithiens.
Cétolisation (condensation de 2 cétones)
Oxydation de Baeyer-Villiger
transformation en Ester
- Hydrazone
On peut également obtenir un dérivé carbonylé (cétone ou aldéhyde) par hydrolyse d'une fonction imine, de formule générale RR'C=N, en catalyse acide ou basique. Cette hydrolyse permet par exemple d'obtenir une cétone comme produit final de l'addition d'un réactif de Grignard (organomagnésien mixte) sur un nitrile.