Éthanol - Définition
La liste des auteurs de cet article est disponible ici.
Propriétés médicales
L'éthanol absolu est parfois injecté dans des tumeurs afin de provoquer leur nécrose. Il n'a toutefois pas une activité ciblée puisqu'il provoque indifféremment la nécrose des tissus sains et cancéreux.
L'éthanol est aussi utilisé comme antidote dans le cas d'intoxication au méthanol, afin de saturer l'ADH (alcool déshydrogenase)
Azéotropie
L'eau en faible proportion forme un azéotrope avec l'éthanol et au-delà de 96% de pureté en EtOH, il devient très difficile de les séparer. Les proportions du mélange varient en fonction de la température et de la pression.
| pression | température | fraction molaire d'éthanol |
|---|---|---|
| 0,1 MPa | 78,35 °C | 0,894 |
| 0,344 MPa | 112,6 °C | 0,882 |
| 0,689 MPa | 135,7 °C | 0,874 |
| 1,378 MPa | 164,2 °C | 0,862 |
| 2,068 MPa | 182,6 °C | 0,852 |
Production industrielle d'éthanol
Par hydratation catalytique directe de l'éthylène
La synthèse de l'éthanol par hydratation de l'éthylène repose sur la réaction suivante :
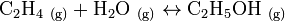
La variation d'enthalpie liée à cette réaction est ΔH = − 43,4 kJ·mol−1. Pour obtenir un rendement à l'équilibre satisfaisant (usuellement compris entre 7 % et 22 %), cette réaction nécessite d'être catalysée. La majorité des catalyseurs décrits dans la littérature technique présentent un caractère acide. On citera notamment l'acide phosphorique et l'acide silicotungstique. Ces catalyseurs imprègnent généralement un support poreux.
Le produit final de l'hydratation de l'éthylène est un mélange contenant entre 10 % et 25 % d'éthanol en poids. Des distillations successives seront donc nécessaires pour obtenir un mélange plus concentré. Au final, les conditions optimales pour la réalisation de cette réaction d'hydratation dépendent grandement du catalyseur utilisé, des caractéristiques du réacteur et des qualités du produit de départ.
Par hydratation indirecte de l'éthylène
La production d'éthanol par hydratation indirecte de l'éthylène fait intervenir un mécanisme réactionnel plus complexe avec deux grandes étapes : un ensemble de réactions d'estérification puis d'hydrolyse. Ce procédé consomme de grandes quantités d'acide sulfurique et nécessite en entrée un mélange gazeux de bonne qualité.
Production d'éthanol à partir de la biomasse
Dans ce cas, on parle de bioéthanol. La majorité du bioéthanol produit aujourd'hui provient du traitement des plantes sucrières (betterave, canne à sucre, …) ou des céréales (maïs, blé, …). La production de bioéthanol à partir de la biomasse se divise sommairement en trois étapes.
- L'hydrolyse de la céréale : contrairement aux plantes sucrières qui donnent du sucre directement, il est nécessaire d'hydrolyser l'amidon (polymère du glucose) contenu dans les céréales afin d'obtenir du glucose. Cette hydrolyse peut se faire par des enzymes (hydrolyse enzymatique) ou par de l'acide (hydrolyse acide, nécessite que le mélange soit porté à ébullition).
- La fermentation du glucose : on utilise pour cette étape des levures que l'on insère dans un mélange de sucre et d'eau. La durée de fermentation varie mais tourne aux alentours de quelques semaines. A l'issue de cette étape on obtient un éthanol très dilué, inutilisable pour l'instant.
- La distillation : pour extraire l'éthanol du mélange d'éthanol et d'eau on peut procéder à une distillation fractionnée. Cette distillation s'appuie sur la température d'ébullition de l'éthanol, inférieure à celle de l'eau. Le mélange appelé parfois alcoolat est porté à ébullition, et l'éthanol s'évapore avant que l'eau ne commence à bouillir. En pratique, une certaine proportion d'eau et de produits plus volatiles que l'éthanol entrent dans le liquide obtenu après la première distillation qu'on appelle parfois flegme, la flegmasse étant le résidu de cette distillation. D'autre part, de multiples distillations ne permettent pas d'obtenir un éthanol à plus de 96% car il forme avec l'eau un azéotrope (96%, PE:78,17 °C). Pour obtenir de l'éthanol plus pur, il faut déshydrater l'azéotrope, par exemple en le distillant sur CaO. Si le point azéotropique est dépassé, les distillations sont de nouveau opérationnelles.
D'autres filières existent cependant, notamment la production de bioéthanol (dit bioéthanol cellulosique) à partir de déchets végétaux (sciure de bois, paille de blé, emballages, …). En effet ces produits contiennent de grandes quantités de cellulose, un autre polymère du glucose. Le problème réside dans l'hydrolyse de la cellulose, difficilement réalisée à ce jour. Le procédé le plus élaboré dans ce domaine est actuellement celui développé par l'entreprise canadienne Iogen Corporation.