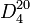Éthanol - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Éthanol | |||
|---|---|---|---|
| |||
| Général | |||
| Nom IUPAC | |||
| Synonymes | alcool éthylique EtOH | ||
| No CAS | |||
| No EINECS | |||
| Code ATC | D01, D08, V03, V03 | ||
| DrugBank | |||
| PubChem | |||
| ChEBI | |||
| No E | E1510 | ||
| FEMA | |||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore, d'odeur caractéristique. | ||
| Propriétés chimiques | |||
| Formule brute | C2H6O | ||
| Masse molaire | 46,0684 ± 0,0023 g·mol-1 | ||
| Moment dipolaire | 1,66 D | ||
| Diamètre moléculaire | 0,469 nm | ||
| Propriétés physiques | |||
| T° fusion | -117 °C | ||
| T° ébullition | 79 °C | ||
| Solubilité | dans l'eau : miscible, Complète dans les solvants polaires et apolaires (acétone, éther diéthylique) | ||
| Masse volumique |
| ||
| T° d’auto-inflammation | 423 à 425 °C; 363 °C (selon les sources) | ||
| Point d’éclair | coupelle fermée : 13 °C pur 17 °C 95 %vol. 21 °C 70 %vol. 49 °C 10 %vol. 62 °C 5 %vol. | ||
| Limites d’explosivité dans l’air | Inférieure : 3,5 %vol Supérieure : 15 %vol | ||
| Pression de vapeur saturante | à 20 °C : 5,8 kPa | ||
| Viscosité dynamique | 1,20 10-3 Pa·s à 20 °C | ||
| Point critique | 240,85 °C, 6,14 MPa, 0,168 l·mol-1 | ||
| Thermochimie | |||
| S0 | 159,86 J/mol·K | ||
| ΔH0 | − 235,3 kJ/mol | ||
| ΔH0 | − 277,0 kJ/mol | ||
| Cp | 111 J·K-1·mol-1 | ||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 10,43 ± 0,05 eV (gaz) | ||
| Cristallographie | |||
| Classe cristalline ou groupe d’espace | Pc | ||
| Paramètres de maille | a = 5,377 Å b = 6,882 Å | ||
| Volume | 298,57 Å3 | ||
| Densité théorique | 1,025 | ||
| Propriétés optiques | |||
| Indice de réfraction |
| ||
| Précautions | |||
| | |||
| |||
| Phrases R : 11, | |||
| Phrases S : 2, 7, 16, | |||
| | |||
| |||
| | |||
|
3 2 0 | |||
| | |||

Danger | |||
| | |||
| Groupe 1 : Cancérogène pour l'homme | |||
| Inhalation | ébriété, nausée, vomissements | ||
| Peau | aucun effet | ||
| Yeux | dangereux | ||
| Ingestion | ébriété, nausée, vomissements, coma éthylique (pouvant entraîner la mort) | ||
| Écotoxicologie | |||
| DL | 5 à 20 g·kg-1 | ||
| CL | 20 000 à 30 000 ppm pendant 4 à 6 heures | ||
| LogP | -0,32 | ||
| Seuil de l’odorat | bas : 49 ppm haut : 716 ppm | ||
| Données pharmacocinétiques | |||
| Métabolisme | au niveau du foie en aldéhyde acétique puis acide acétique, à ~100 mg·kg-1 par heure | ||
| | |||
L’éthanol, ou alcool éthylique, est un alcool primaire, possédant la structure semi-développée suivante : CH3-CH2-OH. En chimie, l’éthanol est usuellement désigné par l’abréviation EtOH. C’est un liquide incolore, miscible à l'eau en toutes proportions.
Dans la vie courante, il est souvent simplement appelé « alcool », car l'éthanol est l'alcool qui se retrouve dans toutes les boissons alcoolisées. Dans la pharmacopée européenne, "éthanol" désigne l’éthanol absolu, c'est-à-dire pur à 100 % (sans eau), en opposition à l'éthanol à 95% ou 70% que l'on trouve en pharmacie. À cela, s'ajoute la qualité "alcool Ph. Eur." (Pharmacopée européenne) qui désigne une qualité d'éthanol dont on a quantifié de nombreuses traces et impuretés. La norme Pr Eur autorise un certain pourcentage d'eau (4 %). Ses synonymes sont esprit de vin, alcool de grain. L'alcoolisme est la consommation excessive de boissons contenant de l'éthanol.
Historiquement, l'éthanol a été produit par fermentation directe de sucres naturels : la production de vin ou de bière fermentée est attestée dans l'empire babylonien dès 3000 av. J.-C. Les premières obtentions pures sont probablement dues aux alchimistes perses qui développèrent l'art de la distillation au VIIIe et IXe siècle de l'ère chrétienne.
On le fabrique aussi industriellement par hydratation de l'éthylène.
L'éthanol est utilisé comme intermédiaire de synthèse dans l'industrie chimique et comme solvant. C'est aussi un désinfectant. Il a été utilisé pour la conservation de la viande.
En Amérique du Sud et surtout au Brésil, certaines essences disponibles à la pompe peuvent comporter jusqu'à 20 % d'éthanol et portent le nom d’ethanol blend.
En France, le gouvernement a lancé officiellement fin 2006 l'E85, un mélange de 85 % d'éthanol et de 15 % d'essence comme biocarburant. Il est disponible dans plusieurs centaines de stations-service depuis la fin de l'année 2007. Un mélange E10 avec 10 % d'éthanol est disponible depuis avril 2009.