Acide bromoacétique - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Acide bromoacétique | |||||
|---|---|---|---|---|---|
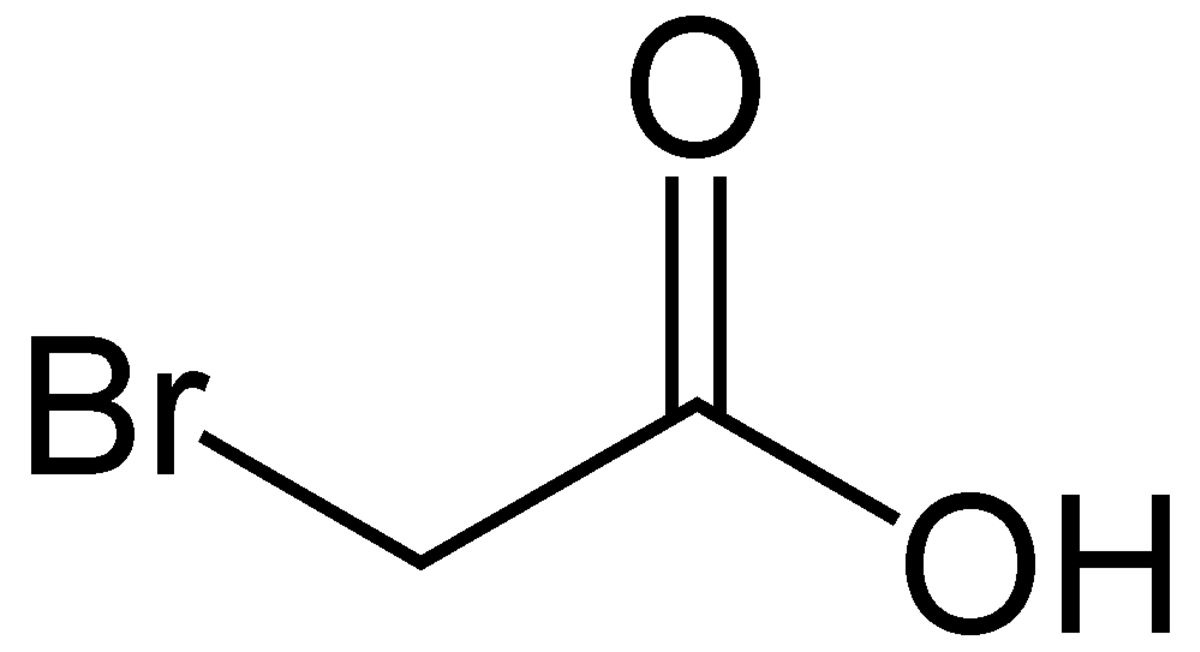
| |||||
| Général | |||||
| Nom IUPAC | |||||
| No CAS | |||||
| No EINECS | |||||
| SMILES | |||||
| InChI | |||||
| Apparence | cristaux incolores | ||||
| Propriétés chimiques | |||||
| Formule brute | C2H3BrO2 | ||||
| Masse molaire | 138,948 ± 0,003 g·mol-1 | ||||
| pKa | 2,69 | ||||
| Propriétés physiques | |||||
| T° fusion | 50 °C | ||||
| T° ébullition | 208 °C | ||||
| Solubilité | 93,8 g·l-1 (eau, 25 °C) | ||||
| Masse volumique | 1,93 g·cm-3 (20 °C) | ||||
| Point d’éclair | > 112 °C (coupelle fermée) | ||||
| Pression de vapeur saturante | 0,07 mbar (20 °C)0,17 mbar (30 °C)0,95 mbar (50 °C) | ||||
| Propriétés optiques | |||||
| Indice de réfraction | 1,4804 (50 °C) | ||||
| Précautions | |||||
| | |||||
| |||||
| Phrases R : 23/24/25, 35, 43, 50, | |||||
| Phrases S : (1/2), 26, 36/37/39, 45, 61, | |||||
| | |||||
| |||||
| | |||||
|
1 3 0 | |||||
| Écotoxicologie | |||||
| DL | 100 mg·kg-1 (souris, oral) 66 mg·kg-1 (souris, i.p.) | ||||
| LogP | 0,41 | ||||
| Composés apparentés | |||||
| Autres composés | acide chloroacétique | ||||
| | |||||
L'acide bromoacétique (ou monobromoacétique) est un composé organique dérivé de l'acide acétique (acide éthanoïque), où l'un des atomes d'hydrogène du groupement méthyle a été substitué par un atome de brome. Ses sels sont appelés bromoacétates.
Propriétés
L'acide bromoacétique se présente sous la forme de cristaux incolores ayant une odeur âcre, qui fondent vers 50 °C et se dissolvent facilement dans l'eau, l'éthanol, l'éther diéthylique et dans d'autres solvants organiques. Sa solution aqueuse est fortement acide, beaucoup plus acide que l'acide acétique (pKa de 2,69 contre 4,76 pour ce dernier), car l'anion bromoacétate ainsi formé est stabilisé par l'atome de brome, électronégatif, et qui permet ainsi de mieux délocaliser la charge négative dans la molécule. Il agit d'électrons et distribués (délocalisées) charge négative de l'anion sur la molécule entière.
Utilisations
L'acide bromacétique est un produit de départ pour de nombreuses synthèses, par exemple de pesticides ou de médicaments. Il a été utilisé de façon directe comme conservateur alimentaire, mais cette utilisation est désormais interdite dans la plupart des États.
L'acide bromacétique est un alkylant fort et possède un effet inhibiteur sur les enzymes portant un groupement -SH (thiol), -OH (alcool) ou NH2 sur leur site actif. Il a autrefois été utilisé pour adoucir le vin français. Un scandale éclata dans les années 1980 en RFA quand fut découvert son utilisation comme conservateur de la bière
Les esters volatiles de l'acide bromoacétique sont utilisés comme gaz lacrymogènes ; ils sont irritants pour le système respiratoire et les yeux, et peuvent être nocifs. À des concentrations plus élevées, ils sont corrosifs et peuvent causer des dommages permanents aux yeux.





















































