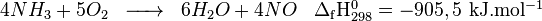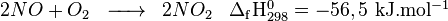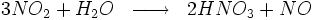Acide nitrique - Définition
La liste des auteurs de cet article est disponible ici.
Production et synthèse
L’acide nitrique dilué est obtenu en mélangeant du dioxyde d’azote (NO) avec de l’eau ; les solutions commerciales comprennent généralement entre 52% et 68% d’acide nitrique. Les solutions plus concentrées sont obtenues par distillation. L’acide nitrique formant un azéotrope avec l’eau dans une proportion de 68% d’acide nitrique et 32% d’eau, l’obtention d’acide nitrique très pur impose de le distiller en présence d’acide sulfurique. Quand la solution comprend plus de 86% d’acide nitrique, il est dit « fumant » et existe en deux variétés : blanche et rouge. L’acide nitrique fumant blanc est aussi appelé 100% car quasiment (moins de 2%) sans eau.
La production commerciale de l’acide nitrique est faite par le procédé Ostwald et se réalise en 3 étapes à partir de l’ammoniac :
En premier, l’ammoniac est oxydé en présence d’un catalyseur comme le platine rhodié, pour former du monoxyde d’azote (NO) (étape fortement exothermique) :
Puis le monoxyde d’azote est oxydé par l’oxygène (O2) et produit du dioxyde d’azote (NO2) :
Enfin, le dioxyde d’azote est dissout dans l’eau selon la réaction :
pour produire l’acide nitrique dilué.
Le monoxyde d’azote produit est recyclé, et l’acide nitrique concentré par distillation jusqu’à un maximum de 68% (azéotrope du mélange acide nitrique - eau). Les concentrations plus élevées sont atteintes par traitement au nitrate de magnésium (Mg(NO3)2). Globalement, ce procédé permet d’atteindre un rendement de 96%.
L’acide nitrique peut également être obtenu en faisant réagir du nitrate de potassium (KNO3) et de l’acide sulfurique concentré (H2SO4), puis en distillant le mélange à 83 °C jusqu’à ce qu’il ne reste plus dans le milieu qu’un solide blanc cristallisé composé de KHSO4. L’acide nitrique obtenu est de acide nitrique fumant rouge. L’acide nitrique fumant blanc peut être obtenu en éliminant les oxydes d’azote dissous en réduisant la pression à 1/3 d’atmosphère environ durant 10-30 minutes. (L’acide nitrique fumant rouge contient une quantité non négligeable d’oxydes d’azote, d’où sa couleur rouge, tandis que l’acide nitrique fumant blanc ne peut contenir qu’un maximum de 0,5% de NO2).
La production mondiale annuelle d’acide nitrique est de l’ordre de 60 millions de tonnes.
Sécurité
L’acide nitrique est un acide fort, qui peut provoquer de graves brûlures. L’inhalation des vapeurs peut entraîner un œdème pulmonaire. Au contact d’acide nitrique concentré, la peau humaine se teint en jaune du fait de réactions avec la kératine. C’est un composé modérément toxique avec une dose létale de 430 mg·kg-1. C’est également un oxydant puissant qui réagit vivement avec les réducteurs et les matières combustibles pouvant occasionner des explosions.