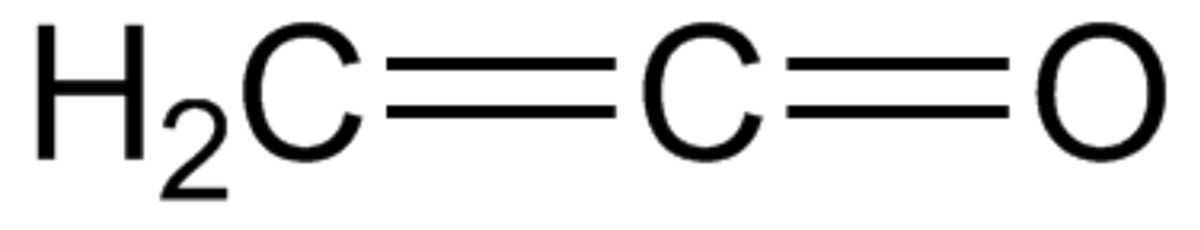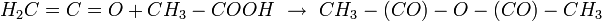Cétène (molécule) - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Cétène (molécule) | |
|---|---|
| |
| Général | |
| Nom IUPAC | |
| Synonymes | carbométhène céto-éthylène |
| No CAS | |
| No EINECS | |
| PubChem | |
| ChEBI | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C2H2O |
| Masse molaire | 42,0367 ± 0,002 g·mol-1 |
| Moment dipolaire | 1,42215 D |
| Propriétés physiques | |
| T° fusion | -150 °C |
| T° ébullition | -49 °C |
| Limites d’explosivité dans l’air | 5,5 - 18 Vol%. |
| Point critique | 65,0 bar, 106,85 °C |
| Thermochimie | |
| ΔH0 | -87,24 kJ·mol-1 |
| ΔH° | 20,4 kJ·mol-1 |
| Cp | 51,75 J·K-1·mol-1 (gaz,25 °C) |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 9,617 ± 0,003 eV (gaz) |
| Précautions | |
| | |
|
0 3 0 | |
| | |


| |
| Écotoxicologie | |
| DL | 1,3 g·kg-1 (rat, oral) |
| | |
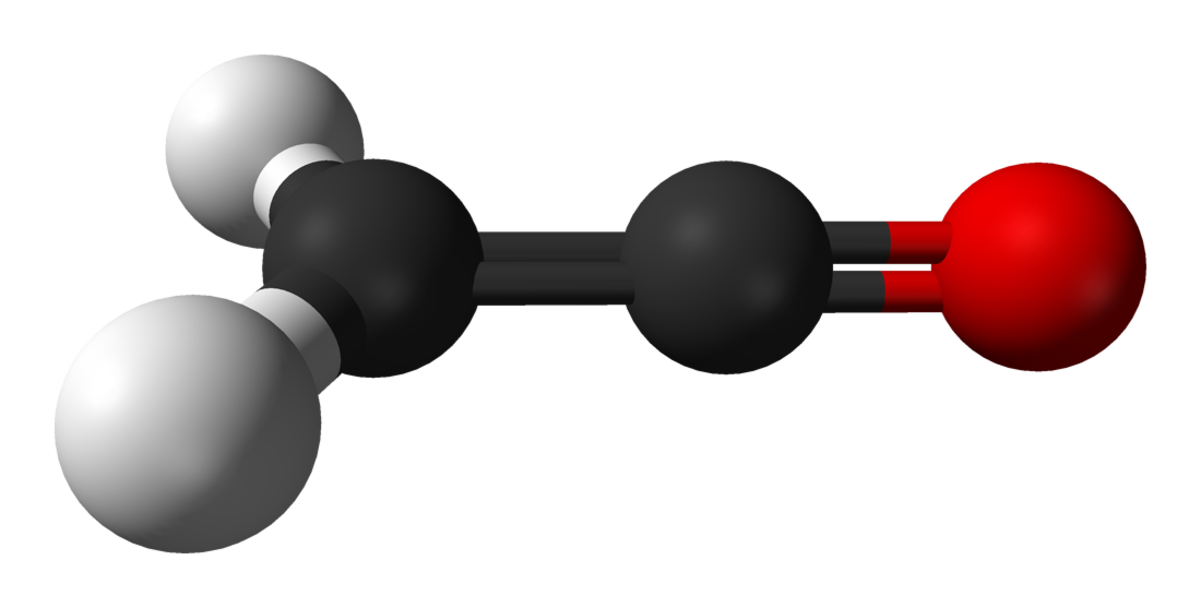
Le cétène est un gaz toxique de formule semi-développée H2C=C=O, instable dans les conditions normales de température et de pression. Son tautomère est l'éthynol.
Propriétés physico-chimiques
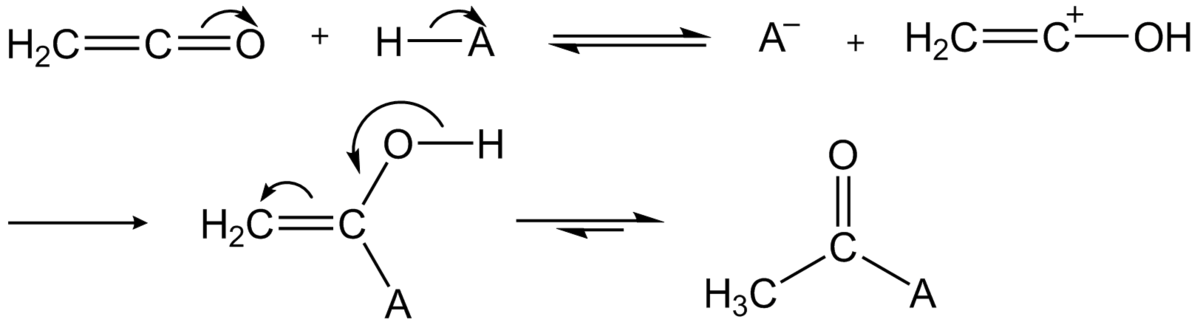
Le cétène est un agent d'acétylation très puissant.
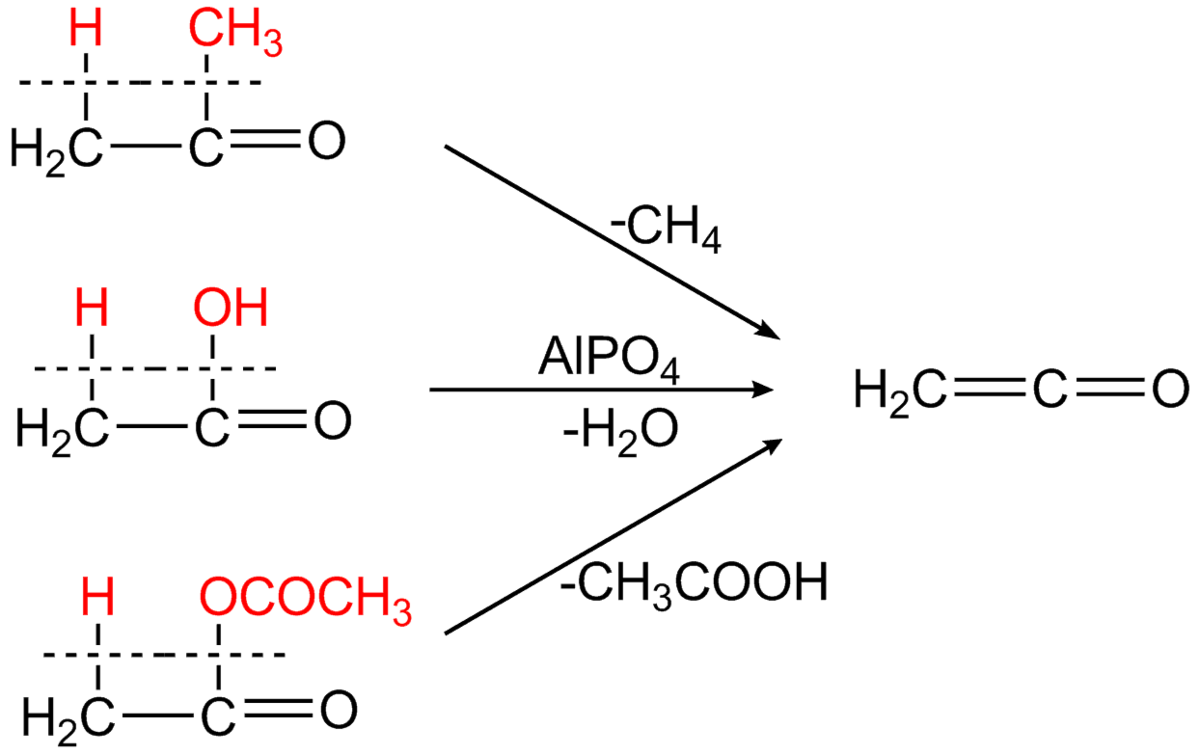
Production et synthèse
La principale voie de synthèse du cétène est la pyrolyse de l'acide acétique. Ce dernier est évaporé et chauffé à une température de 740 à 760 °C, puis du phosphate de triéthyle est ajouté comme catalyseur ainsi que du l'ammoniaque. L'ammoniaque empêche la recombinaison de l'eau et du cétène. Le mélange est ensuite refroidit à moins de 100 °C pour condenser l'eau et l'acide acétique n'ayant pas réagit, le cétène est ensuite absorbé dans un liquide de conditionnement ou récupéré sous forme de dicétène via une pompe à vide.
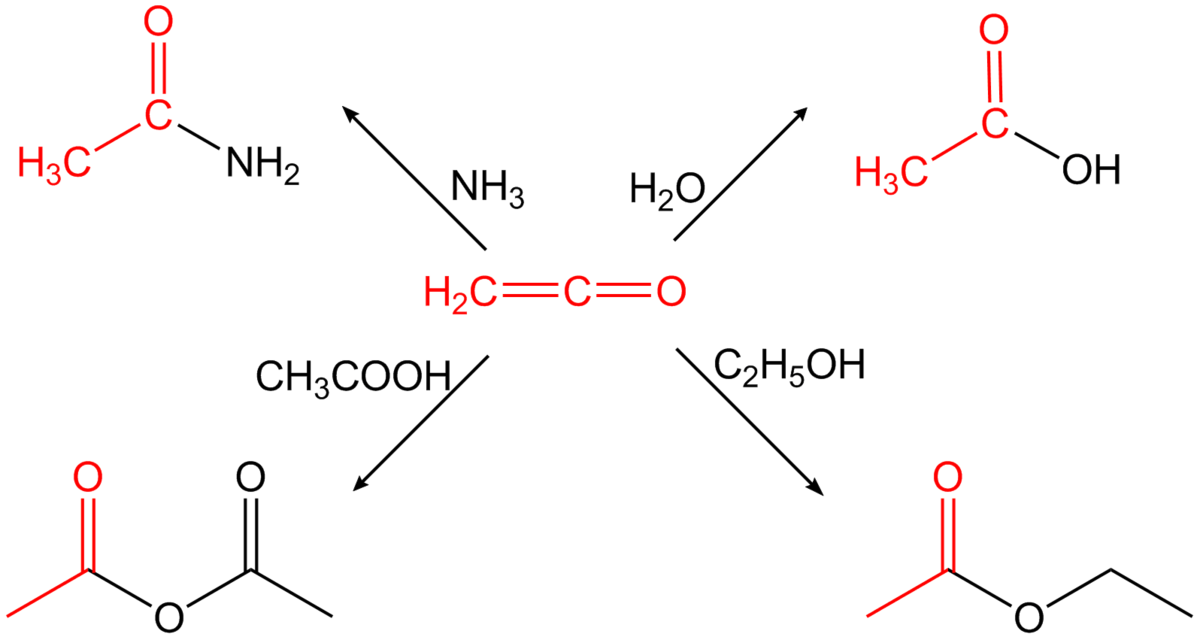
Utilisation
- Production de l'anhydride acétique
La majeure partie de la production du cétène est utilisée pour la production de l'anhydride acétique. Toutefois ce procédé est concurrencé par la carbonylation de l'acétate de méthyle.
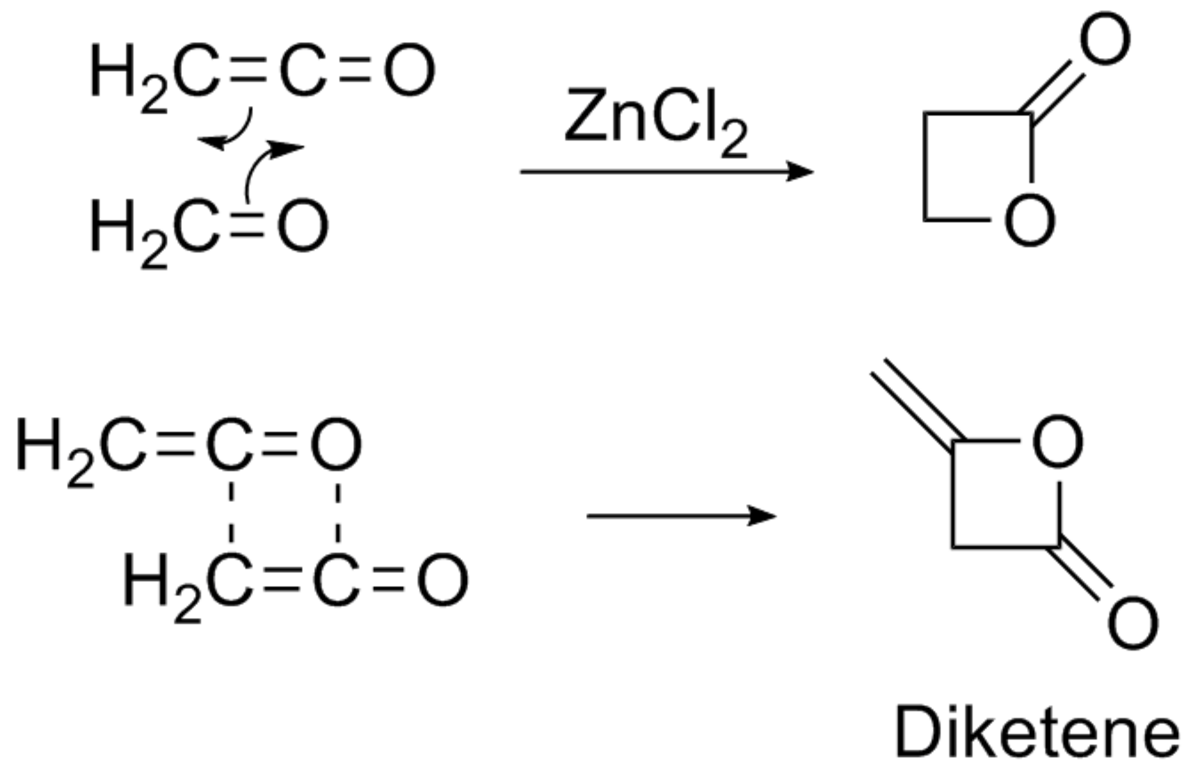
- Production du dicétène
La seconde utilisation du cétène est la production du dicétène par dimérisation contrôlée.
- Production de l'acide sorbique
La réaction du cétène avec le crotoaldéhyde produit le bêta-lactone ou du polyester. Ces derniers sont ensuite convertis par voie thermique ou par voie ctalytique en acide sorbique.