Curiethérapie - Définition
La liste des auteurs de cet article est disponible ici.
Sources de radiation
Les radioéléments utilisés
Le radioélément de base utilisé en curiethérapie est actuellement l'iridium 192 noté 192Ir. Il se présente sous forme de fils souples et sécables entourés d'une gaine en platine dont le diamètre varie entre 0,3 et 0,6 millimètres ou sous forme d'épingle simple ou double dont le diamètre extérieur est de 0,5 millimètres. Les branches de l'épingles ont une longueur comprise entre 30 et 50 millimètres pour un écartement de 12 millimètres.
L'iode 125 est quant à lui utilisé pour le traitement des prostates. Il est conçut sous forme de grains de titane de 4,5 millimètres pour 0,8 millimètres qui renferment deux sphères d'iode. Ces grains sont implantés directement à l'intérieur de la masse tumoral en implant permanent.
D'autres éléments sont beaucoup moins utilisés comme le césium 137, le cobalt 60, le palladium 103 ou encore le strontium 90.
| Radionucléides | Type | Demi-vie | Énergie |
|---|---|---|---|
| Caesium-137 (137Cs) | Rayons γ | 30.17 ans | 0.662 MeV |
| Cobalt-60 (60Co) | Rayons γ | 5.26 ans | 1.17, 1.33 MeV |
| Iridium-192 (192Ir) | Rayons γ | 74.0 jours | 0.38 MeV (milieu) |
| Iodine-125 (125I) | Rayons X | 59.6 jours | 27.4, 31.4 and 35.5 keV |
| Palladium-103 (103Pd) | Rayons X | 17.0 jours | 21 keV (milieu) |
| Ruthenium-106 (106Ru) | Rayons β | 1.02 ans | 3.54 MeV |
Les gaines
Les sources radioactives ne sont jamais mises en contact direct du patient. Les grains radioactifs sont encapsulés dans des gaines insérées à l'intérieur du patient à proximité direct de la zone à traiter.
Deux types de gaines protectrices sont utilisées. Il s'agit des simples enrobages entourant les billes radioactives pour les éléments à bas débit de dose et des projecteurs qui sont des capsules métalliques contenant les éléments à haut débit de dose et permettant le contrôle du temps d'irradiation de la tumeur. Cette dernière permet de rentrer et sortir mécaniquement l'élément radioactif afin de protéger le personnel lors de sa manipulation et de contrôler la dose apportée au patient. Cette capsule absorbe la plupart du rayonnement émis.
Procédure
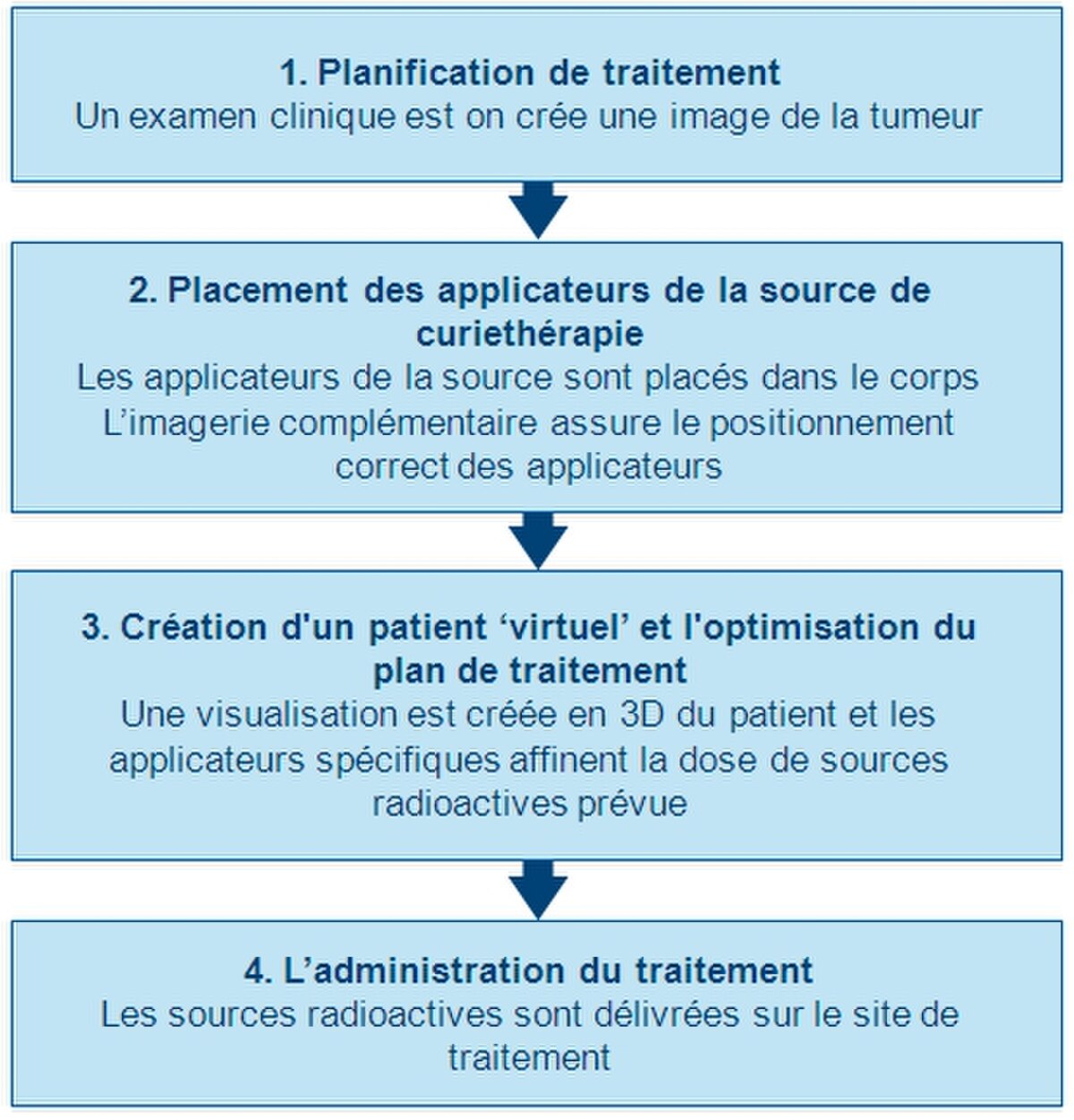
Planification initiale
Afin de planifier avec précision la procédure de curiethérapie, un examen clinique approfondi est effectuée afin de comprendre les caractéristiques de la tumeur. En outre, une gamme de modalités d'imagerie peut être utilisée pour visualiser la forme et la taille de la tumeur et sa relation avec les tissus environnants et les organes. Il s'agit notamment de la radiographie, de l'échographie, de la tomographie axiale par ordinateur (CT ou CAT) et de l’analyse et l'imagerie par résonance magnétique (IRM). Les données de plusieurs de ces sources peuvent être utilisées pour créer une visualisation 3D de la tumeur et des tissus environnants.
En utilisant cette information, un plan de la répartition optimale des sources de rayonnement peut être développé : les supports de sources (instruments), qui sont utilisés pour apporter le rayonnement au site de traitement sont placés et positionnés. Les applicateurs qui sont non radioactifs et sont généralement des aiguilles ou cathéters en plastique. Le type spécifique de l'applicateur utilisé dépendra du type de cancer traité et des caractéristiques de la tumeur cible. Cette planification initiale permet de garantir que les ‘points froids’ (trop peu irradiés) et des ‘points chauds’ (trop irradiés) sont évités pendant le traitement. Ils pourraient se traduire respectivement par l'échec du traitement ou des effets secondaires.
Imagerie et insertion de l'applicateur
Avant que les sources radioactives ne soient délivrées sur le site de la tumeur, les applicateurs doivent être insérées et positionnée correctement en fonction du planning initial.
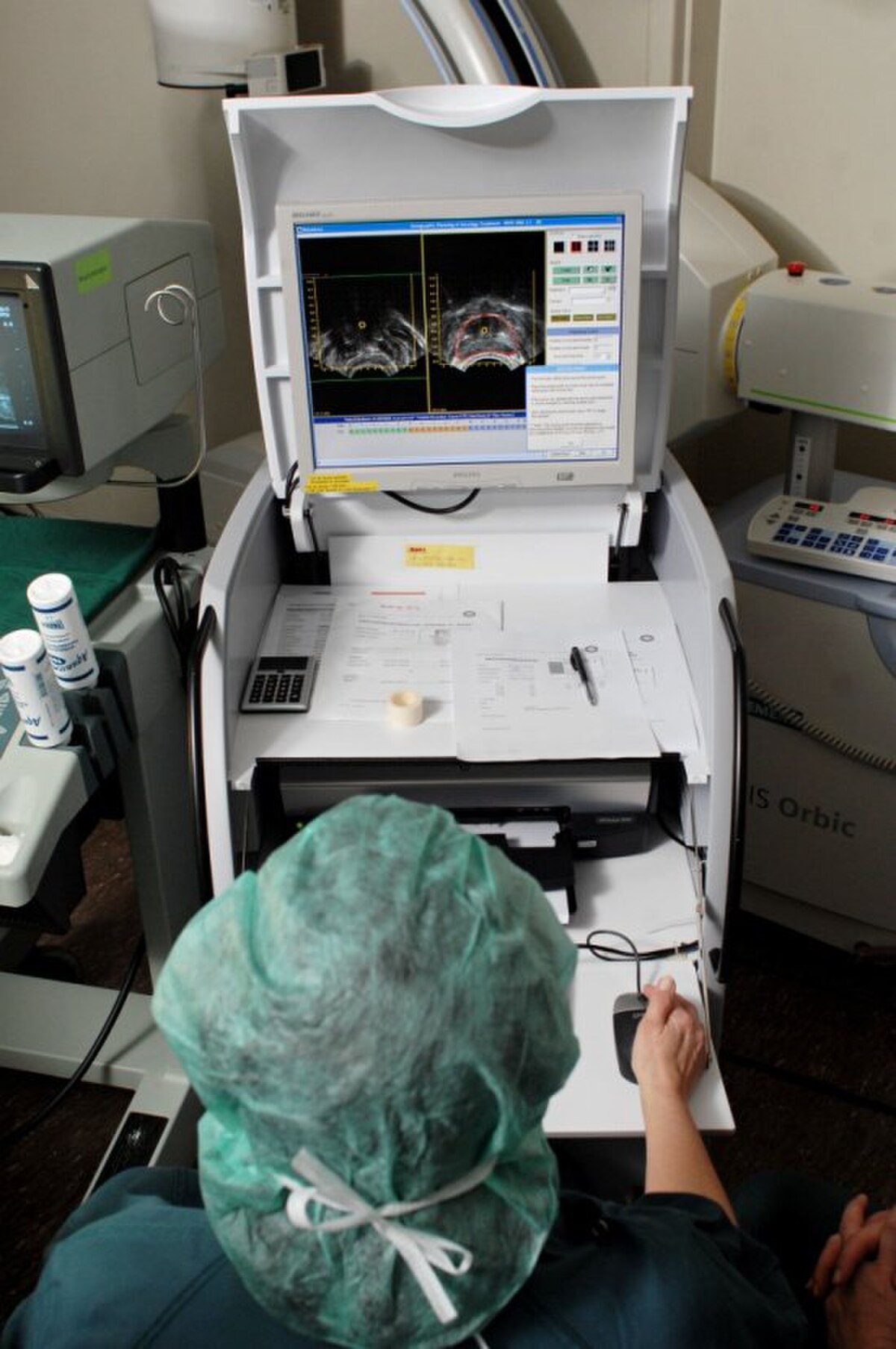
Les techniques d'imagerie, telles que les rayons X, la fluoroscopie et l’échographie sont généralement utilisées pour aider au placement des applicateurs sur leurs positions exactes et de pour affiner le plan de traitement. Les scannes CAT et L'IRM peuvent aussi être utilisés. Une fois que les applicateurs sont insérés, ils sont maintenus contre la peau en utilisant des sutures ou du ruban adhésif pour les empêcher de se déplacer. Une fois que les applicateurs soient bien positionnés, l'imagerie complémentaire peut être réalisée pour orienter la planification du traitement détaillé.
Création d’un patient virtuel
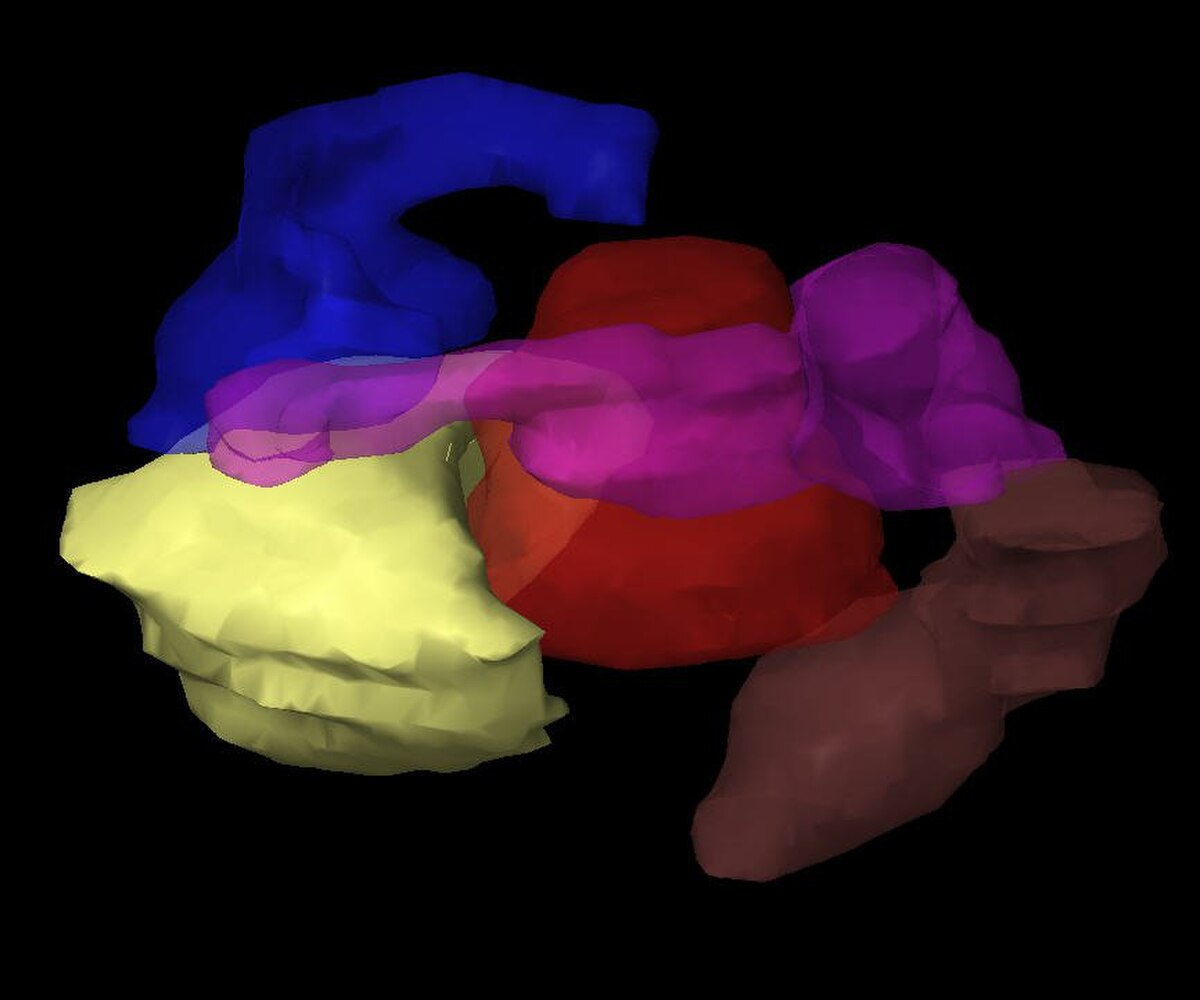
Les images du patient portant les applicateurs in situ sont importées dans un logiciel de planification du traitement. Le patient est alors amené dans une salle dédiée et blindée pour le traitement. Le logiciel de planification du traitement permet l’acquisition de multiples images 2D du site de traitement. Ces images sont traduites en un ‘patient virtuel’ 3D, dans lequel la position des applicateurs peuvent être définis. Les relations spatiales entre les applicateurs, le site de traitement et les tissus environnants sains sont dans ce ‘patient virtuel’, une copie des relations dans le patient réel.
Optimisation du plan d'irradiation
Pour identifier la optimale répartition spatiale et temporelle des sources de rayonnement dans les applicateurs sur ses cibles, le logiciel de planification du traitement place dans un premier temps les sources de rayonnement virtuelles à l'intérieur du patient virtuel. Le logiciel montre une représentation graphique de la distribution de l'irradiation. Cette étape sert de guide à l'équipe de curiethérapie pour affiner la répartition des sources et de fournir un plan de traitement qui est parfaitement adaptée à l'anatomie de chaque patient. Ensuite, la radiation du patient réel peut commencer. Cette approche est parfois appelée ‘peinture de la dose’.
Les sources de rayonnement utilisées pour la curiethérapie sont toujours enfermées dans une capsule protectrice non radioactive. Les sources peuvent être délivrées manuellement, mais sont plus souvent délivrées à travers d’une technique appelée ‘afterloading’, effectué par le biais d’un projecteur de source.
La délivrance manuelle de la curiethérapie est limitée à certaines applications BDD, en raison du risque d'exposition aux rayonnements des personnels cliniques.
A l’opposé, l’‘afterloading’ permet le positionnement précis des applicateurs au site du traitement non radioactifs. Une fois en place, les applicateurs sont chargés avec les sources de rayonnement. En ‘afterloading’ manuel, la source est délivrée à l'applicateur par un opérateur.
Les systèmes d’‘afterloading’ à distance assurent une protection contre l'exposition aux rayonnements des professionnels de santé puisque la source de rayonnement reste confinée. Une fois que les applicateurs sont positionnés correctement dans le patient, ils sont reliés au projecteur de source (‘afterloader’ qui contient les sources radioactives) par une série de tubes de liaison qui guide. Le plan de traitement est envoyé à l’‘afterloader’, qui après contrôle libère les sources le long des tubes de guidage jusqu’à l'applicateur. Cette procédure ne démarre que lorsque le personnel a quitté la salle de traitement. Les sources restent en place pour une période définie selon le plan de traitement. Ensuite, elles retournent à l’‘afterloader’ par les tubes de liaison.
Quand le traitement radioactif est terminé, les applicateurs sont soigneusement retirés du corps. En temps normal, les patients récupèrent rapidement après un traitement par curiethérapie, ce qui leur permet d’être soignés en service ambulatoire.