Phalloïdine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Phalloïdine | |
|---|---|
| Général | |
| No CAS | |
| Propriétés chimiques | |
| Formule brute | C35H48N8O11S |
| Masse molaire | 788,868 ± 0,041 g·mol-1 |
| | |
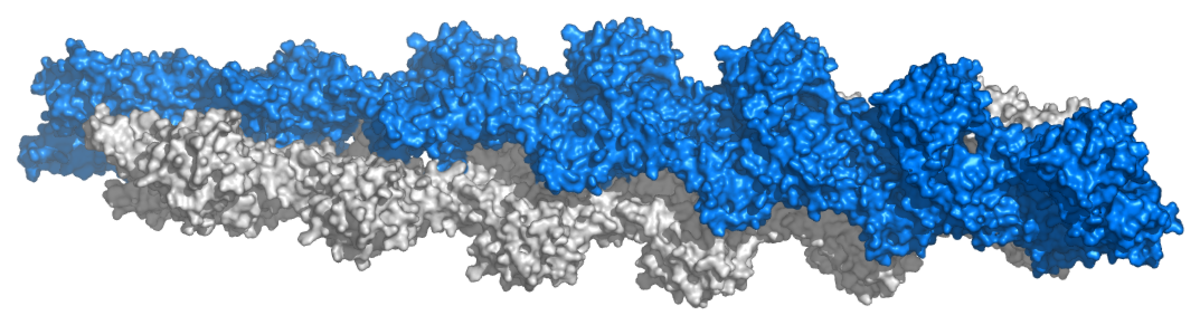
La phalloïdine fait partie des toxines extraites de l'amanite phalloïde (A. phalloides) connues sous le nom de phallotoxines. Elle se lie à l'actine, empêchant sa dépolymérisation et empoisonnant la cellule. Cette propriété de liaison avec l'actine lui permet d'être utilisé en imagerie cellulaire afin de les visualiser.
Effets sur la cellule
La phalloïdine se lie spécifiquement à l'interface entre les sous-unités d'actine F, bloquant les sous-unités adjacentes ensemble. Ce heptapeptide bicyclique qui se lie plus facilement aux filaments qu'aux monomères d'actine, conduisant à la diminution de la constante de vitesse de dissociation des sous-unités d'actine à la fin du filament, ce qui le stabilise en prévenant sa dépolymérisation. De plus, la phalloïdine inhibe l'activité hydrolysase d'ATP de l'actine F. Ainsi, la phalloïdine piège les monomères d'actine dans une conformation distincte de l'actine G et elle stabilise la structure de l'actine F en réduisant de façon importante la constante de vitesse pour la dissociation des monomères, un phénomène associé au piégeage de l'ADP. Globalement, la phalloïdine se trouve réagir stœchiométriquement avec l'actine, promouvant sa polymérisation et stabilisant les polymères.
Cette toxine a des effets différents selon sa concentration dans la cellule. Lorsqu'elle est introduite dans le cytoplasme à de faibles concentrations, la phalloïdine recrute les formes les moins polymérisées d'actine cytoplasmique, ainsi que les filaments, dans des « îlots » stables d'agrégats de polymères, mais elle n'interfère pas avec les câbles de tension, c'est-à-dire les épais faisceaux de microfilaments. Wehland et al. notèrent également qu'a de plus fortes concentrations, la phalloïdine induit une contraction cellulaire.
Limites des phalloïdines
Les phalloïdines passent difficilement à travers les membranes cellulaires, ce qui les rend moins efficaces dans les expériences utilisant des cellules vivantes. De plus, Les cellules traitées à la phalloïdine présentent un nombre important d'effets toxiques et meurent fréquemment. Finalement, les cellules exposées à la phalloïdine présentent un niveau plus important d'actine associée à leurs membranes plasmatiques, et les microinjections de phalloïdine dans une cellule vivante changent la distribution de l'actine ainsi que la mobilité cellulaire.
Utilisation en imagerie
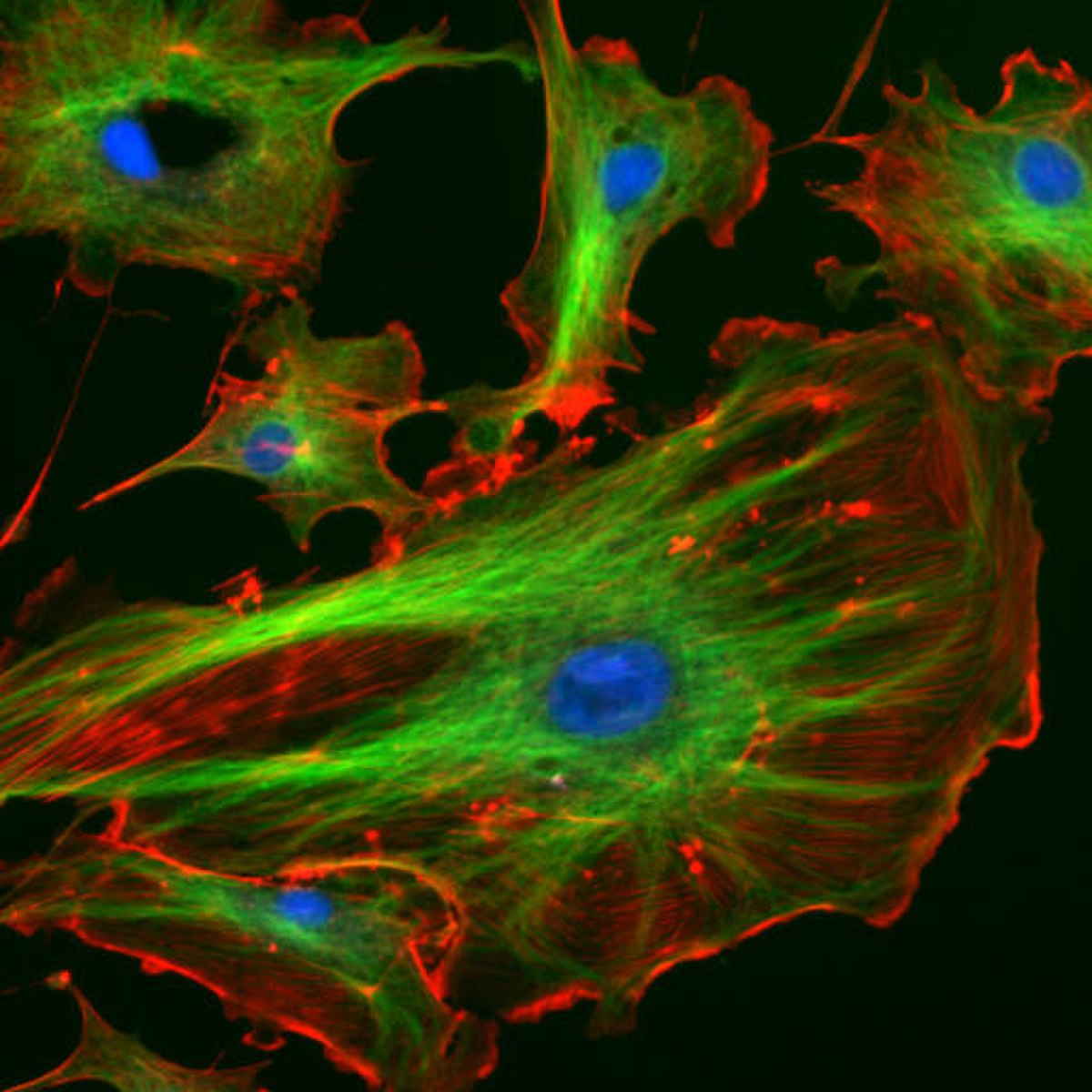
Les propriétés de la phalloïdine font d'elle un outil intéressant dans l'étude de la distribution d'actine F dans les cellules en la couplant avec des analogues fluorescents et en les utilisant pour marquer les filaments d'actine en microscopie optique. Les dérivés fluorescents de la phalloïdine se sont avérés extrêmement utiles dans la localisation des filaments d'actine dans les cellules vivantes ou fixées, ainsi que dans la visualisation d'un filament d'actine individuel in vitro.
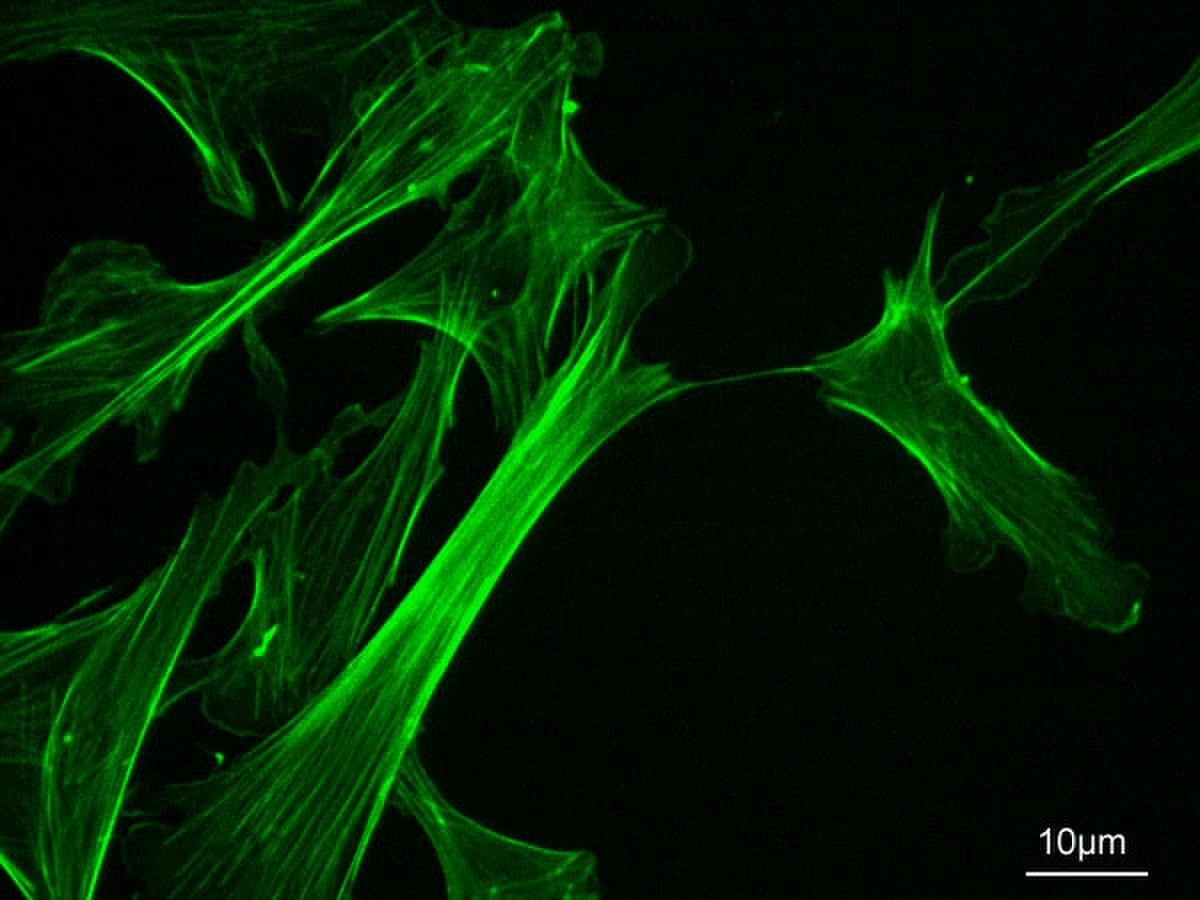
Une technique de haute résolution a été développée pour détecter l'actine F à la lumière et en microscopie électronique en utilisant la phalloïdine conjuguée à l'éosine qui agit comme un marqueur fluorescent. Dans cette méthode connue sous le nom de fluorescence photo-oxydative, des molécules fluorescentes peuvent être utilisées pour conduire à une oxydation de la diaminobenzidine (DAB) afin de créer un produit de réaction qui est dense aux électrons et détectable par un microscope photonique. La quantité de fluorescence observée peut être considérée comme une mesure quantitative de la quantité de filaments d'actine présents dans la cellule si l'on utilise une quantité saturante de phalloïdine fluorescente.
Par conséquent, la microscopie immunofluorescente couplée avec des microinjections de phalloïdine peut être utilisée pour évaluer les fonctions directes ou indirectes de l'actine cytoplasmique à différents stades de la formation du polymère (Wehland et al., 1977). C'est pourquoi la phalloïdine fluorescente peut être utilisée comme un outils important dans l'étude des réseaux d'actine à haute résolution.