Polychlorure de vinyle - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Polychlorure de vinyle | |
|---|---|
| |
| Général | |
| Synonymes | PVC |
| No CAS | |
| PubChem | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | (C2H3Cl)n n = 700 à 1500 |
| Masse molaire | 62,498 ± 0,004 g·mol-1 |
| Propriétés physiques | |
| T° transition vitreuse | 80 °C |
| T° fusion | >180 °C (décomposition) |
| Masse volumique | 1,38 g·cm-3 |
| T° d’auto-inflammation | 600 °C |
| Limites d’explosivité dans l’air | inférieure : 60 g·m-3 |
| Propriétés électroniques | |
| constante diélectrique | 3,39 (1 kHz, 25 °C) 2,9 (1 MHz, 25 °C) 2,8 (1 GHz, 25 °C) 5,3 (1 kHz, 100 °C) 3,3 (1 MHz, 100 °C) 2,7 (1 GHz, 100 °C) |
| Propriétés optiques | |
| Indice de réfraction |
|
| Précautions | |
| | |
| Produit non contrôlé | |
| | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme | |
| | |
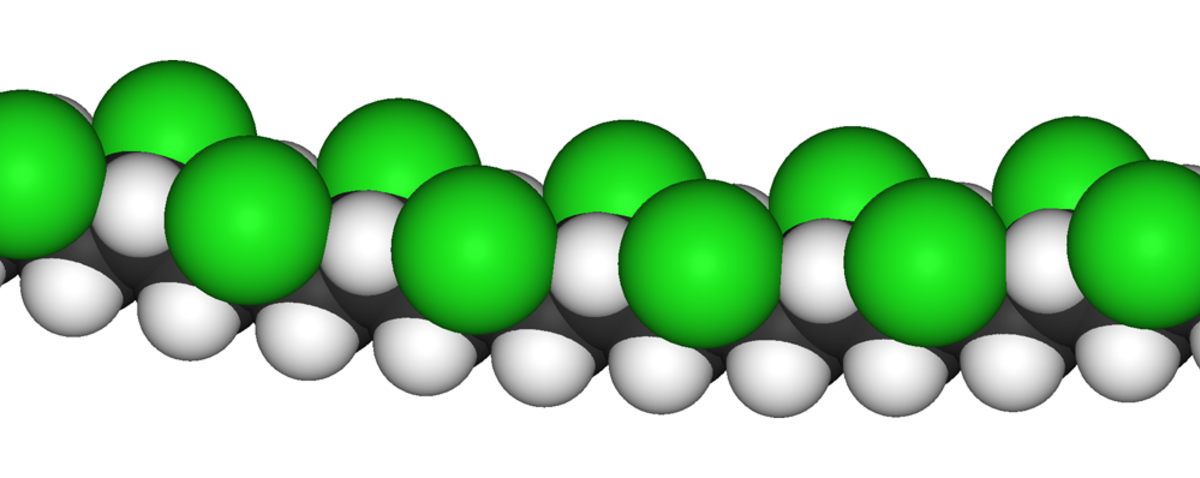
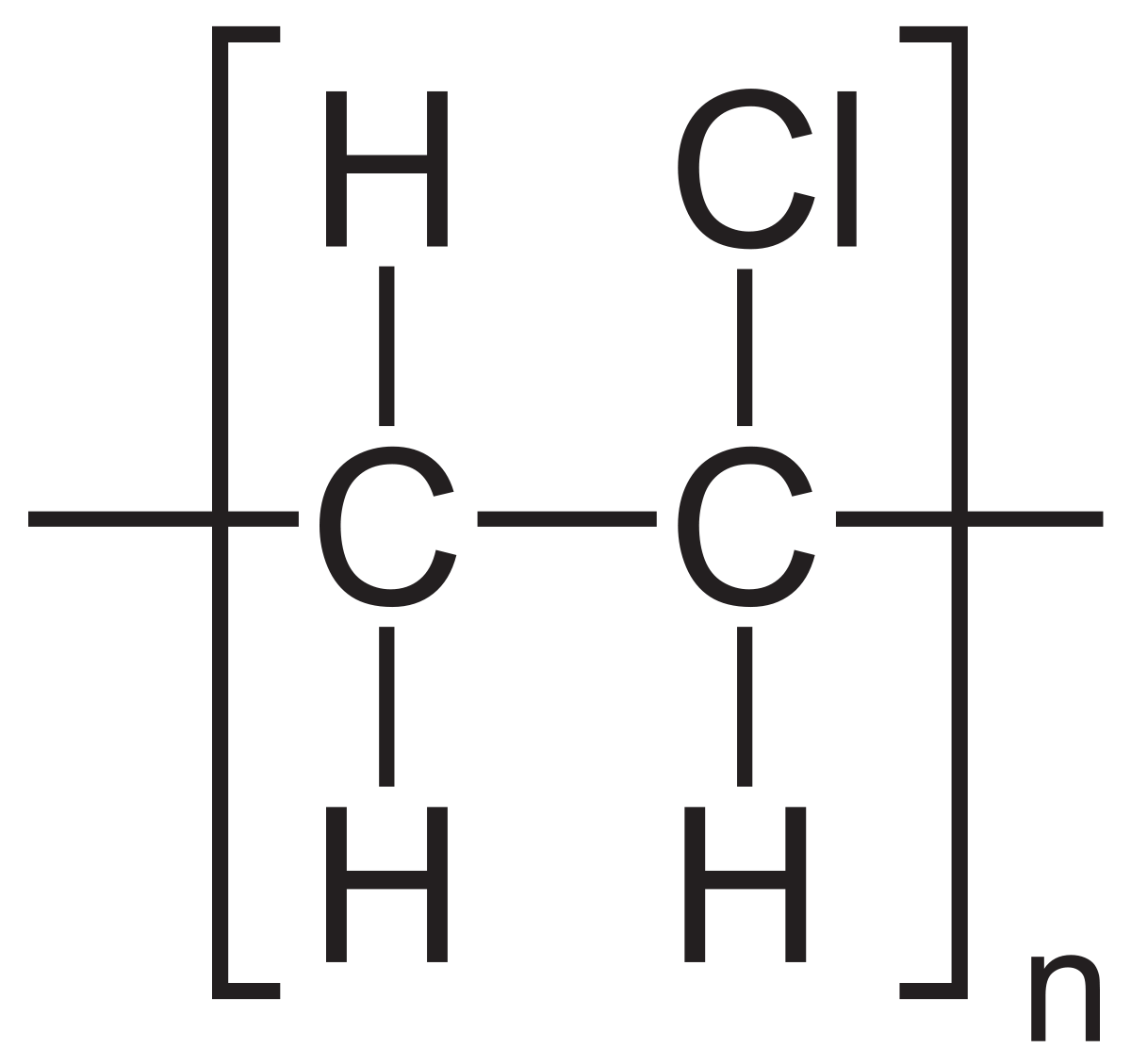
Le polychlorure de vinyle ou chlorure de polyvinyle est un polymère thermoplastique de grande consommation, amorphe ou faiblement cristallin, connu généralement sous le sigle PVC (de l'anglais polyvinyl chloride).
Formule moléculaire
De formule − (CH2 − CHCl)n − , il est obtenu par polymérisation radicalaire du monomère chlorure de vinyle, CH2 = CHCl. Le PVC est un matériau organique.
Synthèse
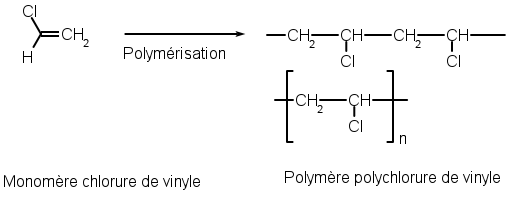
Sa polymérisation est initiée par des radicaux.
Historiquement le monomère de chlorure de vinyle (formule chimique CH2=CHCl) était produit par réaction de l'éthylène avec du chlore gazeux. Aujourd'hui, il s'agit d'une réaction opposant l'éthylène avec l'acide chlorhydrique, en présence d'oxygène, qui est généralement utilisée. Le produit intermédiaire, le dichloroéthane se transforme en chlorure de vinyle sous l'effet de la chaleur.
Le PVC est insoluble dans son monomère.
Historique
Le polychlorure de vinyle a été découvert par accident à au moins deux occasions au cours du XIXe siècle, d'abord en 1835 par Henri Victor Regnault et en 1872 par Eugen Baumann. Dans les deux cas, le polymère est apparu comme un solide blanc dans des bouteilles de chlorure de vinyle après exposition à la lumière solaire. Au début du XXe siècle, les chimistes russes Ivan Ostromislensky et Fritz Klatte ont tous deux tenté d'utiliser le PVC dans des produits commerciaux, mais leurs efforts ne furent pas couronnés de succès à cause des difficultés de transformation du polymère. En 1926, Waldo Semon, en collaboration avec la société B.F. Goodrich, a développé une méthode de plastification du PVC en le mélangeant avec des additifs. Ceci a permis de rendre le matériau plus flexible et plus facile à fabriquer, genèse du succès commercial du PVC.
Plastification et risque toxique
On ajoute très souvent au PVC des plastifiants (pour former par exemple des plastisols) afin d'améliorer certaines caractéristiques (souplesse, allongement à la rupture, tenue au froid et aux chocs, etc.) ou de faciliter la mise en œuvre.
Le PVC souple (plastifié) représente environ 30 % de la consommation de PVC.
Parmi les plastifiants utilisés, de nombreux phtalates sont nocifs. Au cours du temps, ils peuvent migrer (permanence non assurée, due à une incompatibilité avec la matrice polymère) et se déposer en surface (phénomène d’exsudation) des objets souples en PVC. Pour cette raison, leur usage est limité dans les jouets par une directive européenne.
D'autres plastifiants sont autorisés, dans la famille des adipates ou même des huiles végétales (par exemple l'huile de soja). Ils permettent depuis de nombreuses années la fabrication du film étirable alimentaire. Cependant, au contact des corps gras des aliments, certains plastifiants hydrophobes migrent dans la nourriture. D'autres alternatives sont en développement pour remplacer à terme le PVC dans les films alimentaires.