Électrophorèse en gel d'agarose - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
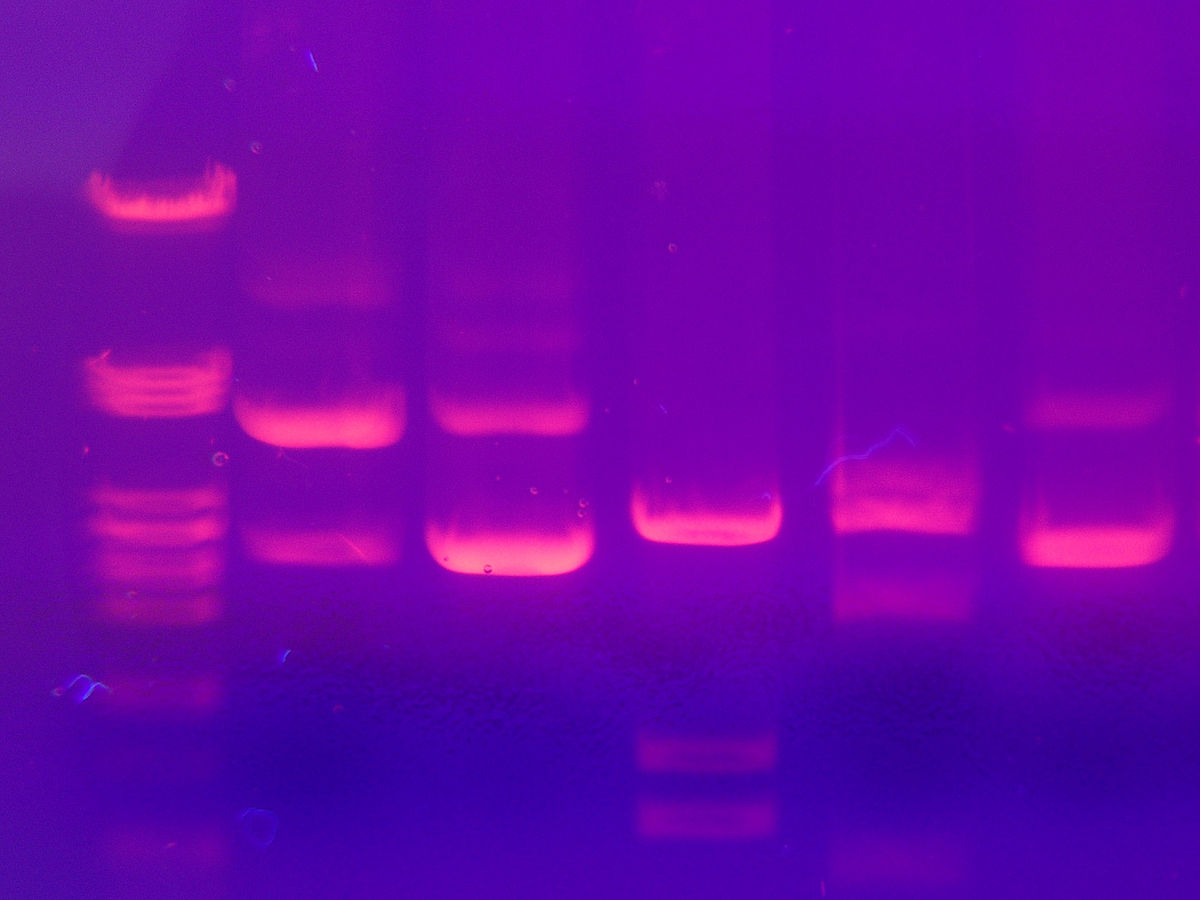
L'électrophorèse en gel d'agarose est une méthode utilisée en biochimie et en biologie moléculaire pour séparer l'ADN, l'ARN ou des protéines en fonction de leur poids moléculaire.
La technique de l'électrophorèse en gel d'agarose est basée sur la séparation des acides nucléiques chargés négativement sous l'effet d'un champ électrique. Cette séparation s'effectue à travers la matrice du gel d'agarose : les molécules de plus petites tailles se déplacent plus rapidement et migreront plus loin que les molécules de tailles supérieures.
Applications
- Estimation du poids moléculaire de fragment d'ADN après une digestion par des enzymes de restriction
- Analyse d'ADN ou d'ARN après une amplification par PCR
- Séparation de fragments ADN digérés avant Southern blot ou d'ARN dans le cas de Northern Blot.
Les avantages de l'électrophorèse en gel d'agarose sont les suivants:
- préparation aisée, rapide, et peu coûteuse des gels d'agarose
- pas de dénaturation des échantillons
- l'agarose plus ferme et moins toxique que le gel de polyacrylamide
- les échantillons peuvent être récupérés en vue d'analyses supplémentaires
Gel d'agarose
On utilise généralement un gel 1% m/v (1 g d'agarose pour 100 ml de volume final) en électrophorèse. Plus on veut un gel discriminant, plus on augmentera le pourcentage d'agarose.
Agarose
L’agarose est un polymère à base d'agar purifié. Différentes puretés d'agarose sont disponibles auprès des fournisseurs. En général, de l'agarose de grande pureté à la solidification lente est utilisé lorsque l'ADN doit être extrait du gel après migration.
Tampons
Il existe un nombre très varié de tampons. Les plus souvent utilisés sont le Tris/Acétate/EDTA (TAE), le Tris/Borate/EDTA (TBE) et le sodium borate (SB).
Le TAE possède le plus faible pouvoir tampon mais produit une meilleure séparation pour les fragments d'ADN de grande taille.
Le SB est relativement nouveau et inefficace pour la séparation de fragments d'ADN d'une taille supérieure à 5000 paires de bases (5 kb). Cependant sa faible conductivité permet l'utilisation d'un plus fort voltage (jusqu'à 35V/cm), ceci réduisant considérablement le temps de migration.
Des fragments d'ADN avec seulement quelques paires de bases de différences sont séparés en utilisant un gel d'agarose à 3% et avec un tampon SB de très faible conductivité (1 mM lithium borate).
Préparation
Exemple pour un mini-gel de 50 ml destiné à séparer des fragments de 2 à 5 kb
- Préparer le moule et le peigne appropriés au nombre et au volume des échantillons à séparer.
- Préparer suffisamment de tampon (TAE, TBE) pour remplir la cuve (par exemple 200 ml) et préparer le gel (50 ml).
- Dans une fiole Erlenmeyer, peser la quantité d'agarose déterminée d'après le tableau suivant et en fonction de la taille des fragments à séparer:
| Concentration d'agarose (% en M/V) | Gamme de tailles idéales (en kb) |
|---|---|
| 0.3 | 5 – 60 |
| 0.6 | 1 – 20 |
| 0.7 | 0.8 – 10 |
| 0.9 | 0.5 – 7 |
| 1.2 | 0.4 – 6 |
| 1.5 | 0.2 – 3 |
| 2.0 | 0.1 – 2 |
- Pour l'exemple, il faudra donc fondre 600 mg d'agarose dans 50 ml de tampon: concentration finale de 1.2%, idéale pour séparer des fragments de 0.6 à 6 kb.
- Dissoudre complètement l'agarose dans le tampon, en plaçant l'Erlenmeyer soit au four à micro-ondes, soit encore dans un bain marie d'eau bouillante, et en agitant de temps en temps. L'agarose est totalement dissout lorsque les grains, initialement visibles sous forme de petites lentilles, ont complètement disparu.
- Mettre sous agitation et laisser refroidir, ou placer dans un bain-marie à environ 50°C (température supportable au toucher). Éventuellement, refroidir plus rapidement en laissant couler un filet d'eau froide le long de l'Erlenmeyer, en agitant constamment. Il est particulièrement important de refroidir l'agarose en dessous de 60°C lors de l'utilisation de moules en PMMA, qui risquent sinon de fondre.
- Si désiré, du bromure d'éthidium peut maintenant être rajouté, à une concentration finale de 0.5 µg/ml. Il est cependant déconseillé d'ajouter à la place du bromure d'éthidium certains autres révélateurs (par exemple du SYBR Gold, un fluorophore semblable au (SYBR Green I) directement dans le gel, car ceux-ci peuvent affecter la mobilité des acides nucléiques lors de l'électrophorèse.
- Couler l'agarose dans le moule avec le peigne et laisser refroidir. Un gel froid et figé prêt à l'emploi se reconnaît par son apparence opalessante lorsqu'il est observé par la tranche, par rapport à un gel encore liquide qui est parfaitement translucide. Emballé dans du film plastique ou dans du tampon (TAE, TBE ou SB), le gel peut alors être conservé à 4°C au réfrigérateur pendant plusieurs jours, avant qu'il ne perde trop d'eau par évaporation. La conservation de gels contenant du bromure d'éthidium dans du tampon n'en contenant pas peut conduire à la diffusion du révélateur hors du gel. Ceci peut faire que la distribution du bromure d'éthidium dans le gel soit inhomogène, ce qui finalement peut affecter l'apparence des bandes (les acides nucléiques, de charge négative, migreront plus vite là où la concentration du révélateur, de charge positive, sera plus faible).
- Juste avant d'effectuer l'électrophorèse, placer le gel dans la cuve et s'assurer qu'il est recouvert de tampon. Retirer ensuite le peigne, charger les échantillons et les standards, et faire migrer en appliquant une tension ou un courant adaptés. La vitesse de migration des acides nucléiques dépendant du champ électrique, on fixe généralement la tension entre 1 et 5 V par cm (distance entre les électrodes) et on laisser varier le courant (parce que la conductivité du gel varie au cours du temps).
Révélation de l'ADN
La méthode révélation la plus utilisée est la révélation au bromure d'éthidium ou BET. Le bromure d'éthidium est un agent d'intercalation couramment utilisé comme marqueur d'acide nucléique dans les laboratoires de biologie moléculaire. Lorsqu'il est exposé à des rayonnements ultraviolets, il devient fluorescent avec une couleur rouge-orangée, 20 fois plus intense lorsqu'il est lié à l'ADN. Cet effet serait dû à l'augmentation de l'hydrophobie de l'environnement, plutôt qu'à une rigidification du cycle benzénique, celui-ci n'étant pas situé entre les paires de bases.
Alternativement, le gel peut être incubé dans un bain contenant du SYBR Green I (pour les acides nucléiques doubles brins) ou du SYBR Green II (pour détecter aussi les acides nucléiques simples brins). Le SYBR Green présente l'avantage d'une moindre toxicité et d'une sensibilité plus élevée permettant de détecter des quantités plus faibles d'acides nucléiques.
Limites de résolution
L'électrophorèse en gel d'agarose permet théoriquement la séparation de fragments d'ADN d'une taille allant de 50 paires de bases à plusieurs millions. Cependant, elle est généralement utilisée pour la séparation de fragment d'une taille allant de 100 pb à 20 kb. La durée moyenne de migration est d'une heure.
Les petits fragments d'acides nucléiques sont mieux séparés par électrophorèse sur gel de polyacrylamide. Les fragments de tailles importantes sont plus difficiles à séparer. En général, l'utilisation de gel d'agarose à forte concentration (3 à 4%) est alors nécessaire pour des fragments inférieurs à 150 pb, car elle permet une meilleure séparation et résolution des différentes bandes en fonction de leur différence de taille. Le principal désavantage est le temps de migration, qui peut aller jusqu'à plusieurs jours. Pour pallier ces problèmes, il est avantageux d'effectuer une électrophorèse en champ pulsé ou bien une électrophorèse en champ inversé.