Historique du concept de molécule - Définition
La liste des auteurs de cet article est disponible ici.
XVIIe siècle
La plus ancienne théorie sur les formes et la connectivité des atomes a été celle proposée par Leucippe, Démocrite et Épicure qui associaient la solidité d'un matériau à la forme que prenaient les atomes qui le composent. Selon cette théorie, les atomes de fer sont solides et durs et composés de crochets qui les relient entre eux pour former le métal. Les atomes d'eau, par contre, sont lisses et glissants ; les atomes de sels, en raison de leur goût, sont pointus et aigus ; et les atomes d'air sont légers et tourbillonnants, infiltrant tous les autres matériaux. Le principal partisan de cette théorie était Démocrite. En utilisant des analogies à partir de nos perceptions, il fournit une image de l'atome où ceux-ci sont distingués les uns des autres par leur forme, leur taille, et leurs arrangements relatifs. De plus, la liaison était expliquée via des liens matériels où les atomes possédaient des points d'attache : certains ayant des crochets et d'autres des creux.
Curieusement, la théorie atomique fut abandonnée pendant près de deux millénaires au profit de la théorie des quatre éléments et plus tard des théories alchimiques. Toutefois, le XVIIe siècle voit ressurgir la théorie atomique à travers les travaux de Descartes, Gassendi et Newton, qui utilisent les anciennes théories atomiques grecques pour expliquer comment les particules ultimes de la matière se lient entre elles. Descartes imagine que les atomes sont attachés entre eux par des crochets microscopiques. Par la suite, l'une des théories moléculaires les plus anciennes sera proposée par le célèbre naturaliste français René Descartes qui croyait que les atomes sont pourvus de crochets, et d'autres de creux. Il soutenait que deux atomes se combinent quand le crochet de l'un se fait piéger dans le creux de l'autre, tel que montré ci-dessous :
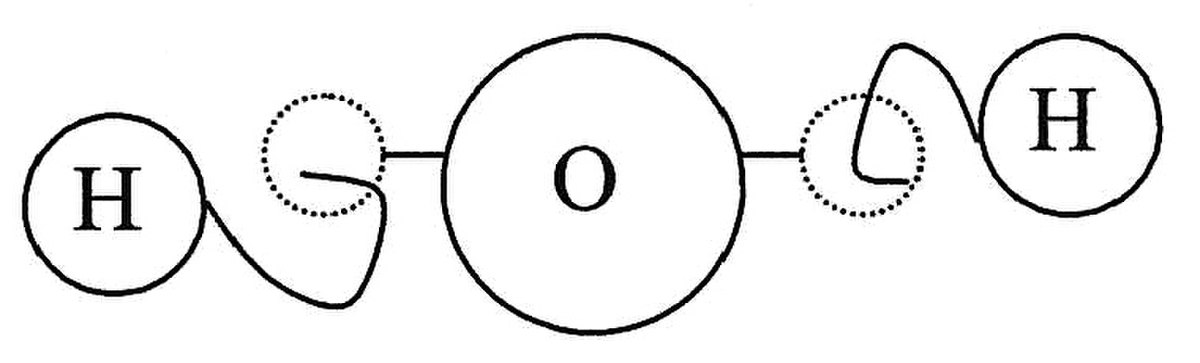
Vers le milieu des années 1770, les théories impliquant des particules comportant des crochets physiques étaient considérées comme de la « chimie cartésienne ». De manière similaire à Descartes, Gassendi, qui avait alors écrit un livre sur la vie d'Épicure, pense que la taille et la forme des atomes qui se déplacent dans le vide doit rendre compte des propriétés de la matière. La chaleur est due à des atomes petits et ronds ; le froid, à des atomes pyramidaux avec des coins pointus, ce qui prend en compte la sensation de picotement lors de grand froid ; tandis que les solides tiennent ensemble par des crochets entrelacés.
Newton, connaissant les diverses théories d'attachement d'atome alors à la mode, c'est-à-dire les « atomes crochus », les « atomes collés » (des corps au repos), et la théorie des « liaisons par mise en commun », croit plutôt, comme indiqué dans le célèbre « Principe 31 » de son Opticks de 1704, que les particules s'attirent les unes les autres par une certaine force, qui « en contact immédiat est extrêmement forte, à de petites distances effectue les opérations chimiques, et à longue distance ne crée pas d'effet sensible sur les particules. »
Cependant, et de façon plus concrète, le concept des agrégats ou des unités d'atomes collés, c'est-à-dire « molécules », trouve ses origines dans l'hypothèse de Robert Boyle en 1661, dans son célèbre traité The Sceptical Chymist : la matière se compose de clusters de particles et les changements chimiques résultent du réarrangement du cluster. Boyle affirme que les éléments de base de la matière sont composés de particules de diverses sortes et tailles, appelées « corpuscules », qui sont capables de s'arranger en groupes.
En 1680, en employant la théorie corpusculaire comme base, le chimiste français Nicolas Lémery stipule que l'acidité de n'importe quelle substance trouve ses origines dans ses particules aiguës, tandis que les alcalis sont dotés de pores de diverses tailles. Une molécule, selon ce point de vue, est composée de corpuscules unis par une fermeture géométrique entre des points et des pores.