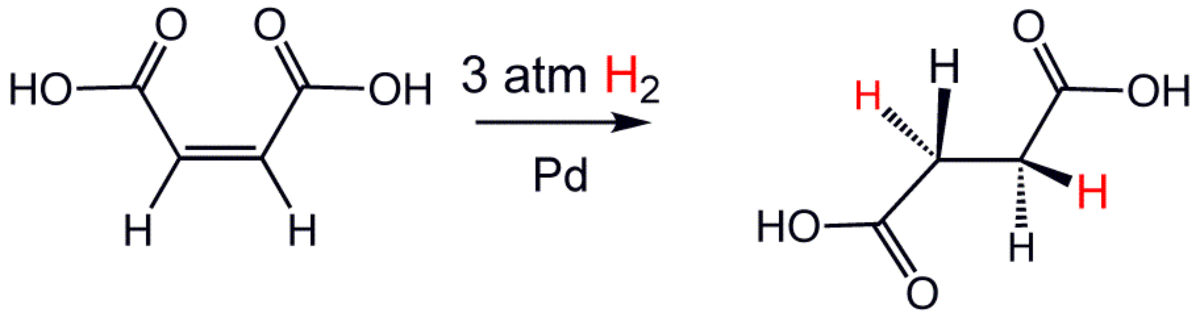Hydrogénation - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
L'hydrogénation est une réaction chimique qui consiste en l'addition d'une molécule de dihydrogène (H2). Cette réaction est habituellement employée pour réduire ou saturer des composés organiques. Cette réaction nécessite en général une catalyse, les réactions sans catalyse nécessitant de très hautes températures.
On appelle la réaction inverse de l'hydrogénation la déshydrogénation. Les réactions ou des liaisons sont brisées tandis que de l'hydrogène est additionné sont appelées hydrogénolyses (cette réaction pouvait s'appliquer aux liasons carbone-carbone comme aux liaisons carbone-hétéroatome — O, N, X). L'hydrogénation diffère de la protonation ou de l'addition d'hydrure: dans l'hydrogénation, le produit ou les produits ont la même charge que les réactifs.
La réaction d'hydrogénation utilise généralement du dihydrogène gazeux comme source d'hydrogène. Cependant cette réaction étant relativement importante, de nombreuses techniques ont été développées, certaines d'entre elles utilisant d'autres sources que H2; on appelle ce type de réaction hydrogénation par transfert.
La réaction d'hydrogénation est utile dans de nombreux domaines, en particulier en pétrochimie (transformation d'alcènes en alcanes) et dans l'industrie agroalimentaire (hydrogénation de graisses insaturées en graisses saturées).
Histoire
La réaction d'hydrogénation a été décrite pour la première fois en 1897 par le chimiste français Paul Sabatier qui est considéré comme le père des procédés d'hydrogénation. En 1897, il a découvert que l'introduction de traces de nickel comme catalyseur facilitaient l'addition de dihydrogène sur des hydrocarbures gazeux, procédé connu à présent sous le nom de procédé de Sabatier. Ses nombreux travaux sur l'hydrogénation des composés organiques lui ont valu entre autres l'attribution du prix Nobel de chimie en 1912, conjointement avec un autre chimiste français, Victor Grignard.
L'hydrogénation a alors été utilisée dans de nombreux procédés:
- Wilhelm Normann a obtenu en 1902 en Allemagne, et en 1903 au Royaume-Uni un brevet sur l'hydrogénation des huiles liquides, ce qui allait devenir un nouvelle industrie à l'échelle mondiale.
- Le procédé Haber-Bosch, procédé d'une grande importance commerciale, décrit pour la première fois en 1905, utilise l'hydrogénation du diazote.
- Dans le procédé Fischer-Tropsch, décrit en 1922, le monoxyde de carbone obtenu facilement à partir du charbon est hydrogéné en combustibles liquides.
En 1922, Voorhees et Adams ont décrit un appareil permettant d'effectuer des hydrogénations à pression élevée. L'agitateur de Parr (Parr shaker), le premier appreil permettant l'hydrogénation à hautes température et pression, basé sur les travaux de Voorhees et Adams, a été commercialisé en 1926 et reste d'usage courant. En 1938, Otto Roelen a décrit le procédé oxo (hydroformylation) qui utilise à la fois l'addition d'hydrogène et de monoxyde de carbone sur les alcènes pour produire des aldéhydes. Puisque ce procédé implique le formation de liaison C-C, il est, ainsi que ses nombreuses déclinaisons (voir carbonylation), toujours d'une grande actualité. Les années 1960 ont vu le développement des catalyseurs homogènes, avec par exemple le catalyseur de Wilkinson. Dans les années 1980, l'hydrogénation asymétrique de Noyori représente l'une des premières applications de l'hydrogénation en synthèse asymétrique, une branche en pleine croissance permettant la production de produits chimiques spécifiques (chimie fine). En 2004, le H-Cube, un appareil sophistiqué à hydrogénation, est développé.