P53 - Définition
La liste des auteurs de cet article est disponible ici.
La fonction de p53 dans une cellule normale
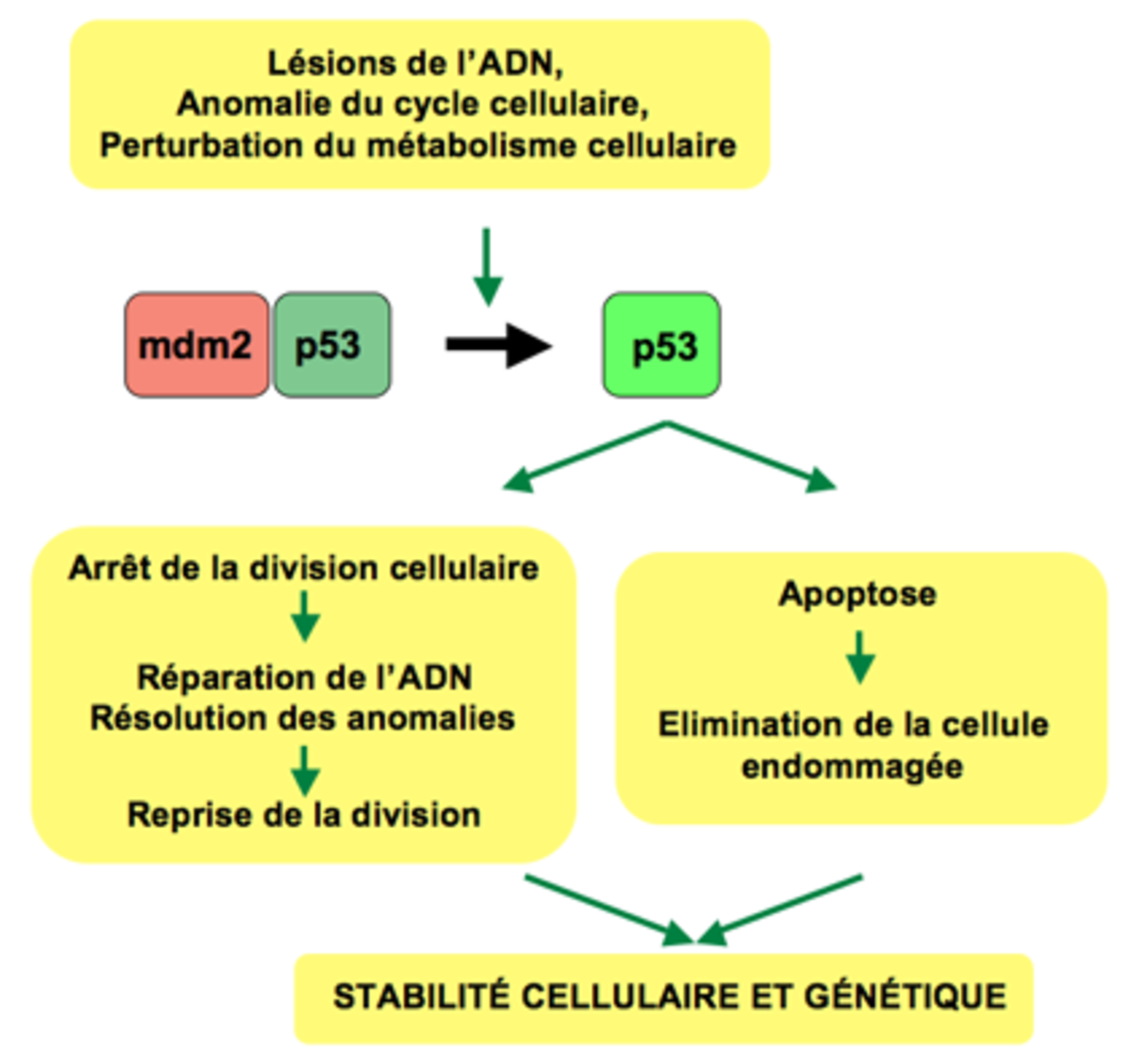
La fonction première de la protéine p53 est d’agir en tant que facteur de transcription. Elle fonctionne en se fixant de manière spécifique sur les régions régulatrices de gènes dont elle contrôle l’expression. Dans une cellule normale, en l’absence de tout stress, il n’y a que très peu de p53 car celle-ci n’est pas nécessaire au fonctionnement de la cellule. Cette absence de p53 est due à l'enzyme mdm2, une E3 ubiquitine ligase, qui en se fixant sur p53, induit sa destruction. Lorsque la cellule se trouve en situation de stress, l’association entre p53 et mdm2 est abolie ce qui conduit à une augmentation de la quantité de p53 dans la cellule. Cette première phase est nommée « phase d’activation ». De nombreux types de stress sont capables d’activer la p53 comme les lésions de l’ADN, les défauts de division ou de métabolisme cellulaire.
Dans un second temps, la p53 va subir de nombreuses modifications post traductionnelles qui vont permettre d’activer sa fonction de facteur de transcription. Cette phase est nommée « phase de modification »
Dans un troisième temps (phase de réponse), la p53 activera la transcription d’un grand nombre de gènes. L’ensemble de ce programme pourra conduire à deux résultats, soit l’arrêt du cycle cellulaire soit l’apoptose. L’arrêt du cycle cellulaire permet à la cellule de stimuler ses mécanismes de réparation (dont certains sont directement activés par p53). Lorsque la réparation est effectuée, le taux de p53 retourne à la normale et le cycle cellulaire reprend. Dans d’autre cas, quand les dommages que la cellule a subi ne peuvent pas être réparés, la cellule décide de se suicider par un mécanisme biologique connu sous le nom d’apoptose ce qui conduit donc à l’élimination de la cellule endommagée. Ce mécanisme apoptotique est directement contrôlé par p53. Un des rôles de p53 est d'activer, entre autres, l'expression du gène de Bax. Bax, en se dimérisant, va perforer la membrane mitochondriale et permettre au cytochrome C de sortir. La sortie de cytochrome C de la mitochondrie vers le cytosol est un évènement central dans le processus apoptotique intrinsèque. À l’heure actuelle, on ne sait pas pourquoi ni comment certaines cellules s'orientent vers un programme apoptotique ou un arrêt du cycle cellulaire.
La protéine p53 est donc une molécule indispensable au maintien de l’intégrité de la cellule et de ses composants. C’est pour cette raison qu’elle est généralement nommée « gardienne du génome »
Si on élimine artificiellement la p53, la cellule ne peut plus répondre à l’ensemble des stress et aucun arrêt du cycle cellulaire ou apoptose n’est observé.
Modification du gène p53 dans les cancers
Altérations du gène p53 dans les cancers humains
Près de 50% des cancers humains ont une p53 mutée qui a perdu ses capacités anti prolifératives et apoptotiques. Dans les cancers du col de l’utérus (toujours associées à un virus de type HPV), la situation est particulière. Une protéine virale (protéine E6) se fixe spécifiquement sur p53 et la détruit ce qui conduit à la même situation qu’une tumeur ayant une p53 mutée.
Pourquoi le gène p53 est-il fréquemment altéré dans les cancers humains
La protéine p53 est l'agent le plus important de la protection de la cellule contre la cancérisation. Les cellules chez qui son gène est intact seront donc moins enclines à la cancérisation. Ceci permet d'affirmer que "l'inactivation de p53 est un préalable indispensable à la cancérisation" bien que le phénomène se passe en réalité dans l'autre sens : si p53 est muté, la cellule devient bien plus à risque de transformation maligne. Ceci explique qu'on observe des mutations de p53 dans plus de la moitié des cancers humains.
Comment le gène p53 est-il altéré ?
Les études d’épidémiologie moléculaire ont démontré de manière formelle que les altérations du gène p53 étaient dues à l’exposition à des carcinogènes dans les cas de cancers bronchiques (tabac), cancer de la peau (rayons UV) ou cancer du foie (alcool) dans les pays en voie de développement (exposition à l’aflatoxine B1). Dans les autres cancers, leurs origines sont plus incertaines.
Relation entre perte de la fonction de p53 et les propriétés de la tumeur
Le but de la thérapie anti cancéreuse est de tuer les cellules malignes en nuisant le moins possible aux cellules normales. L’apoptose est l’une des voies qui est induite par la radiothérapie ou la chimiothérapie. Malheureusement, ce programme apoptotique est contrôlé par la p53. On observe généralement que les tumeurs exprimant une p53 altérée ont une moins bonne réponse à la thérapie par rapport à une tumeur exprimant une p53 mutée. Néanmoins, il existe des cas particuliers chez lesquelles on observe l'inverse. À l'heure actuelle, le statut du gène p53 n'est pas utilisé comme marqueur en routine clinique.