Batterie au plomb - Définition
| Batteries specifications | |
|---|---|
| Énergie/Poids | 160 Wh/Kg |
| Énergie/Volume | 270 Wh/L |
| Rendement charge-décharge | 99.9 % |
| Énergie/Prix publique | Wh/€ |
| Auto-décharge | 5% à 10% /mois |
| Durée de vie | min. 4 à 5 ans |
| Nombre de cycle de charge | 1200 cycles |
| Tension nominale | 3.6 ou 3.7 V |
Une batterie au plomb est un ensemble d'accumulateurs au plomb-acide disposés en série, réunis dans un même boîtier.
Ces systèmes de stockage de l'électricité sont largement utilisés dans l'industrie et, dans l'équipement des véhicules automobiles.
Historique
L'accumulateur au plomb a été inventé en 1859 par le français Gaston Planté. Ce fut le premier accumulateur rechargeable.
À l'origine, les accumulateurs étaient situés dans des cuves en verre. Par la suite, on a systématisé l'emploi des cuves en plastique.
De nos jours, les batteries sans entretien se généralisent : cosses traitées antisulfatage, plaques au plomb-calcium, supprimant le besoin de refaire le niveau de liquide, et donc permettant le scellement.
Caractéristiques techniques
Une batterie au plomb se caractérise essentiellement par :
- La tension nominale qui dépend du nombre d'éléments, la tension nominale U est égale au nombre d'éléments multiplié par 2,1 V
- La capacité de stockage, notée C, qui s'exprime en ampères pendant 1 heure : l'énergie électrique théorique correspondante est C x U, exprimée en Wh. (Notons que la valeur en Ah n'a de valeur que pour une tension ou plutôt une plage de tension. Généralement on considère qu'un accumulateur au plomb est déchargé lorsqu'il atteint la tension de 1.8 V, donc une batterie de 6 éléments ou 12 V est déchargée, lorsqu'elle atteint la tension de 10.8 V).
- Le courant maximal qu'elle peut fournir pendant quelques instants, ou courant de crête en ampères CCA.
Ces valeurs maximales sont donnés par le constructeur pour une batterie neuve et chargée à 100%, elles varient sensiblement en fonction de l'état de charge, se dégradent en fonction du temps ainsi, que de l'usage qui est fait de la batterie.
- Les réactions électrochimiques aux électrodes sont les suivantes :
Anode (oxydation):
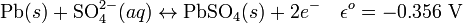
Cathode (réduction):
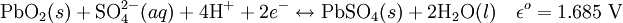
Performances
La batterie au plomb est celle qui a le plus mauvais rapport masse/énergie (35 Wh/kg) après la batterie Nickel-Fer. Cependant, elle est capable de fournir une grande intensité, utile pour le démarrage électrique des moteurs à combustion interne.
Utilisation
Cette batterie sert à alimenter les composants électriques des véhicules à moteur à explosion, particulièrement le démarreur électrique, alimentée par une dynamo ou un alternateur.
Historiquement, les batteries de voitures ou de motocyclettes faisaient le plus souvent 6 volts (3 éléments). À l'époque moderne, les batteries à 12 volts (6 éléments) sont généralisées sur les voitures et motocyclettes, alors que les véhicules lourds ou militaires utilisent le 24 volts.
Les batteries au plomb servent aussi à alimenter toutes sortes d'engins électriques. Les voitures électriques ont toujours échoué du fait du mauvais rapport masse/énergie des batteries.
Ces batteries peuvent servir à stocker de l'énergie produite par intermittence, comme l'énergie solaire ou éolienne.
Causes de dégradation
Les principales causes de dégradation des batteries sont :
- la sulfatation
- la décharge complète
- le cyclage
- l'oxydation des électrodes
- Oxydation des bornes
La sulfatation
Une tension aux bornes de la batterie inférieure à 12,2 V (pour une tension nominale de 12 V) enclenche le processus de sulfatation interne des plaques. Un maintien prolongé à une tension inférieure ou égale à cette valeur engendre une détérioration irréversible de la batterie réduisant sa puissance de démarrage. Une batterie sulfatée soumise à une recharge reprend sa tension nominale mais sa puissance au démarrage est amputée. Le processus de sulfatation est interrompu dès que la batterie est remise en charge.
Exemple : Une batterie sulfatée de 1000 CCA à l'état neuf, mais contrôlée à 12 V et avec une puissance de 500 CCA, reprendra après recharge une tension supérieure ou égale à 12,6 V mais la puissance mesurée de 500 CCA évoluera peu.
Une batterie dans cet état ne permettra pas plusieurs démarrages consécutifs d'un véhicule automobile et pourra provoquer, par exemple, une panne immobilisante dès les premiers froids. De manière générale, il faut recharger sa batterie régulièrement pour la faire durer.
Désulfatation
Il existe un moyen d'inverser le processus de sulfatation d'une batterie. Cela consiste en l'envoi d'impulsions électriques à la fréquence de résonance de la batterie (entre 2 et 6 MHz). Durant ce processus, les ions de souffre entrent en collision avec les plaques, ce qui a pour effet de dissoudre le sulfate de plomb qui les recouvre. [1]
La décharge complète
Pour un véhicule automobile, la décharge complète de la batterie intervient généralement par une faible consommation pendant une durée prolongée (ex plafonniers) ou par une consommation importante (ex feux de croisement, ventilation), moteur à l'arrêt. La tension est alors très faible aux bornes de la batterie, inférieure à 10 volts pour une batterie dont la tension nominale est de 12 V.
Une batterie de démarrage se décharge également toute seule dans le temps. Elle risque donc d'atteindre sa décharge complète si elle n'est pas rechargée régulièrement. Pour cette raison, il existe les chargeurs " d'entretien " de batteries.
Les batteries en état de décharge complète doivent être rechargées dans un délai maximum de 48 heures : au-delà, les dommages sont irréversibles (sauf par désulfatation).
Cyclage
Les constructeurs de batteries indiquent leur durée de vie sous la forme d'un nombre de cycles normalisés de décharge/recharge.
À l'issue d'un certain temps de fonctionnement dépendant du nombre et de l'amplitude des cycles, la batterie est usée : l'électrolyte présente un aspect noirâtre.
Exemple : L'utilisation répétée d'un hayon élévateur moteur à l'arrêt accélère l'usure de la batterie par cyclage.
Oxydation des électrodes
L'oxydation est une cause de dysfonctionnement des batteries. Lorsque le niveau d'électrolyte est trop bas, les plaques entrent au contact de l'air et s'oxydent. La puissance au démarrage est amputée, même si le niveau d'électrolyte est complété. Le manque d'électrolyte peut venir d'une utilisation intensive(ex: équipements auxiliaires...), d'une température extérieure importante (supérieure ou égale à 30 °C) ou d'une tension de charge trop élevée.
Oxydation des bornes
Il arrive qu'une batterie dont les cosses ne sont pas assez serrées, ou qui ne sert que très peu, voie ses bornes s'oxyder, ce qui empêchera le courant de passer et donc, à terme, une décharge complète.


















































