Glucide - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
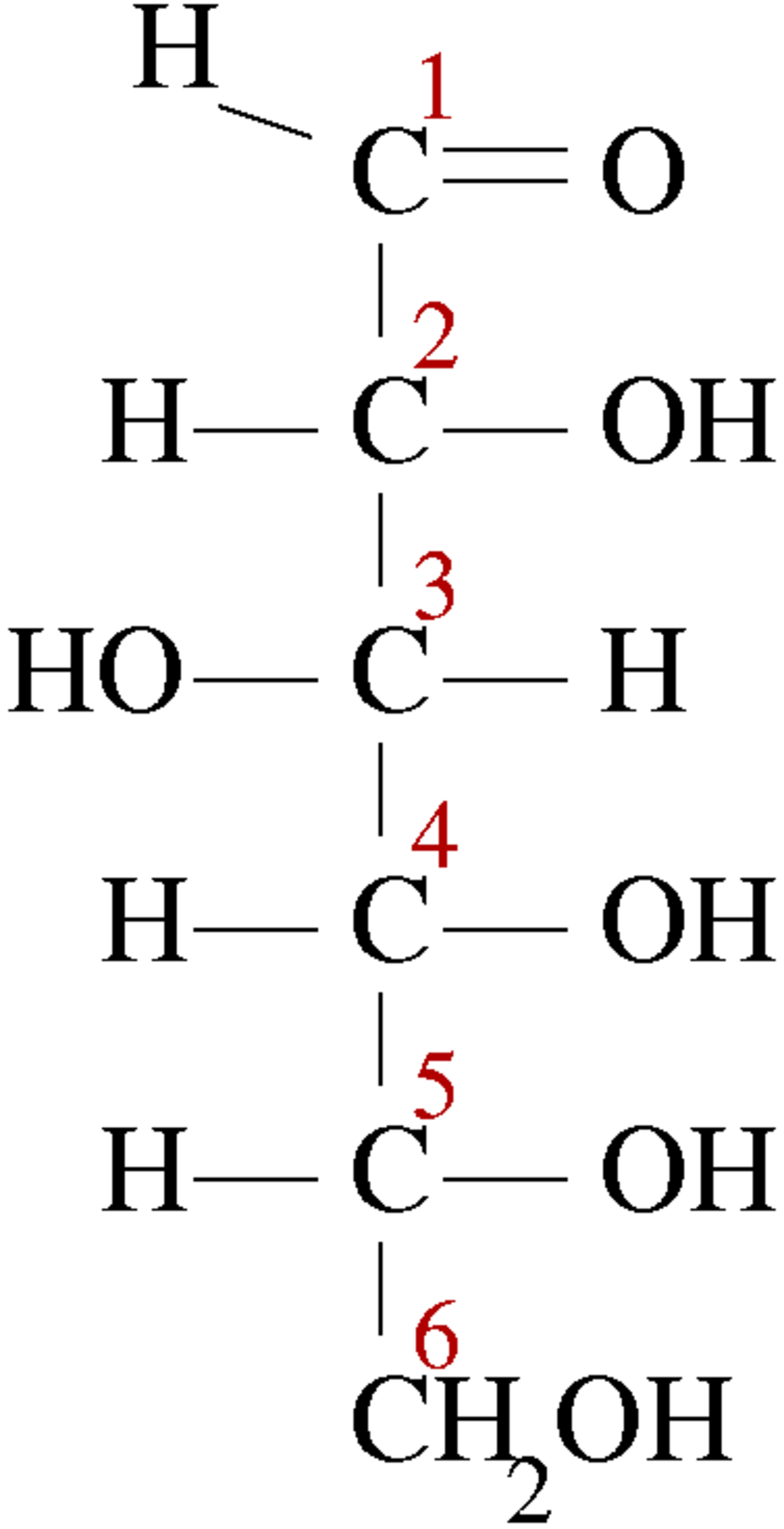
Les glucides sont une classe de molécules organiques contenant un groupement carbonyl (aldéhyde ou cétone) et plusieurs groupements hydroxyle (-OH) . Les glucides étaient historiquement appelés hydrates de carbone. Leur formule chimique est basée sur le modèle Cn(H2O)p (d'où l'appellation historique). Cependant, ce modèle n'est pas valable pour tous les glucides, qui contiennent, pour certains, des atomes d'azote ou de phosphore (par exemple).
Ils font partie, avec les protéines et les lipides, des constituants essentiels des êtres vivants et de leur nutrition, car ils sont un des principaux intermédiaires biologiques de stockage et de consommation d'énergie. Chez les organismes autotrophes, comme les plantes, les sucres sont convertis en amidon pour le stockage. Chez les organismes hétérotrophes, comme les animaux, ils sont stockés sous formes de glycogène puis utilisés comme source d'énergie dans les réactions métaboliques, leur oxydation lors de la digestion des glucides apportant environ 17 kJ/g selon l'étude dans la bombe calorimétrique.
Catégorie
Les glucides sont habituellement répartis entre oses (monosaccharides tel que le glucose, le galactose ou le fructose) et osides, qui sont des polymères d'oses (polysaccharides). Les disaccharides (diholosides), tel que le saccharose ou le lactose, font partie de cette dernière catégorie. Mais seules les monosaccharides et les disaccharides ont un pouvoir sucrant. Les polysaccharides, comme l'amidon, sont insipides.
- Les oses (sucres simples) sont des molécules simples, non hydrolysables, formant des cristaux.
- Les osides (sucres complexes), hydrolysables sont des polymères d'oses liés par une liaison osidique :
- Les holosides sont des polymères exclusivement d'oses ;
- Les oligoholosides (oligosides) ont un indice de polymérisation inférieur à 10 ;
- Les polyholosides (polyosides) ont un indice de polymérisation supérieur à 10 (exemple : amylose, amylopectine, cellulose, glycogène).
- Les homopolyosides sont les glucides dont l'hydrolyse donne un seul type d'oses.
- Les hétéropolyosides sont les glucides dont l'hydrolyse ne donne pas qu'un seul type d'oses.
- Les hétérosides sont des polymères d'oses et de molécule(s) non glucidique l'aglycone :
- Les O-hétérosides où une fonction alcool (-OH) de l'aglycone participe à la liaison osidique;
- Les N-hétérosides où une fonction amine (-N=) de l'aglycone participe à la liaison osidique;
- Les S-hétérosides où une fonction thiol (-SH) de l'aglycone participe à la liaison osidique.
- Les holosides sont des polymères exclusivement d'oses ;
Propriétés chimiques
Propriétés réductrices
Les oses simples et les diholosides ayant un carbone hémiacétalique libre sont réducteurs de par leur fonction aldéhyde. La fonction aldéhyde est oxydée en fonction acide carboxylique. L'une des fonctions alcool primaire peut être oxydée en fonction acide carboxylique.
Les diholosides non réducteurs sont ceux dont aucun carbone hémiacétalique n'est libre, il est mis en jeu dans la liaison osidique.
- Réduction des ions métalliques
Réduction de l'ion cuivre II (Cu2+) en oxyde de cuivre I (Cu2O) (liqueur de Fehling). Cette propriété est utilisée dans la méthode de Bertrand pour le dosage des glucides.
- Réduction de composés organiques
Par exemple le 3,5-dinitrosalicylate (DNS) est réduit en 3-amino-5-nitrosalicylate, composé rouge brun permettant de doser les oses réducteurs par colorimétrie.
- Oxydation par voie enzymatique
En présence de dioxygène, la glucose oxydase oxyde le glucose en gluconolactone (puis acide gluconique) avec libération d'eau oxygénée. L'oxydation du carbone 1 (portant la fonction pseudo-aldéhydique) conduit au gluconolactone (non réducteur), celle en C6 conduit à l'acide glucuronique (réducteur). Une double oxydation en C1 et C6 conduit à l'acide glucosaccharidique (non réducteur). La glucose oxydase est utilisée pour mesurer la glycémie.
Hydrolyse de la liaison osidique
Hydrolyse chimique
L'hydrolyse chimique n'est pas spécifique, elle conduit à la plus petite sous-unité des glucides : les oses. Elle est réalisée en présence d'acide chlorhydrique
Hydrolyse enzymatique
L'hydrolyse enzymatique, contrairement à l'hydrolyse chimique, est spécifique. Ces enzymes sont des hydrolases.
- la β-glucosidase hydrolyse les liaisons osidiques mettant en jeu un glucose dont l'-OH hémiacétalique est en position β ;
- L'α-amylase rompt les liaisons osidiques à l'intérieur de la chaîne d'amylose ;
- La β-amylase hydrolyse les liaisons osidiques à partir des extrémités.