Glucose - Définition
La liste des auteurs de cet article est disponible ici.
Pouvoir sucrant
Le glucose a un faible pouvoir sucrant, de 0,70 à 0,75. En comparaison, celui du saccharose vaut 1 (par convention), le glucose est donc bien moins utilisé que ce dernier dans l'industrie alimentaire pour ses qualités organoleptiques. Il est plutôt utilisé en tant qu'agent de charge (sous forme cristalline monohydratée ou de sirop concentré) et est également présent dans les sirops de glucose et de glucose-fructose. Il est aussi ajouté dans certains produits que l'on trouve sur le marché (par exemple dans le dextro energy). Le glucose (dextrose) est utilisé dans l'industrie alimentaire pour son pouvoir anti-oxydant (conservateur donc).
Métabolisme
Contrairement au saccharose, il est directement assimilable par l'organisme, dont c'est un carburant essentiel, notamment pour le cerveau. L'énergie contenue dans une mole de glucose est de 2 871 kJ (ou 686 kcal, 1 cal = 4,18 J).
Les nouvelles techniques d'imagerie médicale permettent une appréciation de la topologie du métabolisme cellulaire. En tomographie par émission de positons, on utilise pour cela un composé dérivé du glucose : le fluorodésoxyglucose ou 18F-FDG qui, du point de vue structural, est suffisamment proche du glucose pour être capté par les cellules mais inutilisable dans leurs métabolismes. Ce composé étant radioactif, les rayonnements émis sont alors captés et, suivant leur répartition dans l'organisme, produisent une image d'hyperfixation dans les lieux de haut métabolisme (par exemple : le cerveau, le cœur, les tumeurs...).
Propriétés chimiques
Cristallisation
Les solutions concentrées de glucose ( > 30% ) cristallisent spontanément à température ambiante. Le glucose sous forme cristalline, est vendu sous l'appellation de "dextrose" pour éviter toute confusion avec les sirops de glucose, et se trouve sous forme monohydratée. Les solutions de dextrose sont produites industriellement par une hydrolyse totale d'empois d'amidon. L'hydrolyse est réalisée à chaud par des systèmes enzymatiques combinant alpha et bêta amylases.
Réactions en milieu acide
En présence d'un acide dilué, le glucose ne réagit pas, c'est un ose, il n'est pas hydrolysable.
En milieu acide concentré et chaud, le glucose subit une déshydratation et condensation avec l'α-naphtol (réactif de Molisch), ce qui le colore. Le glucose se cristallise.
En milieu alcalin
L'ammoniaque accélère la mutarotation.
En présence de soude diluée, il y a formation d'un ènediol (instable) qui produit (figure 5) :
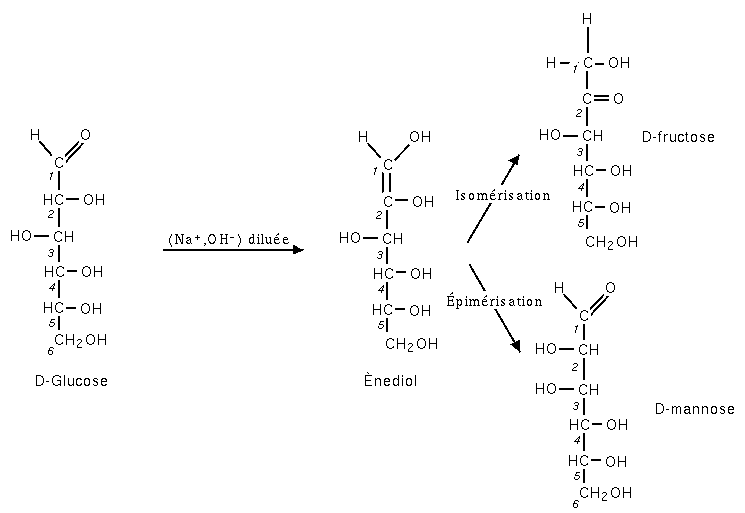
En milieu basique concentré, le glucose est oxydé. Ces réactions sont complexes et non stoechiométriques (dosage par la méthode de Bertrand).
Propriétés de la fonction aldéhyde
- La réduction du glucose donne du sorbitol ;
- L'oxydation du glucose donne de l'acide gluconique.
Le glucose est un glucide réducteur, il est capable de réduire
- les ions métalliques :
- L'ion mercure II (réaction de Baudoin-Lewin) : Hg2+ + Glc → Hg + produits d'oxydation ;
- L'ion fer III (réaction d'Hagedorn-Jensen) : Fe3+ + Glc → Fe2+ + produits d'oxydation ;
- L'ion argent (réaction de Tollens) : Ag+ + Glc → Ag + produits d'oxydation ;
- L'ion cuivre II (réaction de Fehling) : Cu2+ + Glc → Cu2O + produits d'oxydation.
- Les composés organiques :
- le 3,5-dinitrosalicylate (composé jaune) est réduit en 3-amino-5-nitrosalicylate (composé rouge) permet le dosage du glucose et des autres glucides réducteurs.
La réaction de Fehling est utilisée dans la méthode de Bertrand. Le précipité d'oxyde de cuivre II est redissous puis dosé.
Propriétés de la fonction alcool primaire
Cette fonction est portée par le carbone n° 6, son oxydation donne de l'acide glucuronique si la fonction aldéhyde a été protégée en la combinant à autre chose.
L'acide nitrique à chaud oxyde les deux fonctions terminales du glucose des carbone 1 et 6 et forme un acide aldarique (diacide carboxylique) : l'acide glucarique.


















































