Acide butanoïque - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Acide butanoïque | |||
|---|---|---|---|
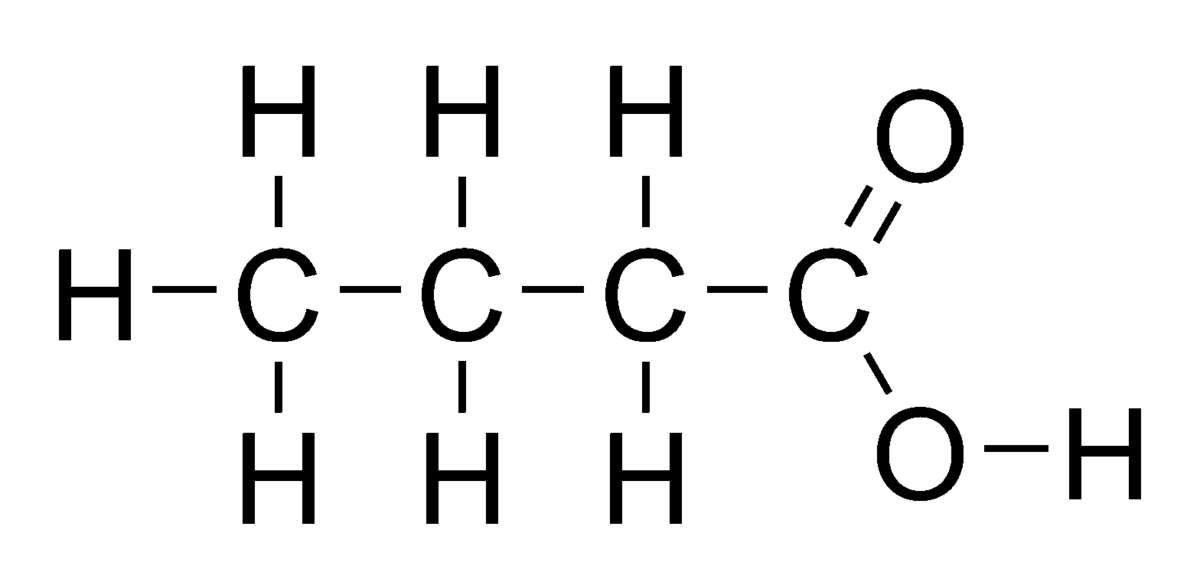
| |||
| Général | |||
| Nom IUPAC | |||
| Synonymes | acide butyrique acide éthylacétique acide n-butanoïque | ||
| No CAS | |||
| No EINECS | |||
| DrugBank | |||
| PubChem | |||
| FEMA | |||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore, huileux, d'odeur caractéristique. | ||
| Propriétés chimiques | |||
| Formule brute | C4H8O2 | ||
| Masse molaire | 88,1051 ± 0,0044 g·mol-1 | ||
| Diamètre moléculaire | 0,560 nm | ||
| Propriétés physiques | |||
| T° fusion | -7,9 °C | ||
| T° ébullition | 164 °C | ||
| Solubilité | dans l'eau : miscible, Miscible avec l'éthanol, l'éther | ||
| Masse volumique | 0,959 g·ml-1 à 20 °C 0,964 g·ml-1 à 25 °C | ||
| T° d’auto-inflammation | 452 °C | ||
| Point d’éclair | 72 °C (coupelle fermée) | ||
| Limites d’explosivité dans l’air | 2–10 %vol | ||
| Pression de vapeur saturante | à 20 °C : 57 Pa | ||
| Point critique | 52,7 bar, 354,85 °C | ||
| Thermochimie | |||
| Cp | |||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 10,17 ± 0,05 eV (gaz) | ||
| Propriétés optiques | |||
| Indice de réfraction | 1,398 à 20 ° (éclairage : sodium) | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 34, | |||
| Phrases S : (1/2), 26, 36, 45, | |||
| | |||
| |||
| | |||
|
2 3 0 | |||
| | |||
| Produit non classifié | |||
| | |||

Danger | |||
| Écotoxicologie | |||
| DL | 8,79 g·kg-1 (rats, oral) | ||
| LogP | 0,79 | ||
| | |||
L'acide butanoïque, aussi appelé acide butyrique du grec βουτυρος (beurre), est un acide carboxylique saturé de formule CH3CH2CH2-COOH
On le trouve par exemple dans le beurre rance, le parmesan, et le contenu gastrique, où il dégage une odeur forte et désagréable. L'acide butyrique peut être détecté par des mammifères avec un bon odorat, comme les chiens, dans des concentrations de 10 ppb, alors que les humains ne peuvent le détecter que dans des concentrations supérieures à 10 ppm.
Dans des conditions normales de température et de pression, l'acide butanoïque est un liquide légèrement huileux qui se solidifie à -8 °C et dont le point d'ébullition est de 164 °C. Il est facilement soluble dans l'eau, l'éthanol, et l'éther et se dissocie de son solvant par l'addition de chlorure de calcium. Le dichromate de potassium et l'acide sulfurique l'oxydent en dioxyde de carbone et en acide acétique, alors que le permanganate de potassium alcalin l'oxyde seulement en dioxyde de carbone. De plus, il a pour isomère de constitution l'acide 2-méthylpropanoïque, qui lui doit son deuxième nom d'acide isobutyrique.
C'est aussi un acide gras à courte chaîne présent dans les huiles végétales et les graisses animales. Le glycéride (ester de glycérol) de l'acide butyrique compose 3 % à 4 % du beurre. Quand le beurre rancit, les glycérides sont hydrolysés, libérant ainsi de l'acide butyrique à l'odeur désagréable. L'acide butyrique normal ou l'acide butyrique de fermentation est également trouvé comme ester hexylique dans l'huile de Heracleum giganteum et comme ester octylique dans celle du panais Pastinaca sativa ; il est aussi présent dans la transpiration.
Il est habituellement produit par la fermentation du sucre ou de l'amidon, provoquée par l'addition de fromage en décomposition, auquel on ajoute du carbonate de calcium pour neutraliser les acides formés dans le processus. La fermentation butyrique de l'amidon est facilitée par l'addition directe de Bacillus subtilis.
Divers esters sont obtenus à partir de l'acide butyrique. Ceux à faible masse molaire, comme le méthylbutyrate, ont la plupart du temps des arômes plaisants. Ils sont ainsi utilisés comme additifs alimentaires ou dans les parfums.
Sa formule brute est la même que celle du formiate de propyle.



















































