Pile électrique - Définition
La liste des auteurs de cet article est disponible ici.
Classification
La plupart des cellules voltaïques sont limitées à 1,5 V, en raison des potentiels électrochimiques de leurs composants. Les cellules à base de lithium peuvent fournir des tensions plus élevées (jusqu'à 4,5 volts).
Par capacité
La capacité d'une pile est souvent exprimée en ampères-heures (1 Ah = 3 600 coulombs). Si une pile peut fournir un ampère (1 A) de courant pendant une heure, elle a une capacité de 1 Ah. Si elle peut fournir 1 A pendant 100 heures ou 2 A pendant 50 heures, etc., sa capacité est de 100 Ah. Elle est directement dépendante de la quantité d'électrolyte et d'électrode dans la pile.
Par format
Le format des piles électriques est normalisé par la Commission électrotechnique internationale (CEI) et par l'American National Standards Institute (ANSI). Bien que la norme CEI soit devenue un standard, un certain nombre d'appellations propres aux fabricants de piles subsiste.
Par technologie
Depuis décembre 1998, les piles au mercure sont interdites en Europe (directive 98/101/CE) et aux États-Unis pour des problèmes environnementaux. Il existe donc trois grandes technologies de piles grand public :
- Pile alcaline 1,5 V ( ⊝ Zn / Zn(OH)42- / K+ + OH- / MnO(OH) / MnO2 / C ⊕ ).
- Pile saline carbone-zinc 1,5 V. Pour des appareils à faibles besoins ( ⊝ Zn / Zn2+ / NH4+ + Cl- / MnO(OH) / MnO2 / C ⊕ ).
- Pile au lithium 1,5 V (appelée aussi L91), capable de maintenir très longtemps la tension électrique. C'est ce type de pile qu'on retrouve le plus fréquemment dans un téléphone mobile.
- On trouve aussi des piles à l'oxyde d'argent (certaines piles boutons pour montres) ou des piles zinc-air (utilisées notamment dans les prothèses auditives) (⊝ Zn / ZnO // Ag2O / Ag / C ⊕).
Histoire
Il existe des objets archéologiques trouvés comme en 1936 ressemblant à des piles. C'est par exemple le cas de la pile électrique de Bagdad qui est datée entre 250 av. J.-C. et 250 mais elles pourraient être encore plus anciennes et expliqueraient le placage si parfait de nombreux bijoux antiques si légers. Elles auraient fonctionné aux jus de fruits voire au sulfate de cuivre, des expérimentations modernes ont validé la faisabilité des deux modèles. Il n'existe aucun lien historique entre ces objets et le développement des piles contemporaines d'autant que l'usage de celles-ci serait le placage de métaux précieux ce qui expliquerait son usage mineur, confidentiel voire associé à un usage de faussaire (voir Archimède et la couronne du roi Hiéron).
En 1786, Luigi Galvani observe que les muscles d'une cuisse de grenouille se contractent quand elle est mise en contact avec des métaux, de la même manière que lorsqu'on la branche sur une machine électrostatique. Il découvre que la réaction est plus forte quand il utilise un instrument composé de deux métaux différents.
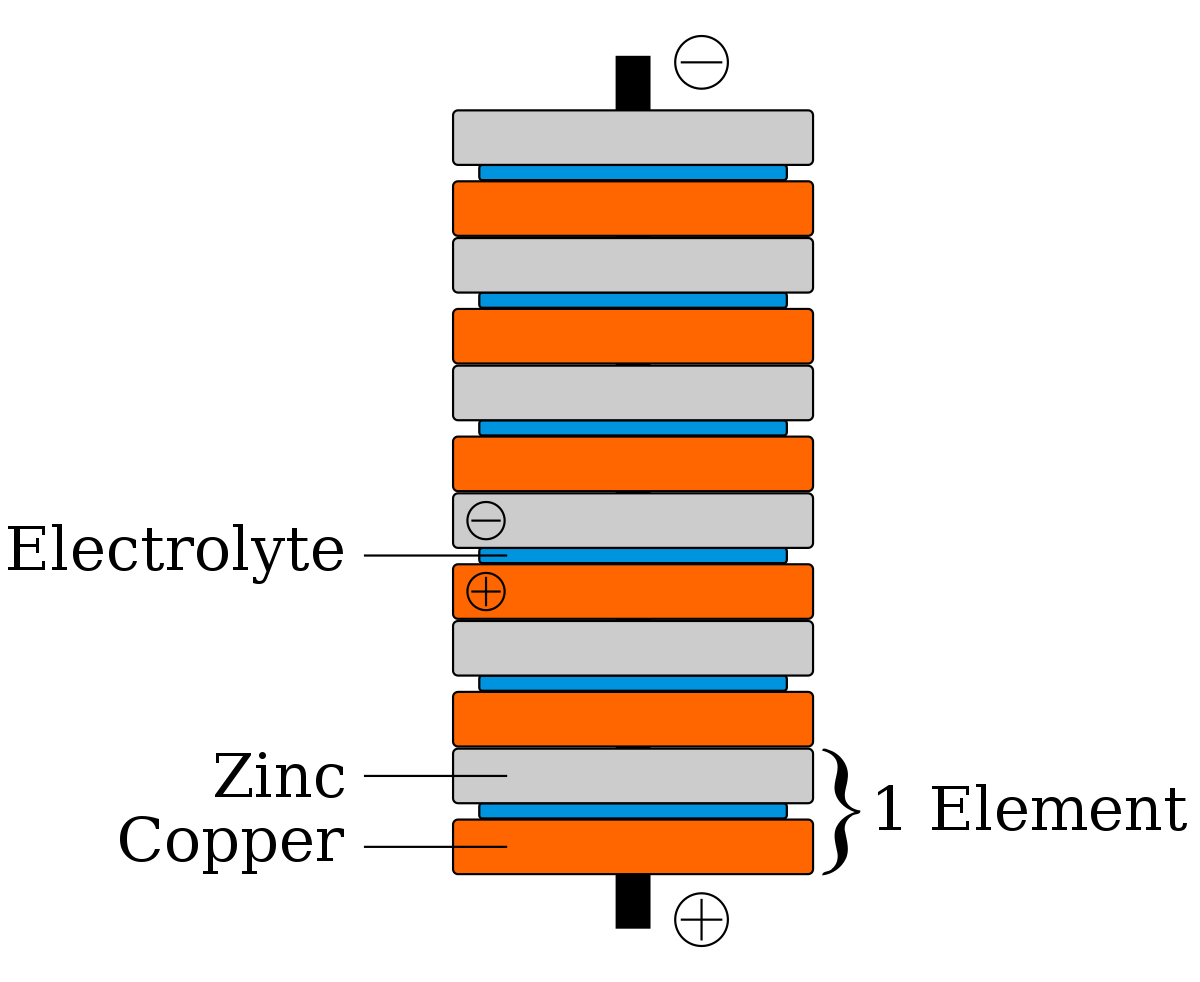
En opposition avec les travaux de Galvani (électricité d'origine animale), Alessandro Volta invente la première pile à colonne le 17 mars 1800 ; ces premiers systèmes étaient constitués d'un « empilement » de disques de deux métaux différents séparés par des disques de feutre, imbibés d'acide, d'où le nom de l'invention. La pression de la colonne sur les disques du bas provoque un assèchement des cylindres de feutre qui finissent par ne plus remplir leur office. Volta invente donc rapidement la pile à couronne, constituée d'empilements plus petits montés en série.
Quelques mois après l'invention de Volta, deux chimistes britanniques, William Nicholson (1753-1815) et Anthony Carlisle (1768-1840) utilisent la pile de Volta pour réaliser la première électrolyse artificielle (électrolyse de l'eau) le 2 mai 1800.
Dès 1802, William Cruickshank crée la pile à auge en disposant verticalement les lames de zinc et de cuivre dans un bac à parois isolantes rempli d'eau acidulée. Elle est beaucoup plus simple à produire que la pile de Volta.

La pile voltaïque, première pile électrique, inventée par Alessandro Volta, est composée d'une alternance de disques de cuivre et de zinc séparés par un tissu imbibé de saumure | 
Une pile d'époque |
Piles polarisables
Entre 1813 et 1815, William Hyde Wollaston développe la pile Wollaston dans laquelle l'électrode de cuivre entoure l'électrode de zinc. Cela permet de doubler la surface de l'électrode et de prolonger le fonctionnement de la pile. Ces premières piles souffrent en effet d'un défaut de fonctionnement : la polarisation.
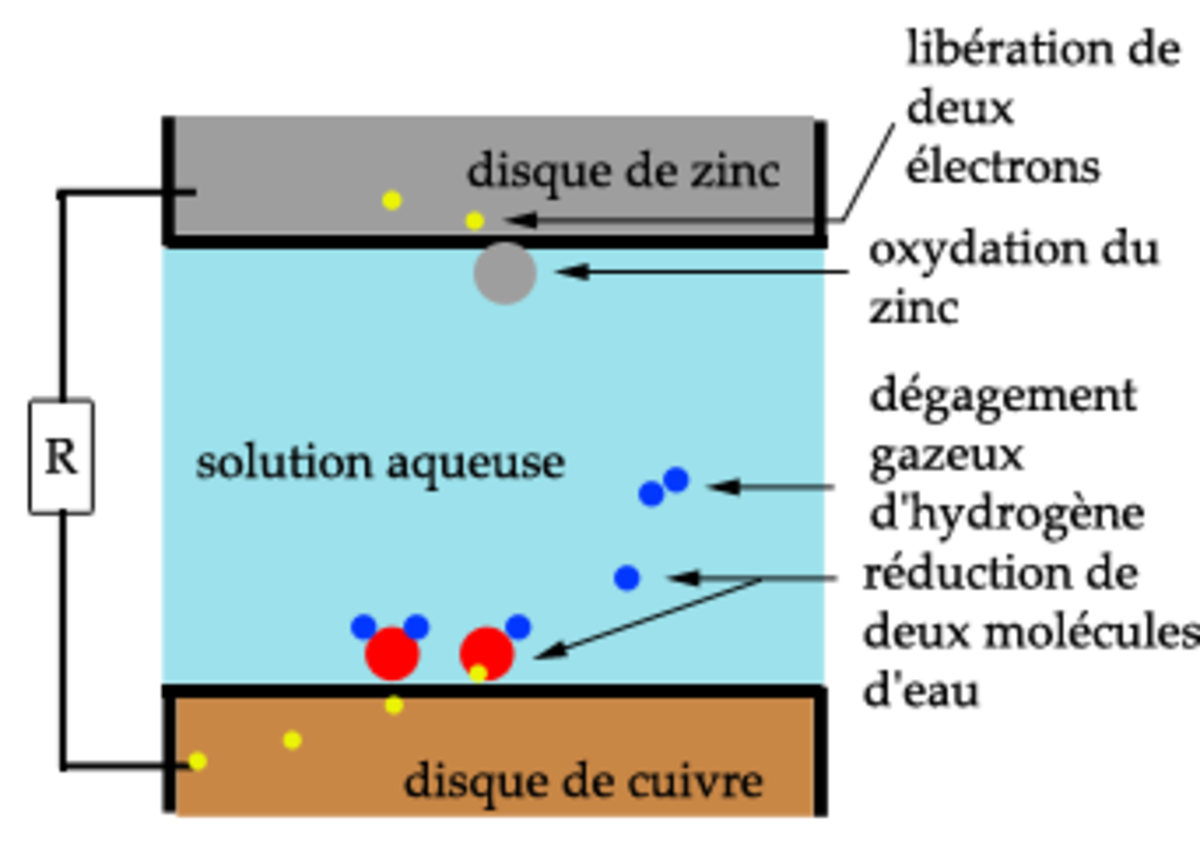
La réaction d'oxydo-réduction provoque une accumulation de sous-produits qui perturbe le fonctionnement de la pile. Dans ces piles zinc-cuivre c'est la réduction de l'acide de l'électrolyte qui produit un dégagement de bulles hydrogène sur le cuivre qui empêche le passage du courant. Au bout d'un certain temps, il est donc nécessaire de nettoyer la pile de ces dépôts pour qu'elle continue de fonctionner.
En 1813, Napoléon fournit à l' École polytechnique une pile voltaïque de 600 couples de cuivre et de zinc, occupant 54 mètres carrés de surface. Humphry Davy fait construire une pile Cruickshank constituée de 200 auges et de 2 000 couples à l'institut Royal de Londres. Avec ces piles monumentales il était possible d'obtenir des intensités de 10 ampères, soit des puissances de l'ordre de la dizaine de kW.
Piles impolarisables
Dans les piles impolarisables, les produits de la réaction d'oxydo-réduction utilisée n'altèrent pas les propriétés électrochimiques de l'ensemble.
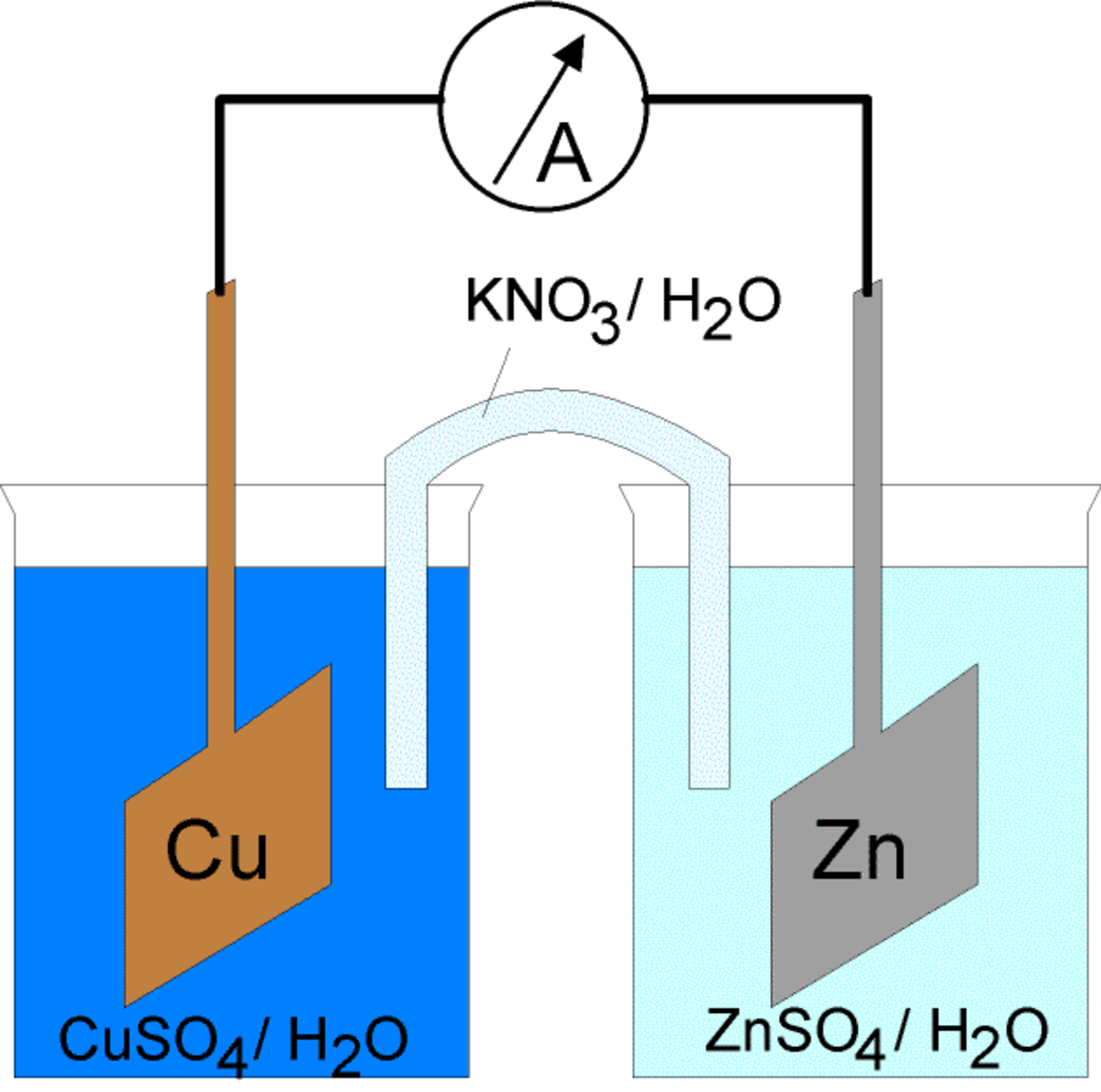
En 1829, Antoine Becquerel crée la première pile à deux liquides séparés en enfermant la plaque de zinc en solution acide dans un gros intestin de bœuf, qui la sépare de l'électrode de cuivre placée dans un bain de sulfate de cuivre. La génération d'hydrogène est remplacée par une accumulation de cuivre sur les parois de la cathode.
Le principe est amélioré en 1836 par John Frederic Daniell qui remplace l'intestin de bœuf par un vase en terre poreuse. La pile Daniell est la première à offrir une source durable d'énergie. Le principe de la pile Daniell sera amélioré : plusieurs améliorations technologiques suivront, comme les piles Callaud qui seront utilisées par les compagnies de téléphone dans les années 1860.
Johann Christian Poggendorff invente en 1842 la pile à bichromate : elle dégage de l'oxygène qui se recombine avec l’hydrogène responsable de la polarisation. Créée en 1850, la pile Grenet est une pile à un seul liquide, avec des électrodes en charbon et en zinc amalgamé (plongé dans le mercure) dans un électrolyte d'acide sulfurique et de bichromate de potasse. Quand la pile n'était pas utilisée, il était nécessaire de retirer l'électrode en zinc de la solution pour la préserver. Diverses améliorations (pile Trouvé, pile Chardin, pile Voisin et Dronier…) vont suivre pour isoler cette électrode.
Ces piles bouteilles seront utilisées jusqu'au début du XXe siècle : la puissance et la tension élevée des piles au bichromate ont été longtemps appréciées au laboratoire. Elles ont été peu utilisées comme pile domestique à cause de la toxicité du bichromate et des problèmes d'entretien de l'électrode.
Piles à dépolarisation
Les piles à dépolarisation utilisent un réducteur pour éliminer les produits de réaction qui se forment à la cathode.
La première pile à dépolarisation est inventée en 1838 par William Robert Grove. Il remplace le cuivre par du platine et utilise de l'acide nitrique (nommé acide azotique à cette époque). Il obtient une pile puissante mais chère car le platine est un métal rare. En 1843 Robert Wilhelm Bunsen remplace le platine par du charbon ce qui réduit notablement les coûts. Mais la dépolarisation nitrique entraîne un dégagement de vapeurs toxiques qui rend l'emploi de ces piles malcommode.
En 1867, Georges Leclanché crée la première pile à dépolarisant solide : elle contient du dioxyde de manganèse. La pile Leclanché est moins puissante que la pile bouteille mais ne nécessite aucun entretien (elle « ne s'use que si l'on s'en sert » comme dira la publicité de la pile Wonder). En 1888, Carl Gassner invente la pile sèche en gélifiant la solution de chlorure d'ammonium avec de l'agar-agar. Avec quelques améliorations, cette pile sèche est toujours utilisée au XXIe siècle.
Samuel Ruben et Philipp Rogers Mallory créent la pile au mercure pendant la Seconde Guerre mondiale. La première pile alcaline grand public sera conçue par Lewis Urry en 1959 pour Union Carbide.
En 1970, les premières piles au lithium, qui permettent de remplacer le zinc par un métal plus réducteur, sont mises au point. Elles sont commercialisées en 1977.
Des piles ont été utilisées comme références pour définir une norme de tension avant d'être détrônée par une mesure basée sur l'effet Josephson : la pile Daniell, puis la cellule de Clark inventée en 1872 par Josiah Latimer Clark a été employée jusqu'en 1905, puis elle a été remplacée par la cellule de Weston jusqu'en 1972.
Piles de concentration
Il existe aussi ce qu'on appelle des piles de concentration qui sont des dispositifs électrochimiques comme les piles (deux solutions et un pont salin) qui tirent leur énergie de la différence de concentration d'un soluté d'une solution à l'autre. Les solutions et les anodes sont toutes de même type. C'est une méthode simple pour fabriquer de l'électricité. Ce modèle de pile intervient surtout dans l'industrie métallurgique au niveau de la galvanisation et de l'étude de la corrosion.