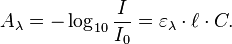Spectroscopie ultraviolet-visible - Définition
La liste des auteurs de cet article est disponible ici.
Loi de Beer-Lambert
La technique d'analyse est souvent utilisée dans un mode quantitatif pour déterminer la concentration d'une entité chimique en solution, en utilisant la Loi de Beer-Lambert :
où I/I0 est la transmittance de la solution (sans unité), A est l’absorbance ou densité optique à une longueur d'onde λ (sans unité), ελ est le coefficient d'extinction molaire (en l.mol−1·cm−1). Il dépend de la longueur d'onde, de la nature chimique de l'entité et de la température. Cette constante représente une propriété moléculaire fondamentale dans un solvant donné, à une température et une pression donnée et s'exprime en M-1.cm ou parfois en AU/M.cm. ℓ est la longueur du trajet optique dans la solution traversée, elle correspond à l'épaisseur de la cuve utilisée (en cm). C est la concentration molaire de la solution (en mol.l−1). Dans le cas d'un gaz, C peut être exprimée comme un volume inverse (unités de longueur réciproque au cube, cm−3).
Cette équation est très utile pour la chimie analytique. En effet, si ℓ et ελ sont connus, la concentration d'une substance peut être déduite de la quantité de lumière transmise par elle.
L'absorbance et le coefficient d'extinction ελ sont parfois définis avec les logarithmes naturels au lieu des logarithmes décimaux.
La loi de Beer-Lambert, utile pour caractériser de nombreux composés, ne doit pas être considérée comme une relation universelle pour caractériser la concentration et l'absorption de toutes les substances. Une relation polynomiale du deuxième ordre entre le coefficient d'extinction et la concentration est parfois considérée pour les très grandes molécules complexes, par exemple les colorants organiques comme l'orange de xylénol ou le rouge neutre.
Spectre ultraviolet-visible
Un spectre ultraviolet-visible est pour l'essentiel un graphe d'une absorbance en fonction de la longueur d'onde dans les régions visible et ultraviolette. Un tel spectre peut parfois être produit directement par des spectrophotomètres sophistiqués, ou les données peuvent être collectées une longueur d'onde à la fois par des instruments plus simples. La longueur d'onde est parfois représentée par le symbole λ. De manière similaire, pour une substance donnée, un graphe standard du coefficient d'extinction (ε) en fonction de la longueur d'onde (λ) peut être tracé. Les lois de Woodward-Fieser sont un ensemble d'observations empiriques pouvant être utilisées afin de prédire λmax, la longueur d'onde de l'absorption UV-visible la plus importante, pour les composés organiques conjugués comme les diènes et cétones.
Les longueurs d'ondes des pics d'absorption peuvent être corrélées avec les types de liaisons dans une molécule donnée et sont valides pour déterminer les groupes fonctionnels dans une molécule. L'absorption UV-visible n'est pas, cependant, un test spécifique pour tout composé. La nature du solvant, le pH de la solution, la température, les hautes concentrations électrolytiques, et la présence de substances interférentes peuvent influencer les spectres d'absorption des composés, comme le peuvent les variations dans la largeur des fentes (largeur de bande effective) du spectrophotomètre.
Qualité des mesures, vérification des spectrophotomètres(à compléter)
Réalisations et applications particulières (à compléter)
Miniaturisation (appareillage et échantillons)(à compléter) Utilisation des fibres optiques pour mesures "in-situ", évanescence...(à compléter) Combinaisons de techniques: spectrophotométrie et: chromatographie liquide, chromatographie gazeuse, biomonitor... (à compléter) Analyse des gaz(à compléter)
Analyses multicomposants