Urée - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Urée | |
|---|---|
| |
| Général | |
| Nom IUPAC | |
| Synonymes | carbamide, carbonyl diamide, isourée |
| No CAS | |
| No EINECS | |
| DrugBank | |
| PubChem | |
| No E | E927b |
| SMILES | |
| InChI | |
| Apparence | cristaux blancs, d'odeur caractéristique |
| Propriétés chimiques | |
| Formule brute | CH4N2O |
| Masse molaire | 60,0553 ± 0,0018 g·mol-1 |
| Propriétés physiques | |
| T° fusion | 132,7 à 135 °C |
| T° ébullition | décomposition |
| Solubilité | 670 g·l-1 (eau, 0 °C), 1 080 g·l-1 (eau, 20 °C), |
| Masse volumique | 0,750 g·cm-3 (liquide) 1,335 g·cm-3 (solide) |
| Thermochimie | |
| S0 | 104 J/mol.K |
| ΔH0 | -333 kJ/mol |
| Cp | 93 J/mol.K (à 298 K) |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 9,7 eV (gaz) |
| Précautions | |
| | |
| Produit non contrôlé | |
| Écotoxicologie | |
| LogP | -3,00 à -1,54 |
| | |
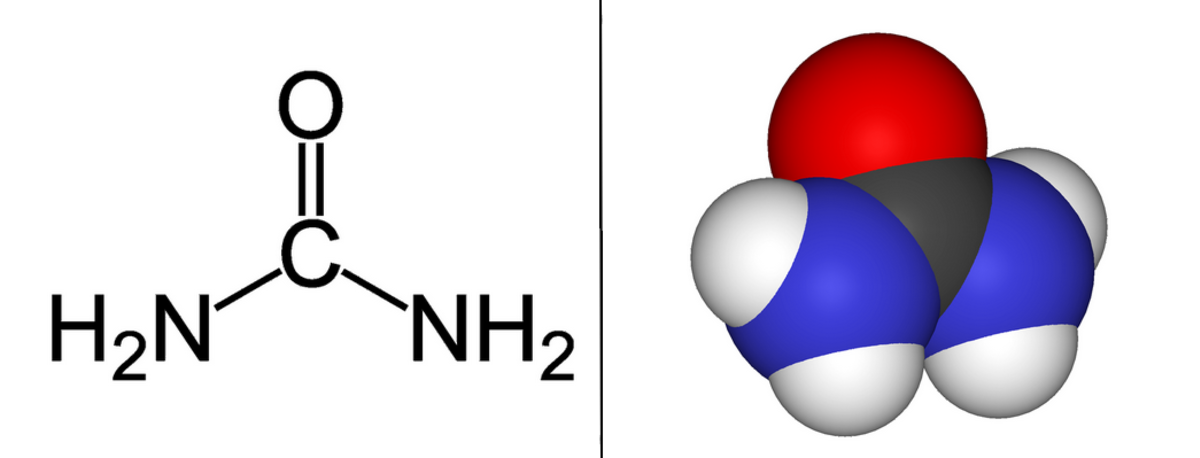
L'urée ou carbamide (DCI) est un composé organique de formule chimique CO(NH2)2. C'est aussi le nom de la famille des dérivés de l'urée de formule générale (R1,R2)N-CO-N(R3,R4).
Histoire
L'urée naturelle est découverte en 1773 par Hilaire Rouelle. Formée dans le foie lors du cycle de l'urée, à partir de l'ammoniac qui provient de la dégradation de trois acides aminés : l’arginine, la citrulline et l’ornithine, l’urée naturelle est éliminée par l'urine.
En 1828, après avoir maîtrisé la synthèse de l'acide cyanique, Wöhler réalise celle de l'urée. En traitant l’acide cyanique par l'ammoniaque, il obtient du cyanate d'ammonium qui s'isomérise en urée :
Cette expérience provoque une révolution. Elle apporte en effet la preuve qu’il est possible de synthétiser un composé organique en dehors d'un organisme vivant. Elle marque ainsi le début de la chimie organique et annonce la fin de la théorie de la force vitale.
Synthèse industrielle
L'urée est fabriquée industriellement à partir d'ammoniac (NH3) et de dioxyde de carbone (CO2).
La réaction de synthèse se fait sous forte pression (de 140 à 160 bar) selon les procédés et sous des températures de 160 °C à 180 °C. Elle a lieu en deux temps :
- 1. synthèse du carbamate d'ammonium ( NH2COONH4 ), produit intermédiaire stable uniquement sous haute pression :
- CO2 + 2 NH3 ⇔ NH2COONH4 ;
- 2. décomposition du carbamate d'ammonium en urée et eau :
- NH2COONH4 → CO(NH2)2 + H2O.
Les réactions ne sont pas totales, mais sont à l'équilibre à la sortie du réacteur sous pression, la solution réactionelle contient de l'urée, de l'eau, du CO2 et de l'ammoniac. Le procédé chimique consiste ensuite en la séparation des produits de réaction par stripping et distillation.
D'une part, l'ammoniac et le CO2 sont entièrement recyclés dans le réacteur de synthèse, d'autre part, la solution d'urée est concentrée par évaporation de l'eau, l'urée est ensuite concentré en une solution à plus de 99 %, restant liquide au-dessus de 132 °C. L'eau distillée est récupérée pour la production de vapeur.
La solution concentrée d'urée est ensuite cristallisée en refroidissant sous forme de granulés adaptés à l'usage agricole.
Les plus grosses unités industrielles actuelles produisent 3 600 tonnes d'urée par jour.
La production mondiale annuelle d'urée atteint 120 millions de tonnes.
Les principaux pays producteurs sont la Chine, l'Inde, le Koweit, l'Arabie Saoudite, le Qatar, l'Égypte, les États-Unis et la Russie.
En France, une unité de production est implantée à Gonfreville-l'Orcher (banlieue industrielle du Havre), usine exploitée en commun par le groupe Total et la société Yara pour une production d'environ 950 t/j.