Carbone - Définition
La liste des auteurs de cet article est disponible ici.
Isotopes
Le carbone possède deux isotopes stables dans la nature, 12C (98,89 %) et 13C (1,11 %). Le premier, 12C, a été choisi comme nucléide de référence unique pour la masse atomique 12, après plusieurs propositions (anciennement l’hydrogène, puis conjointement avec l’oxygène pour les chimistes). La masse atomique du carbone reste cependant légèrement supérieure à 12 à cause de la prévalence de ses autres isotopes.
Le radioisotope 14C a une période de 5 730 ans et est couramment utilisé pour la datation d'objets archéologiques jusqu'à 50 000 ans. Il ne sera d'aucune utilité pour les archéologues de demain intéressés par les trésors de la civilisation actuelle car les explosions thermonucléaires réalisées dans l'atmosphère à partir des années 1960 ont créé des excès considérables.
Le radioisotope 11C a une période de 20 minutes. Cette courte période et la relative facilité de substituer un atome de 11C à un atome de carbone 12C (stable) en font un isotope utilisé en médecine nucléaire, notamment en tomographie à émission de positron. Les radiotraceurs les plus utilisés à ce jour sont le 11C-Raclopride qui se fixe préférentiellement sur les récepteurs dopaminergiques D2, et le 11C-Acétate utilisé en imagerie cardiaque.
Composés courants du carbone
Petites molécule et ions
La forme la plus connue du carbone est le dioxyde de carbone CO, qui est l'un des composants minoritaires de l'atmosphère terrestre (arrivant en quatrième position avec environ 0,03 % mais loin derrière l'azote 78,11 %, l'oxygène 20,953 % et l'argon 0,934 %) produit et métabolisé par les êtres vivants, l'industrie, les voitures et les centrales thermiques. Sa concentration a augmenté de près de 40% depuis le début de l'ère industrielle. Il possède deux modes de vibration qui absorbent la lumière infrarouge, ce qui en fait un gaz à effet de serre. Le CO est un composé majoritaire de l'atmosphère d'autres planètes comme Vénus.
Dans l'eau, il forme de très faibles quantités d'acide carbonique, HCO, qui produit des ions carbonate CO2- ou hydrogénocarbonate (bicarbonate) HCO-. Beaucoup de minéraux sont des carbonates, notamment les diverses formes de calcaire (calcite, craie, marbre…). On connaît les propriétés thérapeutiques du bicarbonate de sodium NaHCO.
Chimie organique
La chimie du carbone est essentiellement covalente. Le carbone est à la base d'une multitude de composés pouvant contenir un grand nombre d'atomes, en association avec l'hydrogène, l'oxygène, l'azote, les halogènes, le phosphore, le soufre, et les métaux, par liaisons simples, doubles ou triples. L'étude et la synthèse de ces composés constitue la chimie organique.
Dangers du carbone et de ses composés
Le (di)sulfure de carbone CS, quoique de structure similaire au dioxyde de carbone, est un liquide hautement toxique utilisé comme solvant (vulcanisation du caoutchouc).
Les autres oxydes de carbone sont le monoxyde de carbone CO, et le suboxyde de carbone CO, moins commun. Le monoxyde de carbone est un gaz incolore et inodore, formé par combustion incomplète des composés organiques ou du carbone pur (charbon). Le monoxyde de carbone se lie plus fortement que l'oxygène, à l'hémoglobine sanguine pour former de la carboxyhémoglobine, un composé stable. Le résultat de cette réaction est l'empoisonnement des molécules d'hémoglobine, ce qui peut être mortel (voir l'entrée en question).
L'ion cyanure CN- a un comportement chimique similaire à un ion halogénure. Les sels contenant l'ion cyanure sont hautement toxiques. Le cyanogène, un gaz de composition (CN) est également proche des halogènes.
Avec les métaux, le carbone forme des carbures C4- ou des acétylures C2-. Quoi qu'il arrive, avec une électronégativité de 2,5, le carbone préfère former des liaisons covalentes. Quelques carbures sont des treillis covalents, comme le carbure de silicium, SiC, qui ressemble au diamant, et est d'ailleurs utilisé pour la taille de ceux-ci.
Les nanotechnologies permettent de produire des molécules particulières, dont les fullerènes, et des nanofils ou nanotubes difficiles à filtrer dans l'air et qui peuvent passer à travers les muqueuses et percer les enveloppes cellulaires. Certains craignent des effets différés comme on en a trouvé pour l'amiante.
Hydrocarbures
On appelle « hydrocarbures » les molécules associant carbone et hydrogène. On classe les hydrocarbures en trois familles :
- les alcanes, où le carbone forme des liaisons sp3 (« simples ») : méthane CH, éthane CH, etc. ;
- les alcènes, où au moins un carbone forme des liaisons (« double ») (carbones sp2) : éthène (éthylène) CH, propène CH, etc. ;
- les alcynes, où au moins un carbone forme des liaisons (« triple ») (carbones sp) : éthyne (acétylène) CH, propyne CH, etc.
Suivant le nombre d'atomes de carbone, on fait précéder le suffixe -ane, -ène ou -yne :
- méth-
- éth-
- prop-
- but-
- pent-
- hex-
- hept-
- oct-
- non-
- déc-
La rotation est libre autour des liaisons simples carbone-carbone. En revanche, les liaisons doubles ou triples sont rigides : la liaison double est planaire, les angles de liaison autour des atomes de carbone sont 120°. Cela conduit à la formation de diastéréomères, c'est-à-dire de composés ayant la même formule chimique mais une disposition différente des atomes dans l'espace. La liaison triple est linéaire.
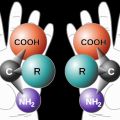
En outre, le carbone sp3 peut former des composés chiraux (du grec ̔η χείρ, la main). Le cas le plus simple est un composé possédant 4 substituants différents autour d'un atome de carbone. Suivant la disposition dans l'espace de ces substituants, on obtient deux molécules qui sont différentes : elles ne sont pas superposables, il s'agit d'une paire d'énantiomères. Les énantiomères sont l'image l'un de l'autre dans un miroir (comme nos deux mains).
Dans les hydrocarbures aromatiques, les atomes de carbone forment des cycles ou noyaux stabilisés par des liaisons π délocalisées.