Physique du solide - Définition
La liste des auteurs de cet article est disponible ici.
Historique
Les connaissances empiriques sur les solides et leurs propriétés sont très anciennes et jalonnent l'histoire de l'humanité. L'apparition de la métallurgie, environ 4 000 ans avant J.-C., marque les premières réussites dans le travail des métaux : l'homme apprend ainsi à travailler le cuivre, le bronze, le fer puis une liste de plus en plus étendue de métaux et d'alliages. Cependant, les connaissances acquises sont très empiriques, transmises de maître à compagnon, et ne sont pas reliées sur une science commune. Le premier, Agricola applique les méthodes scientifiques de la Renaissance et présente une synthèse des techniques de son époque dans son ouvrage De Re Metallica, paru en 1556.
Avant même l'arrivée des méthodes de cristallographie modernes, l'observation et la classification des cristaux amène les scientifiques à comprendre leur structure interne. En 1611, Johannes Kepler fait ainsi l'hypothèse que la symétrie hexagonale des cristaux de neige est due à un arrangement hexagonal de particules d'eau sphériques. Au XVIIIe siècle, Haüy établi que les faces des cristaux peuvent être repérées par un ensemble de trois nombres entiers appelés indice de Miller, ce qui l'amène à associer à chaque cristal un réseau de petits volumes de matière qu'il nommait « molécules intégrantes » et qui correspondent actuellement à la notion de maille élémentaire. Ces notions seront progressivement formalisées au cours du XIXe siècle. Entre autres, Bravais et Schoenflies montrent à l'aide de la théorie des groupes que les cristaux peuvent être catégorisés en 32 groupes ponctuels de symétrie et en 230 groupes d'espace.
Le XIXe siècle voit également l'apparition de nouveaux domaines scientifiques, tels que la mécanique des milieux continus, l'électromagnétisme ou la thermodynamique, qui attribuent des propriétés macroscopiques mesurables à la matière – module d'Young, susceptibilité optique, conductivité électrique et thermique, etc. Bien que ces grandeurs macroscopiques permettent une description phénoménologique satisfaisante des solides, elles ne permettent pas de comprendre leur origine profonde.
Les progrès scientifiques réalisés au tournant du XIXe siècle permettent de soulever un coin du voile. Les rayons X découverts en 1895 vont ainsi permettre à Max von Laue de réaliser la première expérience de diffraction des rayons X sur un cristal en 1912. Cette technique – complétée par la diffraction d'électrons et de neutrons – va être appliquée par la suite de manière systématique à la détermination de la structure cristalline et des distances interatomiques dans les solides. Parallèlement, en 1900 Drude développe un modèle quasi-classique de la conduction des métaux en supposant ceux-ci remplis d'un gaz d'électrons libres auxquels il applique la physique statistique de Ludwig Boltzmann. Au cours du XXe siècle, découvertes, nouveaux outils et modèles se succèdent à un rythme accéléré : étude des propriétés des solides aux basses températures, introduction de la mécanique quantique, apparition du microscope électronique...
Petite typologie des solides
Il existe une grande diversité de solides différents dans la nature, et quels que soient les ensembles que l'on essaie de définir, on trouvera toujours un solide pouvant être classé dans deux ensembles différents. Ci-dessous, nous exposons différentes typologies établies selon les critères suivant : l'existence ou l'absence d'un ordre cristallin, la nature de la liaison entre les atomes ou encore la facilité avec laquelle les solides conduisent le courant électrique.
Verres et cristaux
- Rayer ou supprimer les éléments lorsqu'ils sont intégrés au texte
Un cristal représente une classe importante de solides dans lesquels les mêmes atomes se répètent périodiquement dans les trois dimensions de l'espace. Le cristal forme alors un réseau qui reste identique à lui-même lors de la translation par un vecteur
où
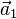
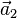
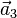
- cristal et ordre à toutes les portées, monocristal et cristallites
- matière amorphe et ordre à courte portée
- fonction de corrélation
- quasi-cristal
Solides ioniques et solides covalents
- Types de liaison
Les forces assurant la cohésion des solides sont toutes de nature fondamentalement électriques. Les diverses formes de celles-ci à l'échelle atomique se retrouvent dans les solides.
Le solide le plus dur, le diamant est maintenu par un ensemble de liaisons covalentes qui se renforcent mécaniquement réciproquement, exactement comme dans une molécule à squelette carboné. A l'autre extrémité, se trouvent les cristaux ioniques, par exemple le chlorure de sodium qui est un empilement de charges positives et négatives ordonné, mais sans liaison chimique : les électrons sont à demeure attachés à un noyau et il n'est pas question pour eux de participer directement à la cohésion entre atomes autrement que par l'intermédiaire des ions qu'ils forment. On parle de liaison ionique. Il existe un type de liaison intermédiaire, la liaison ionocovalente qui est une liaison covalente avec une probabilité plus forte de trouver l'électron dans le voisinage d'un type d'atomes que de l'autre. C'est ce type de liaison qu'on retrouve par exemple dans les cristaux du type blende. Dans le cas où la liaison entre les noyaux et les électrons périphériques est faible, l'électron peut passer indifféremment d'un atome à l'autre sur toute la longueur du cristal. On dit qu'il est délocalisé. Les modèles de telles liaisons sont les métaux, et les électrons délocalisés assurent alors la cohésion en créant un puits de potentiel piégeant les atomes sur tout le volume de l'échantillon. Une telle liaison est appelée liaison métallique. Reste enfin le cas des solides formés d'atomes ou de sous structures électroniquement stables, par exemple les cristaux de gaz rares. Aucun des mécanismes précédents ne peuvent s'appliquer à ceux-ci, mais il reste encore la possibilité d'une corrélation des orbitales électroniques entre deux atomes voisins : c'est la force de Van der Waals.
Métaux et isolants
- Classification des matériaux
L'une des plus anciennes classification des solides est fonction de leur résistivité électrique.
Bien avant de connaitre l'origine atomique de cette singularisation, on a distingué les métaux, presque tous bon conducteurs d'électricité et de chaleur, situés dans la partie inférieure gauche de la table de Mendeleïev. La résistivité de ceux-ci croit avec la température. Les autres éléments sont des isolants électriques. Les matériaux situés sur la quatrième colonne varient du statut isolant pour le carbone diamant à métal pour le plomb. Les matériaux compris entre ces deux extrêmes sont les semi-conducteurs (silicium, germanium). Ces matériaux ont une résistivité qui décroit avec la température, par la promotion thermique d'électrons de valence au statut d'électrons de conduction. L'étain est un cas intéressant car il possède une transition de phase entre un état semi-conducteur basse température (étain gris) et un état métallique haute température (étain blanc) ; c'est la transition de Mott. Celle-ci s'accompagne d'un changement de la structure cristalline et est une cause de désagrégation des étains anciens de collection. Une autre façon de faire varier la conductivité électrique d'un semi-conducteur est le dopage, qui par le biais d'impuretés soigneusement choisies enrichit le matériau en électrons de conduction ou en lacunes d'électrons de valence.