Aspartame - Définition
La liste des auteurs de cet article est disponible ici.
Structure et propriétés
Structure
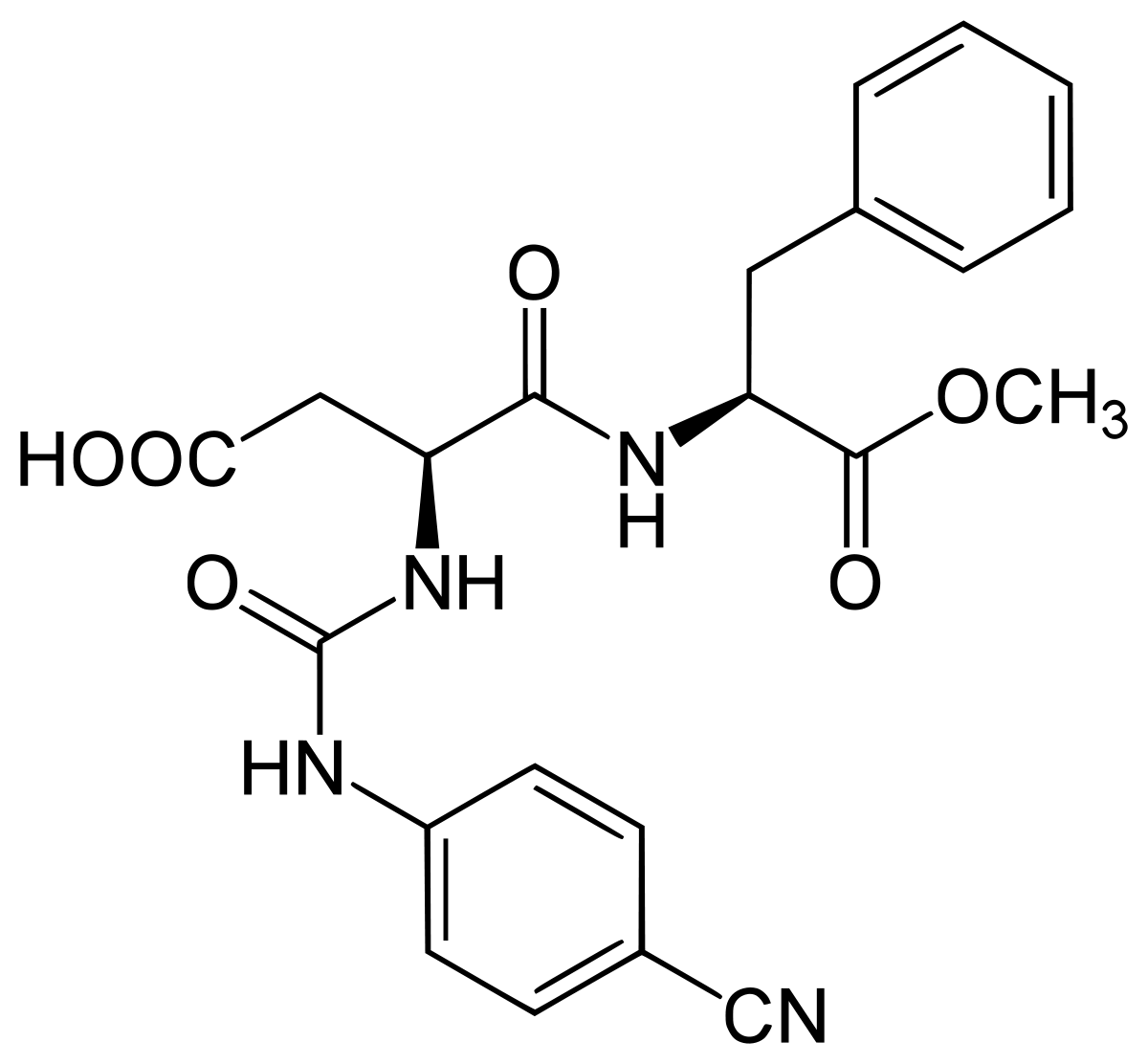
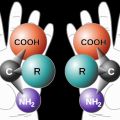
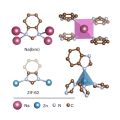
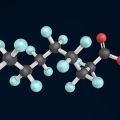
L'aspartame est un dipeptide, dérivant de deux acides aminés, l'acide L-aspartique et l'ester méthylique de la L-phénylalanine. Son nom chimique est donc * L-Aspartyl-L-phénylalanate de méthyle.
Propriétés chimiques
L'aspartame possède une base aminée et un groupement acide lui conférant deux constantes d'acidité, 3,1 et 7,9 à (25 °C).
Hydrolyse
Après ingestion, l'aspartame s'hydrolyse en acide aspartique, phénylalanine et méthanol. Une dégradation plus poussée produit du formaldéhyde, de l'acide formique et une dioxopipérazine.
Il peut également se décomposer pendant son stockage. À température ambiante il est le plus stable à pH 4,3, avec une demi-vie de 300 jours. On constate une décomposition plus rapides aux pH s'éloignant de 4,3. À pH 7, par exemple, sa demi-vie n'est que de quelques jours.
L'instabilité de l'aspartame augmente avec la température : en phase solide, la recombinaison en dicétopipérazine peut avoir lieu à partir de 105 °C. C'est la raison pour laquelle il est déconseillé de « cuisiner » l'aspartame.
L'hydrolyse de l'ester l'aspartame produit du méthanol (10 % en masse) et de l'aspartyl-phénylalanine. Ce dernier peut se recombiner en dicétopipérazine (acide 2-(5-benzyl-3,6-dioxopipérazin-2-yl)acétique) (à partir de 30 °C) ou bien s'hydrolyser en ces deux acides aminés de base l'acide aspartique (40 % en masse) et la phénylalanine (50 % en masse).
Réaction de Maillard
La fonction amine de l'aspartame peut participer aux réactions de Maillard avec les groupes aldéhydes.
Propriétés physiques
L'aspartame est un solide cristallin blanc, inodore et légèrement hygroscopique. Il est faiblement soluble dans l'eau (10 g·l-1 eau à 20 °C) et l'éthanol. Il se solubilise plus vite dans les solutions acides.
Biochimie
L'aspartame, contrairement au sucre, ne peut servir à la formation de graisses dans les tissus adipeux ni aux autres rôles métaboliques utiles de celui-ci.
Propriétés sucrantes
L'aspartame a un pouvoir sucrant environ 200 fois supérieur à celui du saccharose (à poids égal).
À la différence de la saccharine et de l'acésulfame-K, l'aspartame n'a pas de composante ou d'arrière-goût amer. Dans les études en aveugle toutefois, les boissons sucrées au saccharose ressortent comme « plus agréables ».
L'aspartame est souvent utilisé en mélange avec d'autre édulcorant intense (acésulfame-K) pour pallier la diminution de la saveur sucrée. La diminution est due à sa décomposition en milieu aqueux ou à sa disparition lors des réactions de Maillard entre celui-ci et les arômes possédant une fonction aldéhyde.
Un dérivé de l'aspartame, le superaspartame a un pouvoir sucrant de 8 000 à 14 000 fois supérieur à celui du saccharose.
Santé
L'aspartame fait partie des additifs alimentaires les plus étudiés, il est reconnu sûr pour la consommation humaine dans plus de 90 pays, notamment par les agences de sécurité sanitaire comme l'Autorité européenne de sécurité des aliments, le JECFA de l'OMS/FAO et la Food and Drug Administration. Toutefois, « même si des décennies de recherches scientifiques témoignent de l'innocuité de l'aspartame, des allégations négatives sur son innocuité paraissent dans les médias et sur Internet depuis des années. »
Diabète
On a formulé l'hypothèse que la saveur sucrée puisse provoquer une sécrétion d'insuline commandée par le cerveau (cephalic-phase insulin release, ou CPIR). Selon cette hypothèse, cette sécrétion d'insuline sans apport de glucose pourrait provoquer une chute de la glycémie ce qui provoquerait une sensation de faim. Les édulcorants utilisés par les personnes obèses pour perdre du poids auraient eu un effet inverse à celui recherché. Néanmoins, aucune étude n'a mis en évidence ce phénomène.
En 2000, une étude de la modification éventuelle de la thermogenèse apportée par une alimentation édulcorée à l'aspartame en comparaison avec une alimentation sucrée au saccharose n'a mis en évidence aucune différence significative.
Selon le ministère de la santé du Canada, l'utilisation de l'aspartame est sans danger pour les diabétiques.
Métabolisme
Lors de la digestion, l'aspartame perd son groupement hydroxyméthyl (méthanol), puis se décompose en ses deux acides aminés de base, l'acide aspartique et la phénylalanine. Sous l'effet de la chaleur, il peut aussi se recombiner pour former de la dicétopipérazine. En comparaison avec les aliments courants, l'aspartame est une source mineure de phénylalanine, d'acide aspartique et de méthanol.
Phénylalanine
La phénylalanine est un des huit acides aminés essentiels, elle est notamment naturellement présente dans le lait des mammifères. Seules les personnes souffrant de phénylcétonurie (PKU), une maladie génétique rare (1/16 000 naissances) doivent contrôler de façon très stricte l'apport en phénylalanine, c'est pourquoi les produits contenant de l'aspartame doivent renseigner qu’ils contiennent une source de phénylalanine.
Méthanol
Le méthanol est un alcool naturellement présent dans des aliments courants : fruits mûrs, jus de fruits et les aliments fermentés (vin, bière ...). Des allégations parues sur internet et dans certains médias affirment que le méthanol contenu dans l'aspartame serait toxique, ces allégations sont sans fondement selon le ministère de la santé du Canada : « Le méthanol alimentaire, qu'il provienne de l'aspartame ou d'aliments courants, est présent à des concentrations trop faibles pour causer des problèmes de santé. Il ne s'accumule pas dans le corps, mais il est plutôt métabolisé, par les voies du métabolisme normal, en formaldéhyde d'abord, ensuite en acide formique et finalement en eau et en gaz carbonique. »
Toutefois, le méthanol présent dans les aliments courants est souvent lié à d'autres éléments, tels que des peptides dans les fruits, qui permettent sa métabolisation, laquelle n'est pas possible dans le cas de l'aspartame qui libère son groupement hydroxyméthyl seul lors de la digestion.
Acide aspartique
L'acide aspartique est un acide aminé, non toxique pour l'organisme qui ne pose pas de problème lors de la métabolisation de l’aspartame. C'est un constituant courant des protéines de l’organisme.
Dicétopipérazine
La dicétopipérazine n’est pas considérée comme génotoxique (provoquant l'apparition de lésions dans l'ADN, qui peuvent éventuellement conduire à des mutations) ni cancérogène chez le rat et la souris. La dose journalière acceptable de la dicétopipérazine pour l'homme a été fixée à 7,5 mg·kg-1·j-1.
Controverse
Depuis sa mise sur le marché, il y a eu des polémiques sur l'innocuité de l'aspartame, alimentées par des accusations de conflits d'intérêts, certaines publications scientifiques, des théories du complot et des canulars informatiques (hoax) propagés par courrier électronique sous forme de chaîne de lettres.
En juillet 2005, des chercheurs de la Fondation européenne Ramazzini, à Bologne (Italie), ont présenté à la presse une étude menée sur des rats montrant un effet cancérogène au niveau du cerveau. Cette étude a été critiquée par des agences de sécurité sanitaire, notamment pour sa méthodologie qui ne supporterait pas ses conclusions. L'Autorité européenne de sécurité des aliments (EFSA) après une analyse détaillée des conditions opératoires de cette étude a conclu qu'il n'y a aucune raison de changer les conditions d'utilisation de l'aspartame en Europe. La France a aussi émis des réserves sur la méthode d'étude et des doutes quant à la validité des résultats et s'en tient à une « veille toxicologique » sur l'aspartame.