Coumarine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Coumarine | |||
|---|---|---|---|
| |||
| Général | |||
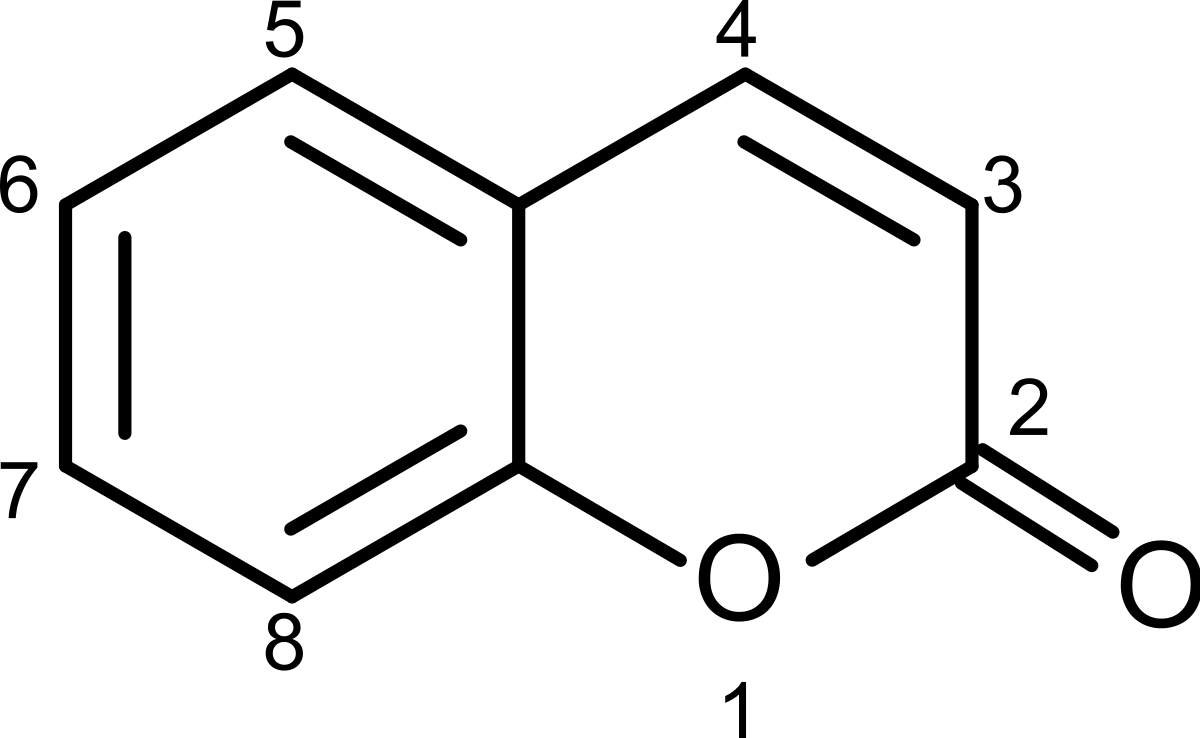
| Nom IUPAC | |||
| Synonymes | 2H-chromenone Cumarine Benzo-α-pyron | ||
| No CAS | |||
| No EINECS | |||
| PubChem | |||
| SMILES | |||
| InChI | |||
| Apparence | flocons incolores, d'odeur caractéristique. | ||
| Propriétés chimiques | |||
| Formule brute | C9H6O2 | ||
| Masse molaire | 146,1427 ± 0,0082 g·mol-1 | ||
| Propriétés physiques | |||
| T° fusion | 69 à 71 °C | ||
| T° ébullition | 301,7 °C | ||
| Solubilité | Faible (1,9 g·l-1 à 20 °C) | ||
| Masse volumique | 0,94 g·cm-3 | ||
| Point d’éclair | 150 °C | ||
| Pression de vapeur saturante | à 106 °C : 0,13 kPa | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 22, | |||
| Phrases S : 36, | |||
| | |||
| |||
| | |||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme | |||
| Écotoxicologie | |||
| DL | 0,196 g·kg-1 (souris, oral) 0,293 g·kg-1 (rats, oral) | ||
| LogP | 1,39 | ||
| Classe thérapeutique | |||
| Anticoagulant | |||
| Composés apparentés | |||
| Isomère(s) | isocoumarine chromone | ||
| | |||
La coumarine est une substance naturelle organique aromatique connue dans la nomenclature internationale comme 2H-1-benzopyrane-2-one qui peut être considérée en première approximation, comme une lactone de l’acide 2-hydroxy-Z-cinnamique. Son odeur de foin fraîchement coupé a attiré l'attention des parfumeurs sur elle dès le XIXe siècle.
Le même terme de coumarine désigne aussi la classe des composés phénoliques dérivés de cette dernière molécule, la 2H-1-benzopyrane-2-one. Ces composés possèdent des hydroxyles phénoliques qui peuvent être méthylés ou être engagés dans des liaison hétérosides. Plus d’un millier de coumarines naturelles ont été décrites. Elles sont très largement distribuées dans le règne végétal.
La coumarine tire son nom de kumarú, le nom dans une langue amérindienne tupi de Guyane de l’arbre poussant en Amérique du Sud, le gaiac de Cayenne (Dipteryx odorata) de la famille des Fabacées, donnant la fève tonka d’où cette molécule fut isolée en 1820 par Vogel. Le nom de tonka vient aussi du tupi et d’une langue caraïbe de Guyane, le kali’na (ou galibi).
La première section traitera de la coumarine simple suivie d’une section portant sur la famille des coumarines.
La coumarine simple
La coumarine fut l'une des premières synthèses aromatiques réalisées vers la fin du XIXe siècle (1868) par le chimiste anglais William H. Perkin. Quelques années plus tard, en 1882, Paul Parquet employa cette molécule de synthèse pour créer "Fougère Royale", un parfum de Houbigant (devenu H pour homme), puis Aimé Guerlain l'utilisa pour "Jicky de Guerlain", en 1889. Ces usages marquèrent un tournant dans l’histoire des parfums et arômes de synthèses.
Elle est depuis peu réglementée pour des raisons d'hépatotoxicité.
Plantes riches en coumarine
La coumarine est présente dans divers végétaux :
- la fève tonka, fruit du gaiac de Cayenne (Dipteryx odorata) de la famille des Fabacées, est très riche en coumarine (de 1 à 3,5 %). À maturité, la fève libère des arômes de vanille, de foin et d’amande. Elle est en vogue auprès de quelques grands chefs qui l’utilisent pour parfumer les crèmes et les gâteaux. Elle servait à aromatiser certains tabacs à pipe comme l'Amsterdamer. La coumarine utilisée en parfumeries (Shalimar de Guerlain ou Contradiction de Calvin Klein) ou pour aromatiser les aliments ou les boissons est surtout obtenue par synthèse
- l’aspérule odorante, (Galium odoratum) ou gaillet odorant (de la famille des Rubiacées ), est peu odorante à l'état frais mais prend au séchage une agréable senteur de foin, due au développement de la coumarine. La plante sèche comporte de 1 à 1,3 % de coumarine (13 000 mg·kg-1)
- la racine de la flouve odorante (Anthoxanthum odoratum) ou "Chiendent odorant" (de la famille des Graminées)
- la cannelle de Chine (Cinnamomum aromaticum) ou casse est riche en coumarine (0,45%) et en aldéhyde cinnamique (2,56 %) et contient des traces d’eugénol alors que l’inverse est vraie de la cannelle de Ceylan (Cinnamomum verum)
- les tiges feuillées du Mélilot officinal ou Mélilot jaune (Melilotus officinalis de la famille des Fabacéess) renferme, surtout dans les jeunes feuilles, du mélilotoside, glucoside de l'acide 2-hydroxycinnamique qui conduit par lactonisation à la coumarine ( 2 000 mg·kg-1 soit 0,2 %)
- la feuille de maïs (Zea mays) avec 0,2 % est aussi riche
- la lavande vraie (Lavandula angustifolia) avec 1 500 mg·kg-1 est beaucoup plus riche que la lavande aspic (Lavandula latifolia) qui n’en contient que 22 mg·kg-1
- l'angélique officinale (Angelica archangelica) renferme de nombreuses coumarines : simples, furaniques et hydroxy-isopropyldihydrofuraniques
- le céleri (Apium graveolens), le panais (Pastinaca sativa), la grande berce (Heracleum sphondylium), la berce du Caucase (Heracleum mantegazzianum) ou la rue (Ruta graveolens) sont photoxiques par contact en raison de la présence de furanocoumarines linéaires (psoralène, bergaptène et xanthotoxine, voir la dernière section sur les coumarines)
La coumarine simple dégage une agréable odeur, rappelant la vanilline et contribue à l'odeur de foin coupé.

Aspérule odorante |
Propriétés physico-chimiques
- Composition élémentaire : 73,96 % C + 21,90 % O + 4,14 % H ;
- Masse molaire : 146,15 g ;
- Point de fusion (1013 hPa) : 342 K (69 °C) ;
- Point d'ébullition (1013 hPa) : 574 K (301 °C) ;
- Hydrosolubilité : faible (2,5 g par dm³ d'eau froide et 20 g/dm³ d'eau portée à ébullition) ;
- Soluble dans les alcools et dans les solvants organiques comme le dioxyde d'éthyle ou les solvants chlorés
- Cristallographie : solide formé de cristaux orthorhombiques ;
- Classe de toxicité : nocif (DL50 d'environ 500 mg·kg-1 pour le rat et le cochon d'Inde).
Absorption et métabolisme chez l'homme
Pour Lake (1999), la source principale de coumarine dans l’alimentation viendrait de la cannelle souvent présente sous forme d’arôme alimentaire. Il estime l'exposition journalière par l'alimentation à 0,02 mg·kg-1·j-1.
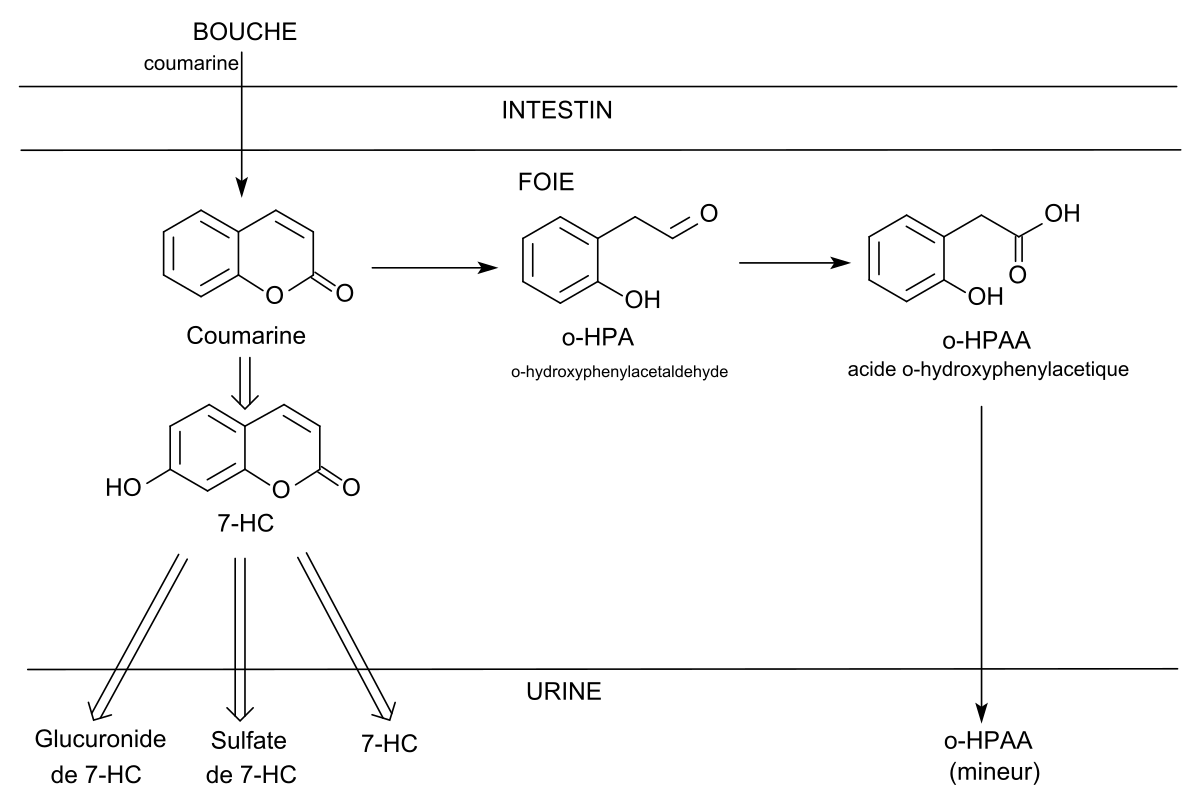
Après ingestion, la coumarine est rapidement et complètement absorbée dans le tube digestif puis massivement métabolisée dans le foie. Elle y subit principalement une hydroxylation en 7-hydroxycoumarine 7-HC (pour 84%) et une ouverture du cycle de la lactone, avant d’être en grande partie excrétée dans les 24 heures, par voie rénale (voir figure 1). Son temps de demi-vie dans l'organisme humain est d’une heure.
Chez l’homme, la voie par la 7-hydroxylation est très largement majoritaire et donne des métabolites peu toxiques : la 7-hydroxycoumarine et ses conjugués glucuronidés et sulfatés. Par contre, chez le rat, aucune 7-HC n’est détectée dans ses urines après une ingestion de coumarine et l’autre voie produit des composés très toxiques.
Usage en médecine
En médecine, la coumarine est utilisée dans le traitement adjuvant du lymphœdème post-mastectomie, en complément des méthodes de contention. Son action antiœdématique résulte de l'augmentation du drainage lymphatique et de la stimulation de l'activité protéolytique des macrophages. Mais la multiplication des cas d’hépatite chez les patientes traitées à fortes doses avec cette molécule a conduit au retrait du marché de la spécialité correspondante.
La coumarine reste utilisée en phytothérapie, mais à des doses beaucoup plus faible, comme dans les spécialités contenant du mélilot.
A la différence de ses dérivés (comme la coumadine), la coumarine elle-même n’a pas d’activité anticoagulante.
Mais la fermentation humide de foin qui renferme de la coumarine (en raison de la présence de mélilot) génère des dérivés anticoagulants, qui entraînent des hémorragies chez les herbivores qui en consomment. Le 4-hydroxy-3-[1-(4-nitrophényl)-3-oxobutyl]coumarine, appelé usuellement acénocoumarol, est antagoniste de la vitamine K et inhibiteur de la synthèse des facteurs de la coagulation vitamino-K-dépendants. Ses propriétés anticoagulantes sont utilisées dans la thérapie des maladies thromboemboliques.
Usage alimentaire
Le codex alimentarius a recommandé en 1985 (réaffirmé en 2006) de ne pas ajouter la coumarine telle quelle aux aliments et aux boissons. Elle peut être présente dans les aliments et les boissons seulement sous la forme de préparations aromatisantes naturelles (par exemple l'extrait de fève tonka) et pas à plus de 2 mg·kg-1 dans les denrées alimentaires et les boissons et de 10 mg·kg-1 dans les caramels spéciaux. En 2004 puis en juillet 2008, l’Autorité européenne de sécurité des aliments (efsa) a recommandé une dose journalière acceptable (DJA) de 0,1 mg de coumarine/kg de poids corporel. Un calcul simple permet de s’apercevoir que la DJA est très largement dépassée par une cuillérée à café de cannelle de Chine. D'où l'importance de bien distinguer cette cannelle de la cannelle de Ceylan, indemne de coumarine.
En cuisine, les fleurs d'aspérule odorante, au parfum caractéristique, sont utilisées dans la région d'Arlon (Belgique) pour la fabrication du Maitrank. La coumarine est aussi présente dans certaines variétés de cannelle.
Enfin la coumarine est fortement contenue dans l'herbe de bison, une plante utilisée notamment pour la fabrication de la vodka polonaise Żubrówka. Cette vodka a d'ailleurs été interdite à la vente aux États-Unis pour cette raison en 1978.
Autres usages
L'odeur de foin fraîchement coupé de la coumarine est très utilisée en parfumerie. Actuellement, elle entre dans la composition de 90% des parfums (dans 60% avec une teneur supérieure à 1%). Elle s'associe bien à la vanilline dont elle atténue le côté alimentaire. Elles est aussi utilisée dans les produits cosmétiques (déodorants, eaux de toilette, crèmes, shampoings, savons de toilette, dentifrice, etc.).
On trouve aussi de la coumarine dans les cigarettes indiennes, les bidî, et les cigarettes aux clous de girofle indonésiennes, les kreteks.
Pour neutraliser ou masquer les mauvaises odeurs, la coumarine est aussi ajoutée aux peintures, insecticides, encres, aux aérosols, au caoutchouc ou aux matières plastiques.