Uranium - Définition
| Données | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Général | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, Symbole, Numéro | Uranium, U, 92 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Série chimique | Actinides | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, Période, Bloc | L/A, 7, f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse volumique | 19 050 kg/m3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Couleur | Gris métallique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse atomique | 238,028 91 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique (calc) | 175 (ND) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de covalence | ND pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de van der Waals | 186 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [Rn] 7s2 5f3 6d1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électrons par niveau d'énergie | 2, 8, 18, 32, 21, 9, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État(s) d'oxydation | 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxyde | base faible | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure cristalline | Orthorhombique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État ordinaire | Solide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Température de fusion | 1405 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Température de vaporisation | 2070 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de fusion | 15,48 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de vaporisation | 477 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molaire | 12,49×10-6 m3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pression de la vapeur | 1,63×10-8 Pa à 453,7 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vélocité du son | 3155 m/s à 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Divers | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électronégativité (Pauling) | 1,38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur massique | 120 J/(kg·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité électrique | 3,8×106 S/m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité thermique | 27,6 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1er potentiel d'ionisation | 597,6 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2e potentiel d'ionisation | 1420 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes les plus stables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI & CNTP, sauf indication contraire. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L'uranium est un élément chimique de symbole U et de numéro atomique 92.
Découverte de l'uranium
L'uranium a été mis en évidence en 1789 par le chimiste prussien Martin Heinrich Klaproth en chauffant la pechblende (UO2), un minerai d'uranium. Klaproth donna le nom d'" urane " ou " uranite " au composé qu'il venait d'identifier, en référence à la découverte de la planète Uranus faite par William Herschel huit ans plus tôt (1781).
Ce n'est que cinquante ans plus tard que le chimiste français Eugène Péligot établit que l'urane était composé de deux atomes d'oxygène et d'un de métal, métal qu'il isola et nomma uranium.
Henri Becquerel ne découvrit la propriété radioactive de l’uranium que beaucoup plus tard, en 1896, lorsqu'il constata que des plaques photographiques placées à côté de sels d'uranium avait été impressionnées sans avoir été exposées à la lumière du soleil. Les plaques avaient été noircies par les rayonnements émis par les sels : le Français Henri Becquerel avait découvert le phénomène de la radioactivité naturelle.
Caractéristiques
De symbole U, l'uranium est le dernier élément naturel du tableau périodique de Mendeleïev. Chaque atome d'uranium possède 92 protons et entre 135 et 148 neutrons.
A l'état pur, l'uranium solide est un métal radioactif gris à blanc (voire argenté), qui rappelle la couleur du nickel. Il est dur et très dense. De plus, l'uranium est l'atome le plus lourd (qui contient le plus de nucléons) présent naturellement sur la Terre.
L'uranium a dix-sept isotopes, tous radioactifs, dont trois seulement sont présents à l'état naturel : 238U ; 235U et 234U.
L'uranium naturel
L'uranium naturel est présent dans pratiquement tous les milieux naturels : roches et eau. Il y a en effet 3 mg/d'uranium par mètre cube d'eau de mer ce qui représente tout de même 4,5 milliards de tonnes d'uranium dans les océans ! L'uranium est vraiment présent dans tous les types d'eau : le Rhône en charrie en effet près de 100 tonnes chaque année. Cet uranium provient du ruissellement des pluies sur les Alpes. L'extraction de l'uranium de l'eau est, techniquement possible, mais non rentable en 2006.
L'uranium est tout de même relativement répandu dans l'écorce terrestre, notamment dans les terrains granitiques et sédimentaires. La concentration d'uranium dans ces roches est de l'ordre de 3 g/tonne. À titre d'exemple, un jardin carré de 20 m de côté contient, pour une profondeur de 10 m, environ 24 kg d'uranium.
Proportions
Quelles que soient les teneurs en uranium des milieux, les proportions entre les trois isotopes formant l'uranium naturel sont (presque) exactement les mêmes : 238U : 99,28% ; 235U : 0,71% ; 234U : 0,0054%.
On trouve donc dans une tonne d'uranium naturel pur : 992,8 kg d'uranium 238, 7,1 kg d'uranium 235 et 0,054 kg d'uranium 234.
Il est à noter que l'isotope 234 est toujours présent sur Terre, bien qu'il ait une demi-vie de seulement 245 500 ans, car il est constamment généré par l'isotope 238 (après 3 radioactivités : α, β − , β − ). L'isotope 236 s'est éteint depuis longtemps bien qu'ayant une demi-vie presque centuple !
Autres propriétés
En raison de son affinité pour l'oxygène, l'uranium s'enflamme spontanément dans l'air à température élevée, voire à température ambiante lorsqu'il se trouve sous forme de microparticules.
De plus, l'élément uranium se retrouve toujours en combinaison avec d’autres éléments tels l'oxygène, l'azote, le soufre, le carbone. On le trouve par exemple en combinaison avec l'oxygène dans l'uranite et la pechblende, deux des principaux minerais d'uranium, constitués d'oxyde uraneux (UO2).
Enfin, les ions uranyles (
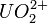
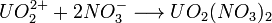
Les isotopes de l'uranium naturel
L'uranium naturel est composé de trois isotopes : l'uranium 235, l'uranium 238 et l'uranium 234.
L'uranium 235 est le seul nucléide naturel qui soit fissile, ou fissible : il est donc susceptible de subir la fission nucléaire.
Au contraire de l'uranium 235, l'uranium 238, lorsqu'il capture un neutron, ne fissionne pas (sauf neutrons rapides). Il devient de l'uranium 239 instable, qui par désintégration β − , va se transformer en neptunium 239. Or ce dernier est lui-aussi radioactif β − , et va alors donner naissance à un nouveau noyau, le plutonium 239. Ce radioisotope est fissile, comme l'uranium 235. L'uranium 238 est un isotope fertile, qui peut produire à des produits fissiles.
L'uranium 234 n'est lui ni fissile, ni fertile, et provient de la décomposition radioactive de l'uranium 238.
Une des origines de la chaleur interne de la Terre
En plus de la chaleur d'accrétion, la chaleur interne de la Terre provient aussi de la désintégration de corps radioactifs, notamment l'uranium 238 et 235 (et bien d'autres). Ceci peut s'expliquer de façon relativement simple : lors de leur désintégration radioactive, l'uranium 238 et l'uranium 235 vont émettre des rayonnements γ, qui sont de l'énergie à l'état pur. Cette énergie est alors convertie en chaleur. Des milliards de milliards de désexcitations γ ont lieu chaque seconde à l'intérieur de la Terre, et on comprend facilement pourquoi la radioactivité est à l'origine de près de 87 % de l'énergie thermique de la Terre.
Utilisation
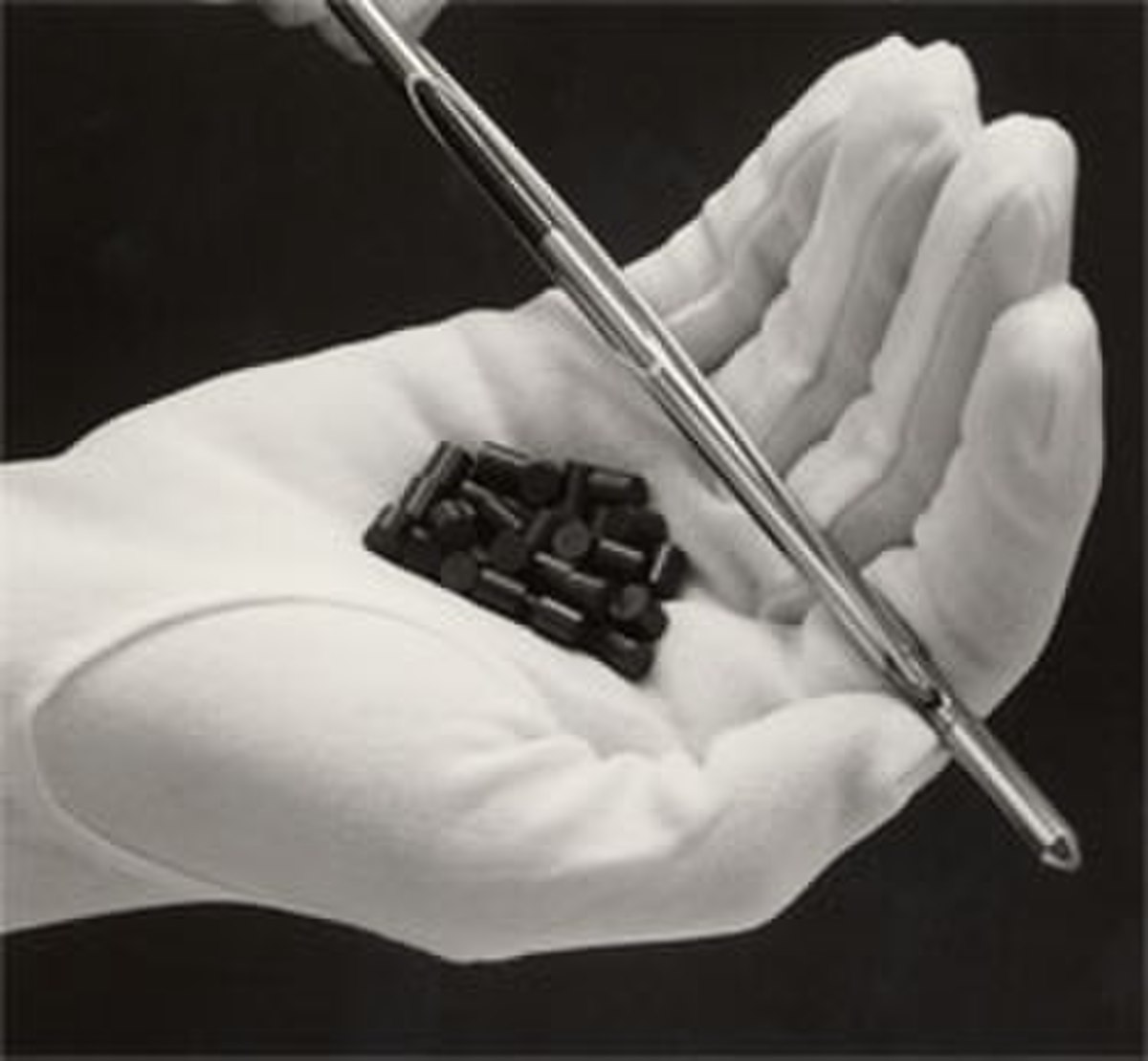
À l'origine, le minerai d'uranium était utilisé dans la céramique et la faïence pour ses pigments jaune, orange et vert.
Les uraniums 238 et 235 ont beaucoup d'applications, militaires notamment, mais aussi civiles comme par exemple la datation de l'âge de la Terre à partir de la datation radiométrique.
Combustible nucléaire
L'uranium est aujourd'hui utilisé comme combustible nucléaire dans les réacteurs nucléaires (voir cycle du combustible nucléaire).
Armes nucléaires
L'uranium enrichi (en uranium 235) peut aussi servir à la réalisation d'armes nucléaires comme les bombes atomiques (bombes A ou " bombes à fission "), ou les bombes H (" bombes à fusion " ou encore " bombes à hydrogène ").
Uranium appauvri
L'uranium appauvri, un sous produit de l'enrichissement de l'uranium, est très prisé pour sa dureté et sa densité. De plus, il est pyrophorique et il est donc employé comme arme antichar ayant un fort pouvoir pénétrant et incendiaire. À très haute vitesse, il perfore aisément les blindages en s'enflammant lors de l'impact, provoquant un incendie qui fait exploser le véhicule visé. Ainsi, des munitions à base d'uranium appauvri (obus de 20 à 30 mm des avions ou hélicoptères chasseurs de chars) ont été utilisées lors des guerres du Golfe (guerre du Koweït et guerre en Irak) et du Kosovo.
L'uranium appauvri est aussi utilisé, avec un complément de plutonium, comme nouveau combustible nucléaire (combustible MOX).
Cependant, l'uranium appauvri peut produire, à courte distance, les mêmes radiations qu'une explosion nucléaire et provoquer de graves problèmes sur le corps humain.[réf. nécessaire]
Gisements et exploitation
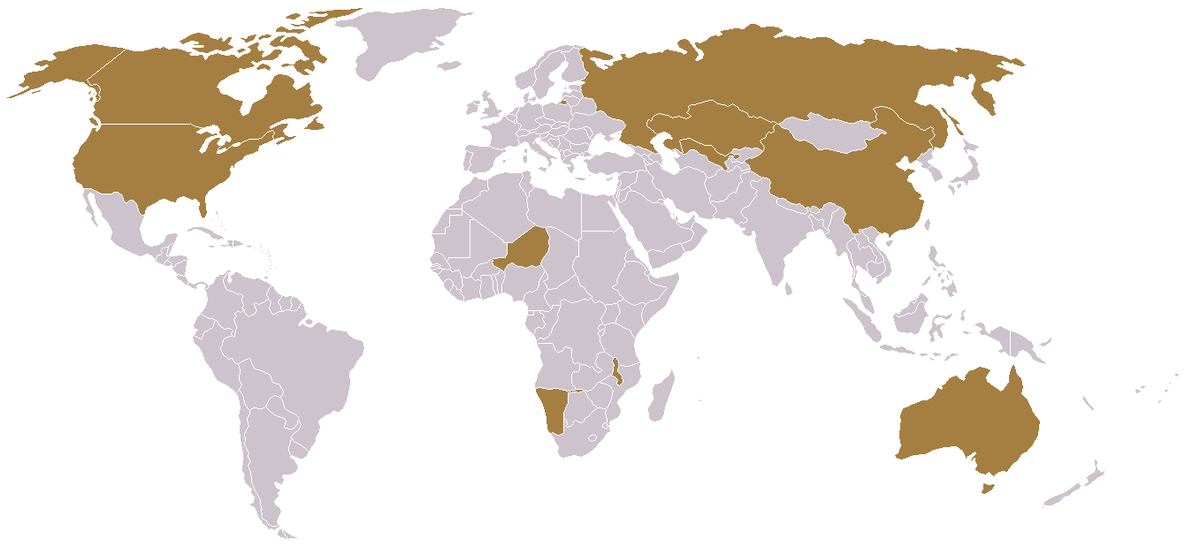
Les principaux gisements uranifères se situent au Canada, en Australie, au Niger et au Kazakhstan (tous des pays d'une grande superficie). On estime actuellement rentables des gisements qui présentent des teneurs supérieures à 0,5 kg/tonne de roche.
En France, on compte près de 170 anciens sites d'extraction et de traitement des minerais d'uranium. Tous ces sites ont représenté une production d'environ 72 800 tonnes d'uranium. Les gisements les plus riches comptent 1 à 5 kilogrammes d'uranium par tonne de minerai. L'activité minière française, pour l'extraction d'uranium en tout cas, a pris fin en 2001 avec la fermeture des mines de Jouac, en Haute-Vienne. En effet, la France ne présente pas de ressources minières en uranium suffisamment rentables.
Quelques sites remarquables
- À la mine de Cigar Lake, au Canada, est extrait un minerai qui contient jusqu'à 210 kilogrammes d'uranium par tonne de minerai !
- La mine de Shinkolobwe, en République démocratique du Congo, est aujourd'hui officiellement fermée. Elle a fourni dès 1939 de l'uranium aux États-Unis d'Amérique qui l'ont notamment utilisé pendant la Seconde Guerre mondiale pour leur programme nucléaire (Projet Manhattan). L'uranium de la bombe atomique lancée sur Hiroshima provenait de cette mine.
- Les mines d'Arlit au Niger, exploitées par Areva, ont fourni depuis les années 1970 l'essentiel de l'uranium français.
Gisements sous discordance
Les minéralisations uranifères de type discordance ont été découvertes pour la première fois à la fin des années 1960 dans les bassins de l'Athabasca (Canada) et de Mc Arthur (Australie). Leur richesse est exceptionnelle. Ce sont actuellement (en 2003) les seuls gisements rentables d'uranium seul.
Les dépôts d'uranium se situent à l'interface entre un socle d'âge archéen à protérozoïque inférieur et une puissante couverture de grès du protérozoïque moyen. Ils sont généralement associés à des failles à graphite et entourés de halos d'altérations argileuses de haute température. Les minéralisations ne sont pas clairement datées mais sont plus récentes que les couvertures sédimentaires.
Le modèle communément admis pour la genèse de ces gisements est diagénétique hydrothermal, c'est-à-dire que le dépôt a lieu pendant la diagenèse à la faveur de circulations de fluides. Une saumure très concentrée et oxydante percole dans le socle et s'enrichit en calcium, magnésium et uranium par dissolution de monazite, s'appauvrit en quartz et augmente sa température. Au contact d'un front rédox à la discordance, cette saumure dissout du quartz et précipite de l'uranium dans l'espace libéré. Des altérations, remobilisations et précipitations successives ont probablement lieu ultérieurement.
Les mécanismes de minéralisation en Australie et au Canada sont assez semblables mais leurs formes et leurs emplacements différent sensiblement, ce qui amène les scientifiques à spéculer sur des mécanismes de réduction différents pour les deux bassins. Les géologues essayent cependant de comprendre ce qu'ils ont en commun pour trouver de nouveaux gisements de ce type. Enfin, l'analogie entre ce type de gisement et la conception actuelle du stockage des déchets radioactifs en couche géologique profonde intéresse fortement les chercheurs.