Chronologie de la chimie - Définition
Source: Wikipédia sous licence CC-BY-SA 3.0.
La liste des auteurs de cet article est disponible ici.
La liste des auteurs de cet article est disponible ici.
XXe siècle
- 1903
- Mikhail Semenovich Tswett invente la chromatographie.
- 1904
- Hantaro Nagaoka propose un modèle de la structure de l'atome, où les électrons orbitent autour d'un noyau dense.
- 1905
- Albert Einstein explique le mouvement brownien et prouve définitivement l'existence des atomes.
- 1907
- Leo Hendrik Baekeland invente la bakélite, l'un des premiers plastiques commercialisés à grand succès.
- 1909
- Ernest Rutherford, Hans Geiger, et Ernest Marsden réalisent l'expérience de la feuille d'or, qui prouve que l'atome est composé d'un noyau positif extrêmement dense entouré d'un nuage électronique diffus.
- 1909
- Robert Millikan mesure la charge élémentaire de l'électron avec une précision inégalée grâce à son expérience de la goutte d'huile, qui confirme que tous les électrons ont la même charge et masse.
- 1909
- Søren Sørensen introduit le concept de pH et développe une méthode de mesure de l'acidité.
- 1909
- Fritz Haber met au point le procédé Haber pour la synthèse de l'ammoniac à partir d'hydrogène et d'azote, ce qui provoquera une révolution dans l'industrie chimique.
- 1911
- Antonius Van den Broek propose l'idée que les éléments sur le tableau périodique sont mieux organisés en les classant par la charge nucléaire positive que par la masse atomique.
- 1911
- Le premier congrès Solvay est tenu à Bruxelles, réunissant les scientifiques les plus renommés de l'époque. Des conférences en chimie et physique continuent à ce jour à être tenues régulièrement.
- 1912
- William Henry Bragg et William Lawrence Bragg proposent la loi de Bragg et créent la discipline de la diffractométrie de rayons X, un outil important dans la détermination des structures cristallines de substances..
- 1912
- Peter Debye développe le concept de dipôle moléculaire pour décrire des distributions de charge asymétriques dans certaines molécules.
- 1913
- Niels Bohr présente le modèle de Bohr, un modèle de la structure atomique utilisant la mécanique quantique et où les électrons ne peuvent se trouver que sur certaines orbitales bien définies.
- 1913
- Henry Moseley, travaillant sur l'idée de Van den Broek (cf. supra), introduit le concept de numéro atomique pour corriger des inconsistances dans le tableau périodique proposé par Mendeleev, qui était lui basé sur la masse atomique des éléments.
- 1913
- Frederick Soddy propose le concept d'isotopes, que des éléments ayant les mêmes propriétés chimiques pouvaient avoir des masses différentes.
- 1913
- Joseph John Thomson démontre que des particules subatomiques chargées peuvent être séparées par leur rapport masse/charge, ce qui est connu sous le nom de spectrométrie de masse.
- 1913
- Carl Bosch et ses collaborateurs complètent l'industrialisation du procédé Haber (également appelé procédé Haber-Bosch), ce qui amènera une révolution dans l'industrie chimique et aura d'importantes conséquences en agriculture.
- 1916
- Gilbert N. Lewis publie The Atom and the Molecule, qui contient les fondations de la théorie de la liaison de valence.
- 1921
- Otto Stern et Walther Gerlach établissent le concept du spin.
- 1923
- Gilbert N. Lewis et Merle Randall publient Thermodynamics and the Free Energy of Chemical Substances, premier traité moderne de thermodynamique chimique. La même année, Gilbert N. Lewis développe la théorie de paire électronique dans la théorie des réactions acide/base.
- 1924
- Louis de Broglie introduit le modèle ondulatoire en mécanique quantique en se basant sur les idées de la Dualité onde-particule.
- 1925
- Wolfgang Pauli développe le principe d'exclusion, qui énonce que deux électrons d'un atome ne peuvent se trouver dans le même état quantique, décrit par quatre nombres quantiques.
- 1926
- Erwin Schrödinger propose l'équation de Schrödinger, qui fournit une base mathématique pour le modèle ondulatoire.
- 1927
- Werner Heisenberg développe le principe d'incertitude qui explique le mécanisme du mouvement de l'électron autour du noyau atomique, tandis que Fritz London et Walter Heitler appliquent les principes de la mécanique quantique pour expliquer la liaison covalente de la molécule d"hydrogène marquant le début de la chimie quantique.
- 1930
- Linus Pauling propose les règles de Pauling, qui sont les principes clés pour l'utilisation de la cristallographie à rayons X pour déduire la structure moléculaire.
- 1930
- Une équipe de chimistes dirigée par Wallace Carothers à DuPont développe le nylon, l'un des polymères synthétiques les plus commercialisés de l'histoire.
- 1931
- Erich Hückel propose la règle de Hückel, qui explique les propriétés aromatiques d'une molécule cyclique plane.
- 1931
- Harold Urey découvre le deutérium par distillation fractionnée d'hydrogène liquide.
- 1932
- James Chadwick découvre le neutron.
- 1932
- Linus Pauling est le premier à décrire les propriétés de l'électronégativité comme un moyen de prédire le moment dipolaire d'un lien chimique.
- 1937
- Carlo Perrier et Emilio Segrè réalisent la première synthèse confirmée de technétium-97, le premier élément artificiel produit, complétant ainsi une case manquante du tableau périodique.
- 1937
- Eugène Houdry développe une méthode pour le craquage catalyique du pétrole, ce qui aboutit au développement de la première raffinerie de pétrole..
- 1937
- Pyotr Kapitsa, John Allen et Don Misener obtiennent de l'hélium à l'état superfluide (de viscosité nulle). Les propriétés macroscopiques de cette phase de l'hélium peuvent être expliquées par la mécanique quantique.
- 1938
- Otto Hahn découvre la fission nucléaire de l'uranium et du thorium.
- 1939
- Linus Pauling a publié The Nature of the Chemical Bond une somme de décennies de travail sur la liaison chimique. Il s'agit d'un des textes chimiques modernes les plus importants. Il détaille la théorie de l'hybridation des orbitales, les liaisons covalentes et ioniques expliquées en fonction de l'électronégativité, ainsi que la mésomérie.
- 1940
- Edwin McMillan et Philip H. Abelson découvrent le neptunium, le plus léger et le premier synthétisé des transuraniens, produit de la fission de l'uranium. McMillan fonde un laboratoire à Berkley où seront découvert plusieurs nouveaux éléments et isotopes.
- 1941
- Glenn T. Seaborg poursuit les travaux de McMillan en créant des nouveaux noyaux d'atomes grâce à la méthode de capture des neutrons puis ensuite par des réactions nucléaires.
- 1945
- Jacob A. Marinsky, Lawrence E. Glendenin, et Charles D. Coryell réalisent la première synthèse du prométhium, comblant un " vide" dans la classification périodique des éléments History of the Elements of the Periodic Table, AUS-e-TUTE. Consulté le 2007-03-26 .
- 1945-1946
- Felix Bloch et Edward Mills Purcell développent le procédé de résonance magnétique nucléaire, une technique importante d'analyse des structures des molécules en chimie organique.
- 1951
- Linus Pauling utilise la cristallographie par rayon X pour déduire la structure secondaire des protéines.
- 1952
- Alan Walsh pionnier dans le domaine de la spectroscopie d'absorption, une importante méthode quantitative qui permet de mesurer la concentration spécifique d'un composé dans un.
- 1952
- Robert Burns Woodward, Geoffrey Wilkinson, et Ernst Otto Fischer découvrent la structure du ferrocène, une des premières découvertes qui marque le début de la chimie organométallique.
- 1953
- James D. Watson et Francis Crick proposent une structure de l'ADN, début de la biologie moléculaire.
- 1958
- Max Perutz et Sir John Cowdery Kendrew utilisent la cristallographie par rayons X pour élucider la structure d'une protéine, la myoglobine du Grand Cachalot.
- 1962
- Neil Bartlett synthétise l'hexafluoroplatinate de xénon, prouvant pour la première fois que les gaz nobles peuvent former des composés chimiques.
- 1964
- Richard R. Ernst réalise des expériences qui vont mener au développement de la RMN par transformée de Fourier, augmentant la sensibilité de cette technique et ouvrant la porte à l'imagerie par résonance magnétique RMI.
- 1965
- Robert Burns Woodward et Roald Hoffmann établissent les règles de Woodward-Hoffmann, qui utilisent la symétrie des orbitales moléculaires pour expliquer la stéréochimie des réactions chimiques.
- 1985
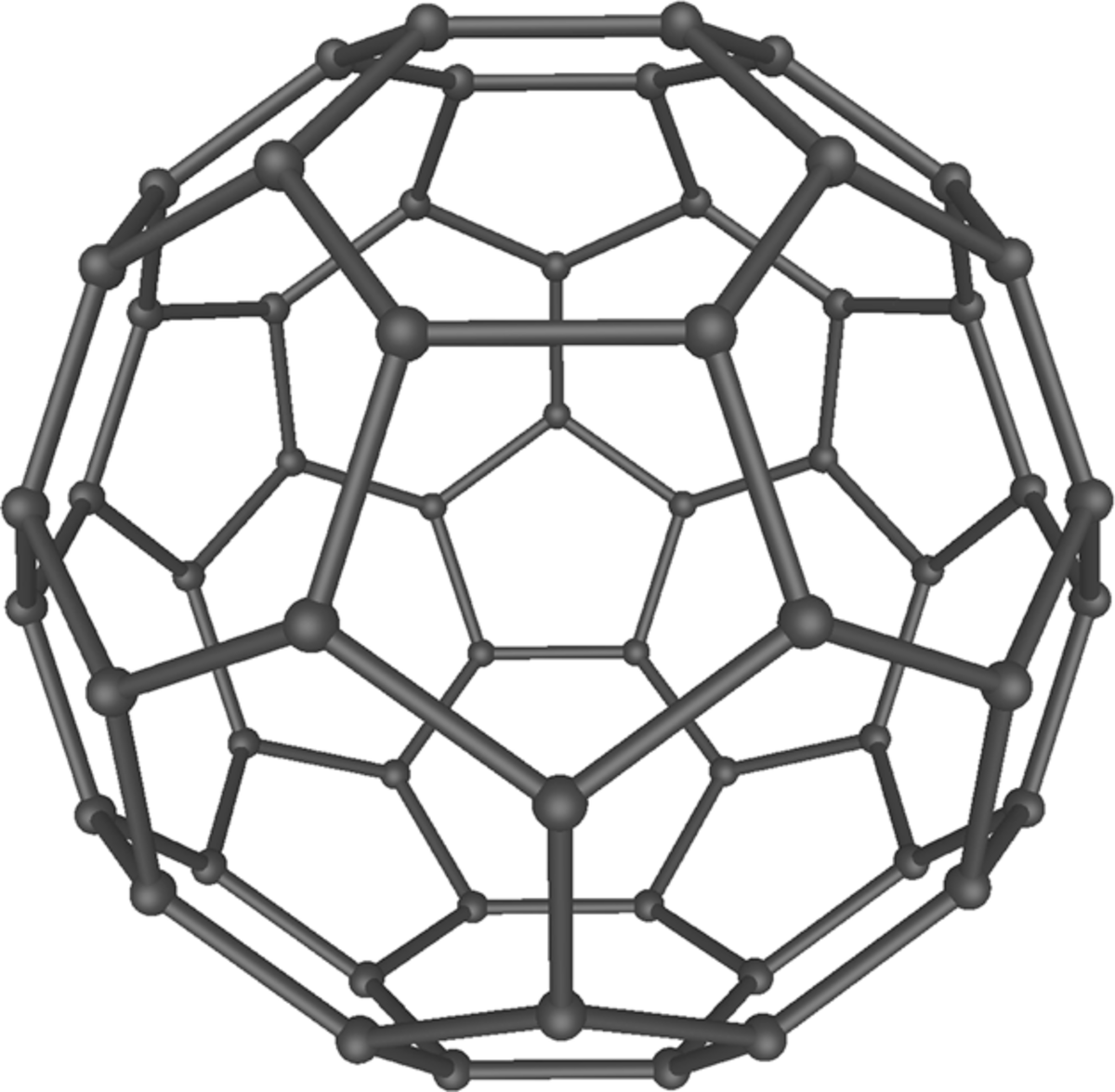
- Harold Kroto, Robert Curl et Richard Smalley découvrent les fullerènes, une large classe de molécules carbonés ressemblant aux dômes géodésiques de l'architecte Richard Buckminster Fuller.
- 1991
- Sumio Iijima utilise la microscopie électronique pour découvrir un type de fullerène cylindrique appelé nanotube de carbone, bien que des études dans ce domaine avaient été effectuées en 1951. Ce composé est très utilisé dans la nanotechnologie.
- 1995
- Eric Cornell et Carl Wieman produisent le premier condensat de Bose-Einstein, une substance qui possède des propriétés de la mécanique quantique à une échelle macroscopique.